本试题 “下图所示的实验,能达到实验目的的是[ ]A.验证化学能转化为电能B.验证铅蓄电池放电时Pb为负极C.验证铁发生析氢腐蚀D.验证AgCl 溶解度小于Ag2S” 主要考查您对溶度积常数
二次电池
原电池原理
金属的电化学腐蚀
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 溶度积常数
- 二次电池
- 原电池原理
- 金属的电化学腐蚀
在AgCl(s)
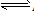 Ag+(aq)+Cl-(aq)中,当溶解速率与结晶速率相等时,达到平衡状态,Ksp(AgCl)=[ Ag+][ Cl-]为一常数,该常数称为难难溶电解质的溶度积常数,简称溶度积。用Ksp表示
Ag+(aq)+Cl-(aq)中,当溶解速率与结晶速率相等时,达到平衡状态,Ksp(AgCl)=[ Ag+][ Cl-]为一常数,该常数称为难难溶电解质的溶度积常数,简称溶度积。用Ksp表示(1)溶度积的通式:
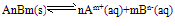 ,
,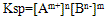
(2)溶度积规律:
①离子积:
 ,
,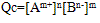
Qc为离子积,表达式中离子浓度是任意的,为此瞬间溶液的实际浓度,其值不确定,但对一难溶电解质,在一定温度下,Ksp为一定值。
②溶度积规则:
A. 当Qc>Ksp时,沉淀从溶液中析出来,体系不断析出沉淀,直至达到平衡(此时Qc=Ksp)
B. 当Qc=Ksp时,沉淀于饱和溶液平衡
C. 当Qc<Ksp时,溶液不饱和,若体系中有沉淀,则沉淀会溶解直至平衡(此时Qc=Ksp)。
(1)蓄电池:蓄电池是可以反复使用、放电后可以充电使活性物质复原、以便再重新放电的电池,也称二次电池。其广泛用于汽车、发电站、火箭等部门。由所用电解质的酸碱性质不同分为酸性蓄电池和碱性蓄电池。
①酸性铅蓄电池铅蓄电池由一组充满海绵状金属铅的铅锑合金格板做负极,由另一组充满二氧化铝的铅锑合金格板做正极,两组格板相间浸泡在电解质稀硫酸中,放电时,电极反应为:
负极:Pb+SO42-=PbSO4+2e- 正极:PbO2+SO42-十4H++2e-=PbSO4+2H2O
总反应:Pb+PbO2+2H2SO4=2PbSO4十2H2O
放电后,正负极板上都沉积有一层PbSO4,放电到一定程度之后又必须进行充电,充电时用一个电压略高于蓄电池电压的直流电源与蓄电池相接,将负极上的PbSO4还原成Pb,而将正极上的PbSO4氧化成PbO2,
充电时发生放电时的逆反应:阴极:PbSO4+2e-=Pb+SO42-阳极:PbSO4+2H2O=PbO2+SO42-+4H++2e- 总反应:2PbSO4+2H2O=Pb+PbO2+H2SO4
②碱性蓄电池日常生活中用的充电电池就属于这类。它的体积、电压都和干电池差不多,携带方便,使用寿命比铅蓄电池长得多,使用信当可以反复充放电上千次,但价格比较贵。商品电池中有镍-镉(Ni-Cd)和镍一铁(Ni-Fe)两类,它们的电池反应是:
Cd+2NiO(OH)+2H2O
 2Ni(OH)2+Cd(OH)2
2Ni(OH)2+Cd(OH)2 Fe+2NaO(OH)+2H2O
 2Ni(OH)2+Fe(OH)2
2Ni(OH)2+Fe(OH)2 反应是在碱性条件下进行的,所以叫碱性蓄电池。
(2)银锌蓄电池 银锌电池是一种高能电池,它质量轻、体积小,是人造卫星、宇宙火箭、空间电视转播站等的电源。目前,有一种类似干电池的充电电池,它实际是一种银锌蓄电池,电解液为KOH溶液。 常见的钮扣电池也是银锌电池,它用不锈钢制成一个由正极壳和负极盖组成的小圆盒,盒内靠正极盒一端充由Ag2O和少量石墨组成的正极活性材料,负极盖一端填充锌汞合金作负极活性材料,电解质溶液为KOH浓溶液,溶液两边用羧甲基纤维素作隔膜,将电极与电解质溶液隔开。
负极:Zn+2OH--2e-=Zn(OH)2
正极:Ag2O+H2O+2e-=2Ag+2OH-?
银锌电池跟铅蓄电池一样,在使用一段时间后就要充电,充电过程表示如下:
阳极:2Ag+2OH--2e-=Ag2O+H2O
阴极:Zn(OH)2+2e-=Zn+2OH-?
总反应式:Zn+Ag2O+H2O
 Zn(OH)2+2Ag
Zn(OH)2+2Ag 一粒钮扣电池的电压达1.59V,安装在电子表里可使用两年之久。
1.定义:将化学能转化为电能的装置。
2.工作原理:
以铜-锌原电池为例

(1)装置图:
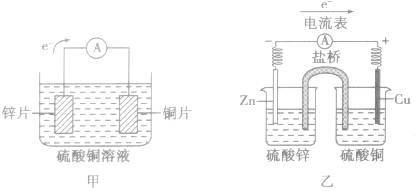
(2)原理图:
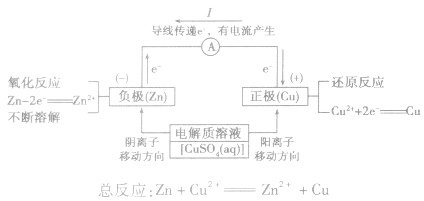
3.实质:化学能转化为电能。
4.构成前提:能自发地发生氧化还原反应。
5.电极反应:
负极:失去电子;氧化反应;流出电子
正极:得到电子;氧化反应;流入电子
6.原电池正负极判断的方法:
①由组成原电池的两级材料判断,一般是活泼金属为负极,活泼性较弱的金属或能导电的非金属为正极。
②根据电流方向或电子流动方向判断,电流是由正极流向负极,电子流动方向是由负极流向正极。
③根据原电池里电解质溶液内离子的定向移动方向,在原电池的电解质溶液中,阳离子移向正极,阴离子移向负极。
④根据原电池两级发生的变化来判断,原电池的负极总是失电子发生氧化反应,正极总是得电子发生还原反应。
⑤X极增重或减重:X极质量增加,说明溶液中的阳离子在X极(正极)放电,反之,X极质量减少,说明X极金属溶解,X极为负极。
⑥X极有气泡冒出:发生可析出氢气的反应,说明X极为正极。
⑦X极负极pH变化:析氢或吸氧的电极发生反应后,均能使该电极附近电解质溶液的pH增大,X极附近的pH增大,说明X极为正极。
原电池中的电荷流动:
在外电路(电解质溶液以外),电子(负电荷)由负极经导线(包括电流表和其他用电器)流向正极,使负极呈正电性趋势、正极呈负电性趋势。在内电路(电解质溶液中),阳离子(带正电荷)向正极移动,阴离子 (带负电荷)向负极移动。这样形成了电荷持续定向流动,电性趋向平衡的闭合电路。
金属的腐蚀:
1.金属腐蚀的概念金属与周围的气体或液体物质发生氧化还原反应而引起损耗的现象。
2.金属腐蚀的实质金属原子(M)失去电子而被氧化的过程。
M-ne-==M n+
金属的电化学腐蚀:
不纯的金属或合金因发生原电池反应而造成的腐蚀。最普遍的钢铁腐蚀是:
负极:2Fe-4e-=2Fe2+
正极:O2+2H2O+4e-=4OH- (注:在少数情况下,若周围介质的酸性较强,正极的反应是:2H++2e-=H2↑)
金属的腐蚀以电化腐蚀为主.例如,钢铁生锈的主要过程为
(1)吸氧腐蚀:金属在酸性很弱或中性溶液里,空气里的氧气溶解于金属表面水膜中而发生的电化腐蚀。
①发生条件:水膜的酸性很弱或呈中性
②反应本质:形成原电池
③铁为负极,(氧化反应);正极反应:(还原反应)
(2)析氢腐蚀:在酸性较强的溶液中发生电化腐蚀时放出氢气,这种腐蚀叫做析氢腐蚀。
①发生条件:水膜的酸性较强
②反应本质:形成原电池
③铁为负极,(氧化反应);正极反应:(还原反应)
钢铁的电化学腐蚀的两种类型:


金属腐蚀快慢的判断:
金属腐蚀的快慢与下列两个因素有关:
(1)与构成原电池的材料有关,两极材料的活泼性差别越大,电动势越大,氧化还原反应的速率越快,活泼金属被腐蚀的速率就越快。
(2)与金属所接触的电解质溶液的性质有关,活泼金属在电解质溶液中的腐蚀快于在非电解质溶液中的腐蚀,在强电解质溶液中的腐蚀快于在弱电解质溶液中的腐蚀。一般来说,可用下列原则判断:电解原理引起的腐蚀>原电池原理引起的腐蚀> 化学腐蚀>有防护措施的腐蚀
与“下图所示的实验,能达到实验目的的是[ ]A.验证化学能转化为电...”考查相似的试题有:
- 燃料电池突出的优点是不经过热能的中间形式而进行能量转化,现已广泛使用.如甲烷燃料电池,其电极反应为:负极:CH4+10OH-→C...
- 锂电池已经成为新一代实用化的蓄电池,该电池具有能量密度大、电压高的特性.锂离子电池放电时的电极反应式为负极反应:C6Li-...
- 一种碳纳米管(氢气)二次电池原理如右图,该电池的电解质为6mol·L—1KOH溶液,下列说法不正确的是 ( )A.储存H2的碳纳米管...
- 氢氧燃料电池是将H2和O2分别通入电池,穿过浸入20%~40%的KOH溶液的多孔碳电极,其电极反应式为H2+2OH--2e-==2H2O和O2+H2O+2e-...
- 下列各个装置中能组成原电池的是( )A.稀硫酸B.CuSO4溶液C.酒精溶液D. 稀硫酸 稀硫酸
- 下列有关说法错误的是A.反应NH3(g)+HCl(g)=NH4Cl(s)低温下能自发进行,说明该反应的△H
- 茫茫黑夜中,航标灯为航海员指明了方向。航标灯的电源必须长效、稳定。我国科技工作者研制出以铝合金、Pt-Fe合金网为电极材料...
- 被称之为“软电池”的纸质电池,采用一个薄层纸片作为传导体,在其一边镀锌,而在其另一边镀二氧化锰。在纸内的离子“流过”水和...
- 为防止海轮船体的腐蚀,应在船体水线以下位置嵌上一定数量的( )A.铜块 B.铅块C.锌块 D.钠块
- 图是钢铁在酸雨环境中腐蚀的示意图.有关说法正确的是( )A.铁被腐蚀发生还原还原反应B.正极上电极反应式为:2H2O+O2+4e-→...