本试题 “社会调查农民在购买、贮存、使用化肥、农药时应注意的事项及理由.注意事项理由(1)购买时要注意农药的名称、化学式以免买错(2)购买时要注意农药的生产日...” 主要考查您对化肥
物质的变质
物质的保存
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 化肥
- 物质的变质
- 物质的保存
化学肥料的概念:
化学肥料是指以矿物、空气、水做原料,经过化学加工制成含有植物生长所需的营养元素的物质,简称化肥。农作物所必需的营养元素有碳、氢、氧、氮、磷、钾、钙、镁等,其中氮、磷、钾需要量较大,因此氮肥、磷肥、钾肥是最主要的化学肥料。另外还有同时含有两种或两种以上营养元素的复合肥,植物生长过程中需要量比较少的微量元素肥料。
常见化学肥料:
1、氮肥
①作用:氮是合成蛋白质、核酸和叶绿素的重要元素,氮肥充足会使植物枝繁叶茂、果实硕大。缺少氮元素,会使植物生长发育迟缓或停滞,光合作用减慢等。外观表现为植株矮小,瘦弱,叶片发黄,严重时叶脉为棕色。
②氮肥的特性
a.氮盐与碱混合受热可产生一种无色、有刺激性气味的气体,它能使湿润的红色石蕊试纸变蓝。例如: NaOH+NH4NO3=NaNO3+H2O+NH3↑
检验按根离子(NH4+)时,需有可溶性碱和红色石蕊试纸。
b.氨水是氨气的水溶液,溶于水的氨气大部分与水反应生成一水合氨。一水合氨在水中发生电离,生成铵根离子和氢氧根离子。由于氨水中存在的阴离子全部是OH-,所以氨水呈碱性,一水合氨属于碱类。请注意,通常情况下氨水指氨气溶于水后生成的一水合氨(NH3·H2O),切勿将氨水的化学式写成NH4OH,因为氨水中没有NH4OH存在。
c.碳酸氢按受热分解:NH4HCO3==NH3↑+ CO2↑+H2O↑。
③氮的固定将氮气转化为氮的化合物的方法。如:豆科植物根部的根瘤菌能把空气中的氮气转化为含氮化合物,这类植物无需或只需少量使用氮肥。
2、磷肥
①作用:磷能促进作物生长,增强抗寒、抗旱能力。若缺乏磷元素,常表现为生长迟缓、产量降低,但磷过量则会引起作物贪青晚熟,结实率下降。外观表现为植株特别矮小,叶片出现紫色。
②常见磷肥有磷矿粉[Ca3(PO4)2]、钙镁磷肥(钙和镁的磷酸盐)、过磷酸钙[磷酸二氢钙Ca(H2PO4)2 和CaSO4的混合物]等。
3、钾肥
①作用:钾肥能保证各种代谢过程的顺利进行、促进植物生民、增强抗病虫害和抗倒伏能力。若缺乏钾元素,常表现为茎秆软弱、容易倒伏、叶片的边缘和尖端呈褐色,并逐渐焦枯。
②常见钾肥有硫酸钾(K2SO4)、氯化钾(KCl)和草木灰(主要成分为K2CO3)等。
(4)复合肥
含两种或两种以土营养元素的化肥。
①特点能同时均匀地供给作物几种养分,充分发挥营养元素间的互补作用,有效成分高。
②种类磷酸按〔磷酸二氢铵NH4H2PO4和磷酸氢二按 (NH4)2HPO4的混合物」、硝酸钾(KNO3)。
常见氮肥及性质:
化肥和农家肥的比较:
使用化肥、农药的利与弊:
①利:化肥、农药对提高农作物的产量具有重要的作用。
②弊:
a.不合理施用化肥会带来很多环境问题,一方面化肥中含有一些重金属元素、有毒有机物和放射性物质,施人后会引起潜在的土壤污染;另一方面化肥在施用过程中,因某些成分的积累、流失或变化,引起土壤酸化,水域中氮和磷含量升高,氮化物和硫化物气体排放等,造成土壤退化和水、大气环境的污染。
b.农药本身有毒,在杀灭病虫害的同时也带来了对自然环境的污染和对人体健康的危害。
使用化肥的注意事项:
①铰态氮肥不能与碱性物质(如碱、草木灰等)一起使用,因为铵态氮肥中的NH4+遇到OH-会生成易挥发的NH3,降低肥效。
②使用氨水或磷酸氢铵时要防止挥发,立即灌溉或用土盖上,人要站在上风口,因氨气对人的眼、鼻等膜有刺激作用。
③硝酸按受热易分解,在高温或猛烈撞击时易发生爆炸。所以当硝酸铵受潮结块时,不要用铁锤砸碎。
④硫酸按不易长时间使用,以免造成土壤酸性增强或土壤板结。
化肥鉴别的方法:
①一看、二闻、三溶看外观,氮肥、钾肥为白色晶体,磷肥是灰白色粉末;闻气味,碳酸氢按有强烈的氨味,可直接将它与其他氮肥相区别;加水溶解,氮肥、钾肥全部溶于水,磷肥大多不溶于水。铵盐的鉴别:(NH4)2SO4、NH4NO3等和熟石灰混合研磨,放出具有刺激性气味的氨气。
②氮肥的简易鉴别氮肥中的氨水呈液态,碳酸氧钱有强烈的氨味,据此可直接将它们与其他氮肥相区别。其他常见氮肥可按下列步骤鉴别:
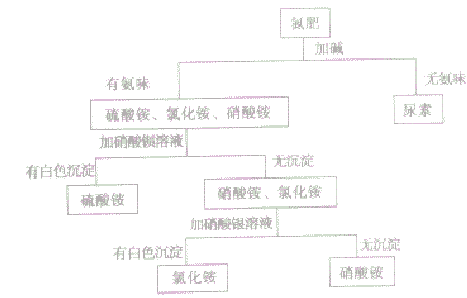
注意硫酸铵、氯化铵、硝酸铵同时鉴别时,不能先加硝酸银溶液鉴别氯化铵,因为硝酸银与硫酸铵反应,可能生成微溶物硫酸银,也可能出现沉淀。所以要区分含SO42-、Cl-和NO3-的三种物质时,一般是先加硝酸钡来鉴别出含有SO42-的物质,再加入硝酸银,鉴别出含有Cl-的物质,无现象的则是含有NO3-的物质。
③化肥鉴别歌鉴别化肥简易行,无锈铁片火烧红;化肥分别铁上放,各自现象皆不同;遇铁冒烟化成水,定是尿素不可疑;若是只熔不冒烟,刺鼻气味是磷铵;一阵烟后冒火星,必是硝铵显神通;铁上发出紫火焰,吱吱微响是硫铵;要想测知氯化铵,触铁味如浓盐酸;磷肥多为灰白色,置于红铁味难闻;放于红铁爆噼啪,无氨味者硫酸钾,氨化磷肥与有别,无烟臭气呛煞人;上述现象若不符,其中有诈须谨慎;认真鉴别把握准,防止上当把钱费。
盐的命名:
(1)只有两种元素组成的盐,读作“某化某”,如 NaCl读作氯化钠,AgI读作碘化银。
(2)构成中含有酸根的,读作“某酸某”。如Na2CO3、ZnSO4、AgNO3、KMnO4、KClO3分别读作:碳酸钠、硫酸锌、硝酸银、高锰酸钾、氯酸钾。
(3)含铵根的化合物,读作“某化铵”或“某酸铵”。如NH4Cl、(NH4)2SO4读作:氯化铵、硫酸铵。
(4)其他:Cu2(OH)2CO3读作“碱式碳酸铜”, NaHSO4读作“硫酸氢钠”, NaHCO3读作“碳酸氢钠”。
化学肥料是指以矿物、空气、水做原料,经过化学加工制成含有植物生长所需的营养元素的物质,简称化肥。农作物所必需的营养元素有碳、氢、氧、氮、磷、钾、钙、镁等,其中氮、磷、钾需要量较大,因此氮肥、磷肥、钾肥是最主要的化学肥料。另外还有同时含有两种或两种以上营养元素的复合肥,植物生长过程中需要量比较少的微量元素肥料。
常见化学肥料:
1、氮肥
①作用:氮是合成蛋白质、核酸和叶绿素的重要元素,氮肥充足会使植物枝繁叶茂、果实硕大。缺少氮元素,会使植物生长发育迟缓或停滞,光合作用减慢等。外观表现为植株矮小,瘦弱,叶片发黄,严重时叶脉为棕色。
②氮肥的特性
a.氮盐与碱混合受热可产生一种无色、有刺激性气味的气体,它能使湿润的红色石蕊试纸变蓝。例如: NaOH+NH4NO3=NaNO3+H2O+NH3↑
检验按根离子(NH4+)时,需有可溶性碱和红色石蕊试纸。
b.氨水是氨气的水溶液,溶于水的氨气大部分与水反应生成一水合氨。一水合氨在水中发生电离,生成铵根离子和氢氧根离子。由于氨水中存在的阴离子全部是OH-,所以氨水呈碱性,一水合氨属于碱类。请注意,通常情况下氨水指氨气溶于水后生成的一水合氨(NH3·H2O),切勿将氨水的化学式写成NH4OH,因为氨水中没有NH4OH存在。
c.碳酸氢按受热分解:NH4HCO3==NH3↑+ CO2↑+H2O↑。
③氮的固定将氮气转化为氮的化合物的方法。如:豆科植物根部的根瘤菌能把空气中的氮气转化为含氮化合物,这类植物无需或只需少量使用氮肥。
2、磷肥
①作用:磷能促进作物生长,增强抗寒、抗旱能力。若缺乏磷元素,常表现为生长迟缓、产量降低,但磷过量则会引起作物贪青晚熟,结实率下降。外观表现为植株特别矮小,叶片出现紫色。
②常见磷肥有磷矿粉[Ca3(PO4)2]、钙镁磷肥(钙和镁的磷酸盐)、过磷酸钙[磷酸二氢钙Ca(H2PO4)2 和CaSO4的混合物]等。
3、钾肥
①作用:钾肥能保证各种代谢过程的顺利进行、促进植物生民、增强抗病虫害和抗倒伏能力。若缺乏钾元素,常表现为茎秆软弱、容易倒伏、叶片的边缘和尖端呈褐色,并逐渐焦枯。
②常见钾肥有硫酸钾(K2SO4)、氯化钾(KCl)和草木灰(主要成分为K2CO3)等。
(4)复合肥
含两种或两种以土营养元素的化肥。
①特点能同时均匀地供给作物几种养分,充分发挥营养元素间的互补作用,有效成分高。
②种类磷酸按〔磷酸二氢铵NH4H2PO4和磷酸氢二按 (NH4)2HPO4的混合物」、硝酸钾(KNO3)。
常见氮肥及性质:
| 名称 | 化学式 | 性质 | 注意事项 |
| 尿素 | CO(NH2)2 | 白色或淡黄色晶体,易溶 于水,含氮量不超过46.7%, 肥效高且持久,对土壤无 不良影响 |
—— |
| 碳酸氢铵 | NH4HCO3 | 白色晶体,易溶于水,受潮 时常温下就能分解,温度越 高,分解越快,在土壤中不 残留有害杂质,含氮量低于 17.7% |
防分解,贮存和运输时 都要密封.不要受潮或暴 晒,施肥后掩盖或立即 灌溉,不要与碱性物质 混合使用 |
| 硝酸铵 | NH4NO3 | 白色晶体,易溶于水,高温 或受猛烈撞击时易爆炸,含 氮量低于35%,对土壤无不 良影响 |
不要与易燃物质或碱性 物质混合在一起,结块 时,不要用铁锤砸碎 |
| 硫酸铵 | (NH4)2SO4 | 白色固体,易溶于水,常温 下性质稳定,不宜长期大量 使用,否则会使土壤酸化、 板结硬化 |
不能与碱性物质混合, 不宜长期大量使用 |
| 氨水 | NH3·H2O | 氨气的水溶液,易挥发,显碱性 | 运愉、扩存、使用时要 防挥发 |
化肥和农家肥的比较:
| 所含元素种类少,但营养元素含量大 | 常含有多种营养元素,但营养元素含量较少 |
| 一般易溶于水,易被农作物吸收,肥效较快 | 一般较难溶于水,经腐熟后逐步转化为可溶于水、能被作物吸收的物质,肥效慢但肥期较长 |
| 便于工业生产,成本较高 | 便于就地取材,成本低廉 |
| 长期使用会破坏土壤的结构,使果蔬、谷物含有超量化肥,影响人体健康;化肥还会造成水体污染,引起水体富营养化 | 能改良土壤结构 |
使用化肥、农药的利与弊:
①利:化肥、农药对提高农作物的产量具有重要的作用。
②弊:
a.不合理施用化肥会带来很多环境问题,一方面化肥中含有一些重金属元素、有毒有机物和放射性物质,施人后会引起潜在的土壤污染;另一方面化肥在施用过程中,因某些成分的积累、流失或变化,引起土壤酸化,水域中氮和磷含量升高,氮化物和硫化物气体排放等,造成土壤退化和水、大气环境的污染。
b.农药本身有毒,在杀灭病虫害的同时也带来了对自然环境的污染和对人体健康的危害。
使用化肥的注意事项:
①铰态氮肥不能与碱性物质(如碱、草木灰等)一起使用,因为铵态氮肥中的NH4+遇到OH-会生成易挥发的NH3,降低肥效。
②使用氨水或磷酸氢铵时要防止挥发,立即灌溉或用土盖上,人要站在上风口,因氨气对人的眼、鼻等膜有刺激作用。
③硝酸按受热易分解,在高温或猛烈撞击时易发生爆炸。所以当硝酸铵受潮结块时,不要用铁锤砸碎。
④硫酸按不易长时间使用,以免造成土壤酸性增强或土壤板结。
化肥鉴别的方法:
①一看、二闻、三溶看外观,氮肥、钾肥为白色晶体,磷肥是灰白色粉末;闻气味,碳酸氢按有强烈的氨味,可直接将它与其他氮肥相区别;加水溶解,氮肥、钾肥全部溶于水,磷肥大多不溶于水。铵盐的鉴别:(NH4)2SO4、NH4NO3等和熟石灰混合研磨,放出具有刺激性气味的氨气。
②氮肥的简易鉴别氮肥中的氨水呈液态,碳酸氧钱有强烈的氨味,据此可直接将它们与其他氮肥相区别。其他常见氮肥可按下列步骤鉴别:

注意硫酸铵、氯化铵、硝酸铵同时鉴别时,不能先加硝酸银溶液鉴别氯化铵,因为硝酸银与硫酸铵反应,可能生成微溶物硫酸银,也可能出现沉淀。所以要区分含SO42-、Cl-和NO3-的三种物质时,一般是先加硝酸钡来鉴别出含有SO42-的物质,再加入硝酸银,鉴别出含有Cl-的物质,无现象的则是含有NO3-的物质。
③化肥鉴别歌鉴别化肥简易行,无锈铁片火烧红;化肥分别铁上放,各自现象皆不同;遇铁冒烟化成水,定是尿素不可疑;若是只熔不冒烟,刺鼻气味是磷铵;一阵烟后冒火星,必是硝铵显神通;铁上发出紫火焰,吱吱微响是硫铵;要想测知氯化铵,触铁味如浓盐酸;磷肥多为灰白色,置于红铁味难闻;放于红铁爆噼啪,无氨味者硫酸钾,氨化磷肥与有别,无烟臭气呛煞人;上述现象若不符,其中有诈须谨慎;认真鉴别把握准,防止上当把钱费。
盐的命名:
(1)只有两种元素组成的盐,读作“某化某”,如 NaCl读作氯化钠,AgI读作碘化银。
(2)构成中含有酸根的,读作“某酸某”。如Na2CO3、ZnSO4、AgNO3、KMnO4、KClO3分别读作:碳酸钠、硫酸锌、硝酸银、高锰酸钾、氯酸钾。
(3)含铵根的化合物,读作“某化铵”或“某酸铵”。如NH4Cl、(NH4)2SO4读作:氯化铵、硫酸铵。
(4)其他:Cu2(OH)2CO3读作“碱式碳酸铜”, NaHSO4读作“硫酸氢钠”, NaHCO3读作“碳酸氢钠”。
易变质的物质:
1. 由于吸水质量增加的物质:氢氧化钠固体,浓硫酸
2. 由于跟水反应质量增加的物质:氧化钙,氧化钠,硫酸铜
3. 由于和二氧化碳反应质量增加的物质:氢氧化钠,氢氧化钾,氢氧化钙
4. 由于挥发质量减少的物质:浓盐酸,浓硝酸,酒精,氨水
5. 由于风化质量减少的物质:碳酸钠晶体
氢氧化钠变质的知识归纳:
氢氧化钠变质主要考点包括:变质原因、检验变质的方法、检验变质的程度、 除去杂质得到就纯净的氢氧化钠。
1 、氢氧化钠变质的原因:
敞口放置, 与空气中的二氧化碳反应, 生成了碳酸钠。 2NaOH+CO 2 =Na 2 CO 3 +H 2 O
2 、检验氢氧化钠是否变质的方法: ( 分别滴加酸、碱、盐溶液,各为一种方法 )
①取少量样品于试管中, 滴加稀盐酸 ( 或者稀硫酸 ) , 如果产生气泡, 说明已变质。 Na 2 CO 3 +2HCl=2NaCl+H 2 O+CO 2 ↑
②取少量样品于试管中,滴加氢氧化钙溶液 ( 或者氢氧化钡溶液 ) ,如果产生白色 沉淀,说明已变质。 Na 2 CO 3 +Ca(OH) 2 =CaCO 3 ↓ +2NaOH
③取少量样品于试管中,滴加氯化钙溶液 ( 或者硝酸钙等其它可溶性钙盐、钡盐 溶液 ) Na 2 CO 3 +CaCl 2 =CaCO 3 ↓ +2NaCl
3 、检验氢氧化钠变质程度的方法:
取少量样品于试管中,滴加足量的 CaCl2 溶液,有白色沉淀生成;静置,像上层澄清液中滴加少量酚酞溶液,如果溶液变红色,说明溶液部分变质;如果溶液呈无色,说明氢氧化钠完全变质。
解释:碳酸钠溶液呈碱性,它的存在会影响到氢氧化钠的检验,所以在检验氢氧化钠前必须把碳酸钠除去。除去碳酸钠时不能用酸,因为酸会与氢氧化钠反应; 不能用碱,因为碱会与碳酸钠反应生成氢氧化钠,干扰原来氢氧化钠的检验。
4 、如何除去部分变质的氢氧化钠中的碳酸钠。 滴加适量氢氧化钙溶液至刚好无沉淀生成为止,然后过滤,就得到氢氧化钠溶液,再蒸发,就得到氢氧化钠固体。 Na 2 CO 3 +Ca(OH) 2 =CaCO 3 ↓ +2NaOH
除杂方法:除杂时为了不引入新杂质,如果除去阴离子,所选择试剂的阴离子 与主题物质一致。
氧化钙和氢氧化钙的变质:
(1)变质的原因
氧化钙在空气中敞口放置会与空气中的水蒸气反应生成氢氧化钙 CaO+H 2 O===Ca(OH) 2 , 氢氧化钙继续与空气中的二氧化碳反应生成碳酸钙。 Ca(OH) 2 +CO 2 ====CaCO 3 ↓+H 2 O
(2)检验变质后物质存在的方法:
氧化钙:
取少量变质后的固体放入烧杯中,加入水充分溶解,用手摸烧杯外壁有灼热感。
氢氧化钙:
(1)取变质后物质溶于水,向其中通入二氧化碳气体,有白色沉淀生成。
(2)取变质后物质溶于水,向其中滴加碳酸钠溶液,有白色沉淀生成。 碳酸钙:取少量变质后固体,向其中滴加稀盐酸,有气泡冒出。 CaCO3 +2HCl===CaCl2 +H2O+CO2 ↑
【特殊强调】:有氧化钙存在的情况下,初中阶段检验不出氢氧化钙的存在。因为氧化钙溶于水后会生成氢氧化钙,会干扰原来氢氧化钙的检验。
其它常见物质变质的知识小结:
NaOH在空气中变质:2NaOH+CO2==Na2CO3+H2O
检验: 取样滴加稀 HCl,若有气泡产生,则已经变质 (Na 2 CO 3 +2HCl===2NaCl+H 2 O+CO 2 ↑ )
消石灰 [Ca(OH)2] 放在空气中变质: Ca(OH) 2 +CO 2 ====CaCO 3 ↓ +H 2 O
检验: 取样滴加稀 HCl,若有气泡产生,则已经变质 (CaCO 3 +2HCl===CaCl 2 +H 2 O+CO 2 ↑ )
生石灰 (CaO) 暴露在空气中变质: CaO+H 2 O===Ca(OH) 2
检验: 取样用试管加热,若试管内壁有小水珠产生,则已变质 [Ca(OH) 2 = 加热 =CaO+H 2 O]
铁生锈:4Fe+3O 2 ===2Fe2O3
检验:观察颜色 , 若有红色粉末在表面, 则已变质
铜生锈:2Cu+O 2 +CO 2 +H 2 O===Cu 2 (OH) 2 CO 3
检验:观察颜色 , 若有绿色粉末在表面,则已变质。
1. 由于吸水质量增加的物质:氢氧化钠固体,浓硫酸
2. 由于跟水反应质量增加的物质:氧化钙,氧化钠,硫酸铜
3. 由于和二氧化碳反应质量增加的物质:氢氧化钠,氢氧化钾,氢氧化钙
4. 由于挥发质量减少的物质:浓盐酸,浓硝酸,酒精,氨水
5. 由于风化质量减少的物质:碳酸钠晶体
氢氧化钠变质的知识归纳:
氢氧化钠变质主要考点包括:变质原因、检验变质的方法、检验变质的程度、 除去杂质得到就纯净的氢氧化钠。
1 、氢氧化钠变质的原因:
敞口放置, 与空气中的二氧化碳反应, 生成了碳酸钠。 2NaOH+CO 2 =Na 2 CO 3 +H 2 O
2 、检验氢氧化钠是否变质的方法: ( 分别滴加酸、碱、盐溶液,各为一种方法 )
①取少量样品于试管中, 滴加稀盐酸 ( 或者稀硫酸 ) , 如果产生气泡, 说明已变质。 Na 2 CO 3 +2HCl=2NaCl+H 2 O+CO 2 ↑
②取少量样品于试管中,滴加氢氧化钙溶液 ( 或者氢氧化钡溶液 ) ,如果产生白色 沉淀,说明已变质。 Na 2 CO 3 +Ca(OH) 2 =CaCO 3 ↓ +2NaOH
③取少量样品于试管中,滴加氯化钙溶液 ( 或者硝酸钙等其它可溶性钙盐、钡盐 溶液 ) Na 2 CO 3 +CaCl 2 =CaCO 3 ↓ +2NaCl
3 、检验氢氧化钠变质程度的方法:
取少量样品于试管中,滴加足量的 CaCl2 溶液,有白色沉淀生成;静置,像上层澄清液中滴加少量酚酞溶液,如果溶液变红色,说明溶液部分变质;如果溶液呈无色,说明氢氧化钠完全变质。
解释:碳酸钠溶液呈碱性,它的存在会影响到氢氧化钠的检验,所以在检验氢氧化钠前必须把碳酸钠除去。除去碳酸钠时不能用酸,因为酸会与氢氧化钠反应; 不能用碱,因为碱会与碳酸钠反应生成氢氧化钠,干扰原来氢氧化钠的检验。
4 、如何除去部分变质的氢氧化钠中的碳酸钠。 滴加适量氢氧化钙溶液至刚好无沉淀生成为止,然后过滤,就得到氢氧化钠溶液,再蒸发,就得到氢氧化钠固体。 Na 2 CO 3 +Ca(OH) 2 =CaCO 3 ↓ +2NaOH
除杂方法:除杂时为了不引入新杂质,如果除去阴离子,所选择试剂的阴离子 与主题物质一致。
氧化钙和氢氧化钙的变质:
(1)变质的原因
氧化钙在空气中敞口放置会与空气中的水蒸气反应生成氢氧化钙 CaO+H 2 O===Ca(OH) 2 , 氢氧化钙继续与空气中的二氧化碳反应生成碳酸钙。 Ca(OH) 2 +CO 2 ====CaCO 3 ↓+H 2 O
(2)检验变质后物质存在的方法:
氧化钙:
取少量变质后的固体放入烧杯中,加入水充分溶解,用手摸烧杯外壁有灼热感。
氢氧化钙:
(1)取变质后物质溶于水,向其中通入二氧化碳气体,有白色沉淀生成。
(2)取变质后物质溶于水,向其中滴加碳酸钠溶液,有白色沉淀生成。 碳酸钙:取少量变质后固体,向其中滴加稀盐酸,有气泡冒出。 CaCO3 +2HCl===CaCl2 +H2O+CO2 ↑
【特殊强调】:有氧化钙存在的情况下,初中阶段检验不出氢氧化钙的存在。因为氧化钙溶于水后会生成氢氧化钙,会干扰原来氢氧化钙的检验。
其它常见物质变质的知识小结:
NaOH在空气中变质:2NaOH+CO2==Na2CO3+H2O
检验: 取样滴加稀 HCl,若有气泡产生,则已经变质 (Na 2 CO 3 +2HCl===2NaCl+H 2 O+CO 2 ↑ )
消石灰 [Ca(OH)2] 放在空气中变质: Ca(OH) 2 +CO 2 ====CaCO 3 ↓ +H 2 O
检验: 取样滴加稀 HCl,若有气泡产生,则已经变质 (CaCO 3 +2HCl===CaCl 2 +H 2 O+CO 2 ↑ )
生石灰 (CaO) 暴露在空气中变质: CaO+H 2 O===Ca(OH) 2
检验: 取样用试管加热,若试管内壁有小水珠产生,则已变质 [Ca(OH) 2 = 加热 =CaO+H 2 O]
铁生锈:4Fe+3O 2 ===2Fe2O3
检验:观察颜色 , 若有红色粉末在表面, 则已变质
铜生锈:2Cu+O 2 +CO 2 +H 2 O===Cu 2 (OH) 2 CO 3
检验:观察颜色 , 若有绿色粉末在表面,则已变质。
初中化学中常见物质的保存:
1.钠保存在煤油中
2.NaOH溶液用橡胶塞
3.硝酸用玻璃塞棕色瓶
4.硝酸银用棕色瓶
5.白磷保存在水中
物质保存中需注意:
一、 防挥发:
1 .油封:氨水,浓盐酸,浓硝酸等易挥发无机液体,在液面上滴 10 ~ 20 滴矿物油,可以 防止挥发(不可用植物油)。
2 .水封:二硫化碳中加 5mL 水,便可长期保存。汞上加水,可防汞蒸气进入空气。汞旁放 些硫粉,一但失落,散布硫粉使遗汞消灭于化学反应中。
3 .腊封:乙醚、乙醇、甲酸等比水轻的或易溶性挥发液体,以及萘、碘等易挥发固体,紧 密瓶塞,瓶口涂腊。 溴除进行原瓶腊封外,应将原瓶置于具有活性炭的塑料筒内, 筒口进行 腊封。
二、防潮:
1 .漂白粉、过氧化钠应该进行腊封,防止吸水分解或吸水爆炸。氢氧化钠易吸水潮解,应 该进行腊封; 硝酸铵、 硫酸钠易吸水结状, 倒不出来, 以至导致试剂瓶破裂, 也应严密腊封。
2 .碳化钙、无水硫酸铜、五氧化二磷、硅胶极易吸水变质,红磷易被氧化,然后吸水生成 偏磷酸,以上各物均应存放在干燥器中。
3 .浓硫酸虽应密闭,防止吸水,但因常用,故宜放磨口瓶中,磨口瓶塞应该原配,切勿对调。
4 .“ 特殊药品 ” 的地下室,下层布块灰,中层布熟石灰上层布双层柏油纸,方可存放药物。
三、防变质:
1 .防氧化:亚硫酸钠、硫酸亚铁、硫代硫酸钠均易被氧化,瓶口应涂腊。
2 .防碳酸化:硅酸钠、过氧化钠、苛性碱均易吸收二氧化碳,应该涂腊。
3 .防风化:晶体碳酸钠、晶体硫酸铜应进行腊封,存放在地下室中。
4 .防分解:碳酸氢铵、浓硝酸受热易分解,涂腊后,存放在地下室中。
5 .活性炭能吸附多种气体而变质,(木炭亦同),应放在干燥器中。
6 .黄磷遇空气易自燃,永远保存水中,每 15 天查水一次:磷试剂瓶中加水、置于有水水 糟中,上加钟罩封闭。
7 .钾、钠保存在火油中。
8.硫酸亚铁溶液中滴几滴稀硫酸,加入过量细铁粉,进行腊封。
9 .葡萄糖溶液容易霉变,稍加几滴甲醛即可保存。
10 .甲醛易聚合,应开瓶后立即加少量甲醇;乙醛则加乙醇。
四、防光:
1 .硝酸银,浓硝酸及大部份有机药品应该放在棕色瓶中。
2 .硝酸盐存放在地下室中既防热,又防光、防火还能防震。
3 .有机试剂橱窗一律用黑漆涂染。
4 .实验室用色布窗帘,内红外黑双层。
五、防毒害:
1 .磷、硝酸银、氯酸钾、氯化汞等剧毒物放地下室内,双人双锁,建立档案,呈批取用, 使用记载,定期检查。
2 .磷化钙、磷化铝吸水后放出剧毒性磷化氢,应放在干燥器中保存,贴上红色标签。
3 .由于没有通风橱,经常在地面布石灰,吸附某些毒害气相物质。
4 .浓酸,浓碱、溴、酚等腐蚀的药物,使用红色标签,以示警戒。
六、防震:
1 .硝酸铵震动易爆炸,放地下室中。
2 .自制的大晶体明矾、大晶体硫酸铜,用软纸垫包放大口试剂瓶中,进行缓冲,并按 “ 四位 数字 ” 进行编号入厨。
1.钠保存在煤油中
2.NaOH溶液用橡胶塞
3.硝酸用玻璃塞棕色瓶
4.硝酸银用棕色瓶
5.白磷保存在水中
物质保存中需注意:
一、 防挥发:
1 .油封:氨水,浓盐酸,浓硝酸等易挥发无机液体,在液面上滴 10 ~ 20 滴矿物油,可以 防止挥发(不可用植物油)。
2 .水封:二硫化碳中加 5mL 水,便可长期保存。汞上加水,可防汞蒸气进入空气。汞旁放 些硫粉,一但失落,散布硫粉使遗汞消灭于化学反应中。
3 .腊封:乙醚、乙醇、甲酸等比水轻的或易溶性挥发液体,以及萘、碘等易挥发固体,紧 密瓶塞,瓶口涂腊。 溴除进行原瓶腊封外,应将原瓶置于具有活性炭的塑料筒内, 筒口进行 腊封。
二、防潮:
1 .漂白粉、过氧化钠应该进行腊封,防止吸水分解或吸水爆炸。氢氧化钠易吸水潮解,应 该进行腊封; 硝酸铵、 硫酸钠易吸水结状, 倒不出来, 以至导致试剂瓶破裂, 也应严密腊封。
2 .碳化钙、无水硫酸铜、五氧化二磷、硅胶极易吸水变质,红磷易被氧化,然后吸水生成 偏磷酸,以上各物均应存放在干燥器中。
3 .浓硫酸虽应密闭,防止吸水,但因常用,故宜放磨口瓶中,磨口瓶塞应该原配,切勿对调。
4 .“ 特殊药品 ” 的地下室,下层布块灰,中层布熟石灰上层布双层柏油纸,方可存放药物。
三、防变质:
1 .防氧化:亚硫酸钠、硫酸亚铁、硫代硫酸钠均易被氧化,瓶口应涂腊。
2 .防碳酸化:硅酸钠、过氧化钠、苛性碱均易吸收二氧化碳,应该涂腊。
3 .防风化:晶体碳酸钠、晶体硫酸铜应进行腊封,存放在地下室中。
4 .防分解:碳酸氢铵、浓硝酸受热易分解,涂腊后,存放在地下室中。
5 .活性炭能吸附多种气体而变质,(木炭亦同),应放在干燥器中。
6 .黄磷遇空气易自燃,永远保存水中,每 15 天查水一次:磷试剂瓶中加水、置于有水水 糟中,上加钟罩封闭。
7 .钾、钠保存在火油中。
8.硫酸亚铁溶液中滴几滴稀硫酸,加入过量细铁粉,进行腊封。
9 .葡萄糖溶液容易霉变,稍加几滴甲醛即可保存。
10 .甲醛易聚合,应开瓶后立即加少量甲醇;乙醛则加乙醇。
四、防光:
1 .硝酸银,浓硝酸及大部份有机药品应该放在棕色瓶中。
2 .硝酸盐存放在地下室中既防热,又防光、防火还能防震。
3 .有机试剂橱窗一律用黑漆涂染。
4 .实验室用色布窗帘,内红外黑双层。
五、防毒害:
1 .磷、硝酸银、氯酸钾、氯化汞等剧毒物放地下室内,双人双锁,建立档案,呈批取用, 使用记载,定期检查。
2 .磷化钙、磷化铝吸水后放出剧毒性磷化氢,应放在干燥器中保存,贴上红色标签。
3 .由于没有通风橱,经常在地面布石灰,吸附某些毒害气相物质。
4 .浓酸,浓碱、溴、酚等腐蚀的药物,使用红色标签,以示警戒。
六、防震:
1 .硝酸铵震动易爆炸,放地下室中。
2 .自制的大晶体明矾、大晶体硫酸铜,用软纸垫包放大口试剂瓶中,进行缓冲,并按 “ 四位 数字 ” 进行编号入厨。
发现相似题
与“社会调查农民在购买、贮存、使用化肥、农药时应注意的事项及...”考查相似的试题有:
- 下列物质中,属于复合肥料的是( )A.硫酸钾、K2SO4B.硝酸钾、KNO3C.尿素、CO(NH2)2D.磷酸二氢钙、Ca(H2PO4)2
- 农作物生长需要不同肥料,下列属于复合肥的是( )A.碳酸氢铵(NH4HCO3)B.氯化钾(KCl)C.磷酸二氢铵(NH4H2PO4)D.尿素...
- 下列化肥中,属于钾肥的是( )A.NH4ClB.CO(NH2)2C.K2CO3D.Ca(H2PO4)2
- 植物缺钾容易倒伏,这时需施用的化肥是( )A.KClB.NH4HCO3C.CO(NH2)2D.Ca(H2PO4)2
- 小亮设计如图所示装置进行趣味实验。(1)使用甲装置进行实验时,将滴管中的物质挤入烧杯中,然后打开止水夹,可以观察到烧瓶...
- 下列各物质的俗名与化学式对应关系不正确的是 A.食盐:NaClB.纯碱:NaOHC.小苏打:NaHCO3D.熟石灰:Ca(OH)2
- 复分解反应探究的是酸、碱、盐等化合物在溶液中相互反应的情况。回答下列问题:书写方程式:①氢氧化钠溶液与稀盐酸混合:____...
- 科学探究中常用到推理的方法。根据下列实验事实推出结论正确的是( )编号实验事实实验结论A某溶液使酚酞溶液变红该溶液一定...
- (10无锡24)在一定条件下,下列转化不能由一步反应实现的是A.CuSO4——FeSO4B.Ca(HCO3)2----CaCO3C.C—Na2CO3D.Na2CO3—-NaOH
- 下列各酸溶液,经敞口存放一段时间后,溶液变稀,但溶液质量减少的是( )A.浓硫酸B.稀硫酸C.浓盐酸D.稀盐酸