本试题 “化学就在我们身边,它与我们生产、生活息息相关.请从①稀有气体、②石灰石、③氧气、④明矾中选择符合题意的物质,并用其序号填空.(1)可用作工业炼铁原料之一...” 主要考查您对水的净化
金属的冶炼(铁的冶炼)
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 水的净化
- 金属的冶炼(铁的冶炼)
定义:
清除水中不好的或不需要的杂质,使水达到纯净的程度。
四种净化水的方法,原理,作用:
| 净化水的方法 | 原理 | 作用 |
| 沉淀 | 食难溶性的杂质沉淀下来,并与水分层 | 使难溶性大颗粒沉降或加入明矾,形成的胶状物吸附杂质沉降 |
| 过滤 | 把液体与难溶于液体的固体物质分离 | 除去难溶性杂质 |
| 吸附 | 利用物质的吸附作用,吸附水中一些难溶性杂质,臭味和色素 | 除去难溶性杂质,部分可溶性杂质,臭味和色素 |
| 蒸馏 | 通过加热的方法使水变成水蒸气后冷凝成水 | 除去可溶性杂质,使硬水软化 |
水净化的方法:
吸附,沉淀,过滤,蒸馏,杀菌
吸附:常用明矾和活性炭,明矾溶于水后形成胶状物吸附水中的悬浮物,
活性炭不仅可以吸附水中的悬浮物,还可以吸附在水中有异味的物质和色素
沉淀:水中悬浮物别吸附后形成密度大的颗粒,从而使杂质沉淀
过滤:除去水中不溶性的杂质
蒸馏:除去可溶性杂质的方法
杀菌:常用杀毒剂:漂白粉,氯气以及新型消毒剂二氧化氯等
吸附、沉淀、过滤和蒸馏中单一操作净化程度较高的是蒸馏。综合运用时,按吸附→沉淀→过滤→蒸馏的顺序操作净化效果更好
加絮凝剂(明矾)与活性炭净水的比较:
| 净化水的方法 | 原理 | 能除去的杂质 |
| 明矾净水 | 明研溶于水后形成胶状物质,对杂质进行吸附,将微小颗粒吸附在一起形成大的固体颗粒而沉阵下来 | 不溶于水的微小固体颗粒 |
| 活性炭净水 | 利用内部疏松多孔的结构来吸附水中的微小颗粒和一些可溶于水的杂质 | 不溶于水的微小固体颗粒和部分能溶于水的杂质以及气味,颜色等 |
自来水厂净化水的过程图及步骤
1、净化过程图
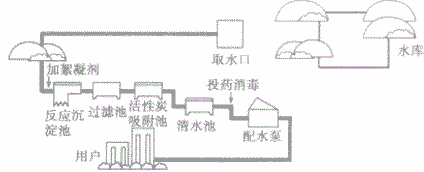
2、自来水净化步骤
①从水库中取水。
②加絮凝剂(主要是明矾),使悬浮的小颗粒状杂质被吸附凝聚。
③在反应沉淀池中沉降分离,使水澄清
④将沉淀池中流出的较澄清的水通入过滤池中,进一步除去不溶性杂质。
⑤再将水引人活性炭吸附池中,除去水中的臭味和残留的颗粒较小的不溶性杂质。
⑥细菌消毒(常用通入氯气的办法)。它是一个化学变化过程,因为除去病菌的过程.就是把病菌变成其他物质的过程。
⑦杀菌后的水就是洁净、可以饮用的自来水,通过配水泵供给用户,但水中仍然含有可以溶于水的一些杂质,所以还是混合物。
金属冶炼:
金属冶炼是把金属从化合态变为游离态的过程
矿石
①工业上能用来提炼金属的矿物叫做矿石。
②常见的矿石赤铁矿(Fe2O3)、黄铁矿(FeS2)、褐铁矿(Fe2O3·xH2O)、水铝石(Al2O3·H2O)、菱铁矿(主要成分是FeCO3)、磁铁矿(Fe3O4)、方铅矿(PbS)、孔雀石 [Cu2(OH)2CO3]、赤铜矿(Cu2O)、铝土矿(主要成分是Al2O3)、黄铜矿(主要成分是CuFeS2)、辉铜矿(主要成分是Cu2S)。
铁的冶炼
①原理:把铁矿石冶炼成铁是一个复杂的过程,其主要的反应原理是:
在高温下,利用还原剂一氧化碳把铁从铁矿石里还原出来,其反应的化学方程式是: Fe2O3+3CO 2Fe+3CO2
2Fe+3CO2
②炼铁的原料及作用:
铁矿石:提供原料
焦炭:提供能量,产生还原剂
石灰石:将矿石中的二氧化硅转变为炉渣。
③设备:高炉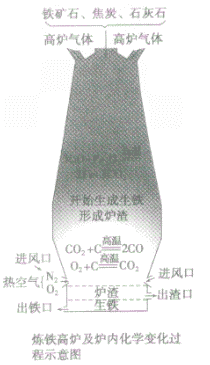
④高炉内有关反应:
a.产生CO提供能量:C+O2 CO2;CO2+C
CO2;CO2+C 2CO
2CO
b.在高温下用CO将Fe从Fe2O3中还原出来:3CO+ Fe2O3 2Fe + 3CO2
2Fe + 3CO2
c.用石灰石将矿石中的SiO2转变为炉渣除去。
CaCO3 CaO+CO2↑,CaO+SiO2
CaO+CO2↑,CaO+SiO2 CaSiO3
CaSiO3
⑤产品:生铁
炼铁高炉中出铁口低于出渣口的原因:
炼铁高炉中出铁口与出渣口的高低取决于铁水和炉渣的密度〔铁水的密度大于炉渣的密度)。
金属的冶炼方法:
①热分解法(适用于Hg,Ag不活泼的金属的冶炼,加热使其氧化物分解) 如:
2HgO=Hg+O2↑
②热还原法(适用于金属活动性顺序表中,Zn- Cu金属的冶炼)
a.用H2作还原剂(优点:制得金属纯度高,污染小) 如:Fe3O4+4H2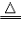 3Fe+4H2O
3Fe+4H2O
b.用焦炭、一氧化碳作还原剂(易混入杂质,污染大气,适合工业化大规模生产) 如:
炼铁的反应方程式为Fe2O3+3CO 2Fe +3CO2
2Fe +3CO2
炼锌的反应万程式为2ZnO+C 2Zn+CO2↑
2Zn+CO2↑
c.用Al作还原剂(铝热剂用来焊接铁轨) 如:
8Al+3Fe3O4 9Fe+4Al2O3
9Fe+4Al2O3
d.电解法(适用于活泼金属Na,Mg等的冶炼) 如:
2NaCl(熔融) 2Na+Cl2↑ ;MgCl2(熔融)
2Na+Cl2↑ ;MgCl2(熔融) Mg+Cl2↑
Mg+Cl2↑
e.湿法冶金(从溶液中通过化学反应来获取金属) 如:
Fe+CuSO4==Cu+FeSO4
金属冶炼是把金属从化合态变为游离态的过程
矿石
①工业上能用来提炼金属的矿物叫做矿石。
②常见的矿石赤铁矿(Fe2O3)、黄铁矿(FeS2)、褐铁矿(Fe2O3·xH2O)、水铝石(Al2O3·H2O)、菱铁矿(主要成分是FeCO3)、磁铁矿(Fe3O4)、方铅矿(PbS)、孔雀石 [Cu2(OH)2CO3]、赤铜矿(Cu2O)、铝土矿(主要成分是Al2O3)、黄铜矿(主要成分是CuFeS2)、辉铜矿(主要成分是Cu2S)。
铁的冶炼
①原理:把铁矿石冶炼成铁是一个复杂的过程,其主要的反应原理是:
在高温下,利用还原剂一氧化碳把铁从铁矿石里还原出来,其反应的化学方程式是: Fe2O3+3CO
 2Fe+3CO2
2Fe+3CO2 ②炼铁的原料及作用:
铁矿石:提供原料
焦炭:提供能量,产生还原剂
石灰石:将矿石中的二氧化硅转变为炉渣。
③设备:高炉

④高炉内有关反应:
a.产生CO提供能量:C+O2
 CO2;CO2+C
CO2;CO2+C 2CO
2COb.在高温下用CO将Fe从Fe2O3中还原出来:3CO+ Fe2O3
 2Fe + 3CO2
2Fe + 3CO2 c.用石灰石将矿石中的SiO2转变为炉渣除去。
CaCO3
 CaO+CO2↑,CaO+SiO2
CaO+CO2↑,CaO+SiO2 CaSiO3
CaSiO3⑤产品:生铁
炼铁高炉中出铁口低于出渣口的原因:
炼铁高炉中出铁口与出渣口的高低取决于铁水和炉渣的密度〔铁水的密度大于炉渣的密度)。
金属的冶炼方法:
①热分解法(适用于Hg,Ag不活泼的金属的冶炼,加热使其氧化物分解) 如:
2HgO=Hg+O2↑
②热还原法(适用于金属活动性顺序表中,Zn- Cu金属的冶炼)
a.用H2作还原剂(优点:制得金属纯度高,污染小) 如:Fe3O4+4H2
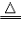 3Fe+4H2O
3Fe+4H2O b.用焦炭、一氧化碳作还原剂(易混入杂质,污染大气,适合工业化大规模生产) 如:
炼铁的反应方程式为Fe2O3+3CO
 2Fe +3CO2
2Fe +3CO2炼锌的反应万程式为2ZnO+C
 2Zn+CO2↑
2Zn+CO2↑ c.用Al作还原剂(铝热剂用来焊接铁轨) 如:
8Al+3Fe3O4
 9Fe+4Al2O3
9Fe+4Al2O3 d.电解法(适用于活泼金属Na,Mg等的冶炼) 如:
2NaCl(熔融)
 2Na+Cl2↑ ;MgCl2(熔融)
2Na+Cl2↑ ;MgCl2(熔融) Mg+Cl2↑
Mg+Cl2↑ e.湿法冶金(从溶液中通过化学反应来获取金属) 如:
Fe+CuSO4==Cu+FeSO4
发现相似题
与“化学就在我们身边,它与我们生产、生活息息相关.请从①稀有气...”考查相似的试题有:
- (1)今年以来,咸潮已成为珠江河口地区严重的环境问题之一,它对居民生活用水、农业用水以至城市工业生产及其发展都有相当大...
- 国家颁布的新版《生活饮用水卫生标准》包含以下内容:指标检测项目及单位限值微生物指标总大肠杆菌群(MPN/100mL)不得检出感...
- 某山区所饮用的水常是河水,由于河水中常含有大量的泥沙、悬浮物和细菌等杂质.可用次氯酸(HClO)杀死细菌,将漂白粉(主要...
- 小发收集到一瓶浑浊的河水,他要模拟自来水厂的净水过程,最终制成蒸馏水.其实验过程如下所示.请回答以下问题.(1)A物质...
- 人们的生活与化学密切相关.根据所学知识,回答下列问题.(1)小刚为净化收集到的雨水,自制了一个如右图所示的简易净水器,...
- 某同学要净化一杯浑浊的水.(1)向浑浊的水中加入一定量的明矾,搅拌后静置一段时间,观察到现象______,(2)实验室现有下...
- 净化水的方法有____________、____________、____________和____________。
- 如图是与水有关的3个实验.请回答下列问题:(1)A中烧瓶里的水只发生了______变化(填“物理”或“化学”).(2)B中试管1内气...
- 下列关于废旧手机中的金属材料回收利用的说法不正确的是( )A.可以节约金属资源B.可以节约冶炼相关金属所消耗的能源C.可以...
- 下图为某化工企业生产流程示意图:下列说法正确的是A.钛酸亚铁(FeTiO3)中钛元素为+3价B.①中反应方程式为:2FeTiO3+6C+7Cl...