本试题 “下列推断合理的是[ ]A.明矾[KAl(SO4)2·12H2O]在水中能形成Al(OH)3胶体,可用作净水剂B.金刚石是自然界中硬度最大的物质,不可能与氧气发生反应C.浓H2SO4有...” 主要考查您对铝盐(铝离子)
二氧化硫
(浓)硫酸
碳单质及化合物
水的净化与处理
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 铝盐(铝离子)
- 二氧化硫
- (浓)硫酸
- 碳单质及化合物
- 水的净化与处理
铝盐:
铝盐是指正三价铝离子和酸根阴离子组成的盐,一般来说呈白色或无色晶体,溶于水,个别不溶于水。
常用的铝盐主要有三氯化铝、硫酸铝和明矾。
(1)与碱反应:Al3++3OH-(少量)==Al(OH)3↓
Al3++4OH-(过量)== AlO2-+2H2O
(2)Al3++3AlO2-+6H2O==4Al(OH)3↓
铝盐的性质:
Al3+易水解,显酸性Al3++3H2O==Al(OH)3+3H+
(1)与碱反应:Al3++3OH-(少量)==Al(OH)3↓
Al3++4OH-(过量)==AlO2-+2H2O
(2)易发生双水解:Al3++3AlO2-+6H2O==4Al(OH)3↓
铝盐与强碱溶液作用生成Al(OH)3沉淀的计算
反应关系如下:
(1)Al3++3OH-==Al(OH)3(生成沉淀)
(2)Al(OH)3+OH-==AlO2-+2H2O(沉淀溶解)
(3)Al3++4OH-==AlO2-+2H2O(生成沉淀,又恰好溶解)
分析以上三个化学反应方程式,所得Al(OH)3沉淀的物质的量与n(Al3+)、n(OH-)的关系为:
当 ≤3时,所得沉淀的物质的量:n[Al(OH)3]=
≤3时,所得沉淀的物质的量:n[Al(OH)3]=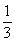 n(OH-)
n(OH-)
当 ≥4时,所得沉淀的物质的量:n[Al(OH)3]=0
≥4时,所得沉淀的物质的量:n[Al(OH)3]=0
当3< <4时,所得沉淀的物质的量:n[Al(OH)3]=4n(Al3+)-n(OH-)
<4时,所得沉淀的物质的量:n[Al(OH)3]=4n(Al3+)-n(OH-)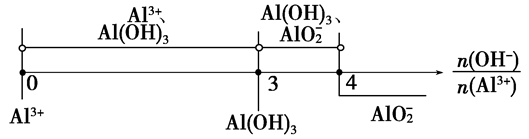
2、有关Al(OH)3的图像分析
①向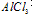 溶液中滴加
溶液中滴加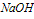 溶液
溶液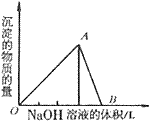
O~A段: 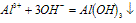
A~B段: 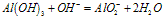
②向强碱溶液中滴入铝盐溶液 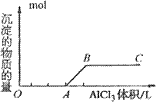
O~A段: 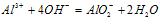
A~B段: 
③向铝盐溶液中滴入氨水或向氨水中滴加铝盐溶液
A. 向铝盐中滴加氨水时,当氨水增加到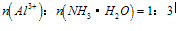 时,产生最大沉淀量
时,产生最大沉淀量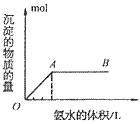
B. 向氨水中滴加铝盐溶液时,开始时氨水过量,如图所示 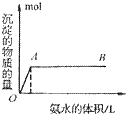
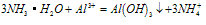
分析得:氢氧化铝不溶于弱碱氨水中。
④向偏铝酸盐溶液中滴入强酸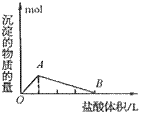
O~A段:
O~B段: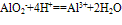
⑤向盐酸中滴加偏铝酸盐溶液 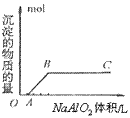
O~A段: 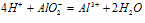
A~B段: 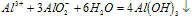
“铝三角”关系:
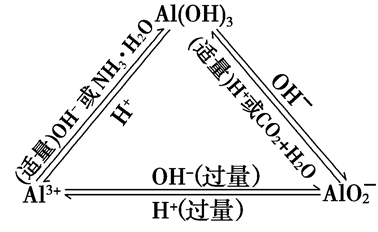
Al3++3OH-===Al(OH)3↓
Al(OH)3+OH-===AlO2-+2H2O
Al3++4OH-===AlO2-+2H2O
AlO2-+2H2O+CO2===Al(OH)3↓+HCO3-
AlO2-+H++H2O===Al(OH)3↓
AlO2-+4H+===Al3++2H2O
典型例题解析:
在50mLbmol·L-1的AlCl3溶液中加入50mLamol·L-1NaOH溶液。
(1)当a≤3b时,生成Al(OH)3沉淀的物质的量为________。
(2)当a、b满足________条件时,无沉淀产生。
(3)当a、b满足________条件时,先有沉淀生成,后又有部分沉淀溶解,此时Al(OH)3的质量为________g。
解析:依题意知,在AlCl3溶液中加入NaOH溶液有如下两个反应发生: AlCl3+3NaOH===Al(OH)3↓+3NaCl ①
AlCl3+4NaOH===NaAlO2+3NaCl+2H2O ②
根据以上两反应可以看出:
(1)当a≤3b时,只发生第一个反应,此时NaOH不足量,产生沉淀的量取决于NaOH。3n[Al(OH)3]=n(NaOH)?。所以答案为0.05a/3mol。
(2)如果无沉淀生成,Al元素全部以AlO2-形式存在。 n(AlCl3)∶n(NaOH)≤1∶4,即a∶b≥4∶1,所以答案为a≥4b。
(3)此种情况应当是两个反应均发生,铝元素以Al(OH)3和AlO2-两种形式存在。符合关系: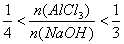 即
即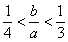 ,整理得:3b<a<4b或
,整理得:3b<a<4b或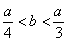 。
。
求沉淀的量的方法很多。
解法一:联立方程法。
设反应①中,AlCl3物质的量为x,则Al(OH)3为x,NaOH为3x。
反应②中AlCl3物质的量为y,NaOH为4y。 
解得x=(0.2b-0.05a)mol=0.05(4b-a)mol。 m[Al(OH)3]=78g·mol-1×0.05(4b-a)mol=3.9(4b-a)g。
解法二:守恒法。此种条件下,溶液中的离子有Na+、Cl-、AlO2-。
n(AlO2-)=n(Na+)-n(Cl-)=0.05amol-0.05×3bmol。
n[Al(OH)3]=n(Al3+)总-n(AlO2-)=0.05bmol-(0.05amol-0.15bmol)=(0.2b-0.05a)mol=0.05(4b-a)mol。
m[Al(OH)3]=78g·mol-1×0.05(4b-a)mol =3.9(4b-a)g。
【答案】 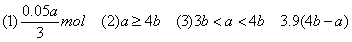
①化学式:SO2
②分子结构:SO2是由极性键形成的极性分子,因此易溶于水,其晶体为分子晶体。
二氧化硫的物理性质和化学性质:
1.物理性质:
SO2是无色、有刺激性气味的有毒气体,密度比空气大,易溶于水(常温常压下,1体积水大约溶解40体积的SO2),易液化(沸点-10℃)。
2.化学性质
(1)具有酸性氧化物的通性
①将SO2通入紫色石蕊试液中,试液变红。
②能与碱性氧化物、碱及某些盐反应。如:
(2)还原性 

(3)弱氧化性 
(4)漂白性(不能漂白酸碱指示剂) 能和某些有色物质化合生成无色物质,生成的无色物质不稳定,易分解而恢复原色,因此,SO2的漂白并不彻底。在中学化学常见试剂中,能用SO2漂白的只有品红溶液,品红溶液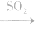 无色溶液
无色溶液 恢复原色。
恢复原色。
SO2与一些物质反应的实验现象:


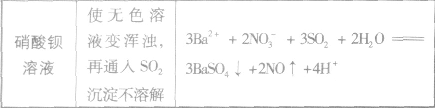
SO2与强碱反应后固体成分的确定:
SO2与强碱(如NaOH)溶液发生反应后的固体成分取决于二者的用量。遇到类似的问题,可以采用数轴分析法讨论。设SO2的物质的量为n(SO2),NaOH物质的量为n(NaOH),数轴代表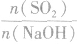 ,如下数轴所示:
,如下数轴所示: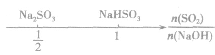
分析数轴可得:
(1)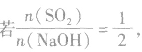 则固体物质为Na2SO3,
则固体物质为Na2SO3,
(2)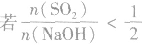 ,则固体物质为NaOH 和Na2SO3.
,则固体物质为NaOH 和Na2SO3.
(3)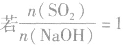 ,则同体物质为NaHSO3
,则同体物质为NaHSO3
(4)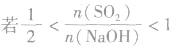 ,则固体物质为Na2SO3和NaHSO3,
,则固体物质为Na2SO3和NaHSO3,
(5)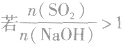 ,则固体物质为NaHSO3。
,则固体物质为NaHSO3。
二氧化硫的制备:
工业制法:

实验室制法:
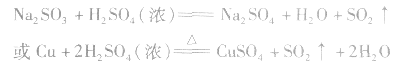
(1)收集:向上排空气法。
(2)检验:品红溶液。SO2是中学阶段学到的唯一种既能使品红褪色,加热后又能使其恢复原色的气体。
(3)尾气处理:用NaOH溶液吸收。
二氧化硫的用途:
工业上用二氧化硫漂白纸浆、毛、丝、草编制品等。此外,二氧化硫还可用于杀菌消毒,可以用作防腐剂。
二氧化硫对环境的污染及治理:

硫酸:
硫酸的分子式:H2SO4;结构式: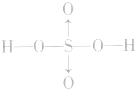 ,H2SO4中硫元素为+6价,处于最 0 高价,具有氧化性,但只有浓H2SO4表现出强氧化性,而稀硫酸、硫酸盐巾的硫元素通常不表现氧化性。
,H2SO4中硫元素为+6价,处于最 0 高价,具有氧化性,但只有浓H2SO4表现出强氧化性,而稀硫酸、硫酸盐巾的硫元素通常不表现氧化性。
硫酸的物理性质和化学性质:
1.硫酸的物理性质
纯硫酸是无色、黏稠的油状液体,密度大,沸点高,是一种难挥发的强酸,易溶于水,能以任意比与水互溶.浓硫酸溶于水时放出大量的热。常见浓硫酸的质量分数为98.3%,其密度为 1.84g·cm-3,沸点为338℃,物质的量浓度为18.4mol·L-1.H2SO4的浓度越大,密度越大,若将30%的H2SO4溶液与10%的H2SO4溶液等体积混合,所得溶液的质量分数大于20%。
2.稀硫酸的化学性质
稀硫酸具有酸的通性。
(1)与指示剂作用:能使紫色石蕊试液变红。
(2)与碱发生中和反应
(3)与碱性氧化物或碱性气体反应 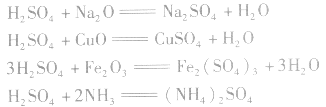
(4)与活泼金属发生置换反应 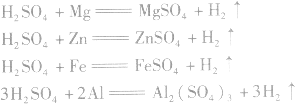
(5)与某些盐溶液反应 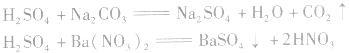
4.浓硫酸的特性
(1)吸水性将一瓶浓硫酸敞口放置在空气中,其质量将增加,密度将减小,浓度降低,体积变大。这是因为浓硫酸具有吸水性,实验室里常利用浓硫酸作干燥剂。
浓硫酸不仅可以吸收空气中的水,还可吸收混在气体中的水蒸气、混在固体中的湿存水、结晶水合物中的部分结晶水。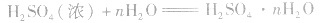 。
。
浓H2SO4中的H2SO4分子可强烈地吸收游离的水分子形成一系列的硫酸水合物: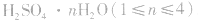 。这些水合物很稳定,所以浓H2SO4可作某些不与其反应的气体、固体的干燥剂,同时不能暴露在空气中。能够用浓H2SO4干燥的气体有
。这些水合物很稳定,所以浓H2SO4可作某些不与其反应的气体、固体的干燥剂,同时不能暴露在空气中。能够用浓H2SO4干燥的气体有 、
、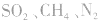 等酸性或中性气体,而具有还原性的气体
等酸性或中性气体,而具有还原性的气体 和碱性气体NH3则不能用浓H2SO4干燥。另外在酯化反应中,如
和碱性气体NH3则不能用浓H2SO4干燥。另外在酯化反应中,如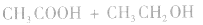
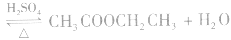 中,浓H2SO4作催化剂和吸水剂。
中,浓H2SO4作催化剂和吸水剂。
(2)脱水性指浓H2SO4将有机物里的氧、氧元素按原子个数比2:1脱去生成水的性质。浓H2SO4从有机物中脱下来的是氢、氧元素的原子,不是水,脱下来的氢、氧元素的原子按2:1的比例结合成H2O;对于分子中所含氢、氧原子个数比为2:l的有机物(如蔗糖、纤维素等),浓H2SO4可使其炭化变黑,如: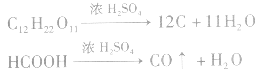
(3)强氧化性常温下,Fe、Al遇浓H2SO4会发生钝化。但热的浓 H2SO4能氧化大多数金属(除金、铂外)、某些非金属单质及一些还原性化合物。如: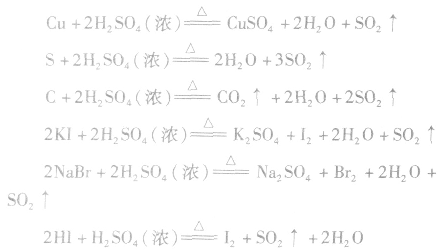
在这些氧化还原反应中,浓硫酸的还原产物一般为SO2。
浓、稀硫酸的比较与鉴别:
1.比较
稀硫酸—弱氧化性—可与活泼金属反应,生成H2—氧化性由H+体现。
浓硫酸——强氧化性——加热时可与绝大多数金属和某些非金属反应,通常生成SO2——氧化性由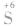 体现。
体现。
2.鉴别
从浓H2SO4和稀H2SO4性质的差异人手,可知鉴别浓H2SO4和稀H2SO4的方法有多种。
方法一:取少量蒸馏水,向其中加入少量试样硫酸,如能放出大量热则为浓H2SO4,反之则为稀H2SO4。
方法二:观察状态,浓H2SO4呈黏稠状,而稀H2SO4为黏稠度较小的溶液。
方法三:用手掂掂分量,因为浓H2SO4的密度较大 (1.84g·cm-3,相同体积的浓H2SO4和稀H2SO4,浓H2SO4的质量比稀H2SO4大很多。
方法四:取少量试样,向其中投入铁片,若产生气体,则为稀H2SO4, ;若无明显现象(钝化),则为浓H2SO4。
;若无明显现象(钝化),则为浓H2SO4。
方法五:用玻璃棒蘸取试样在纸上写字,立即变黑 (浓H2SO4的脱水性)者为浓H2SO4,另一种为稀H2SO4。
方法六:取少量试样,分别投入一小块铜片,稍加热发生反应的(有气泡产生)为浓H2SO4。(浓H2SO4的强氧化性),无现象的是稀H2SO4.
硫酸的用途及使用:
(1)用途硫酸是化学工业最黄要的产品之一,它的用途极广(如下图)。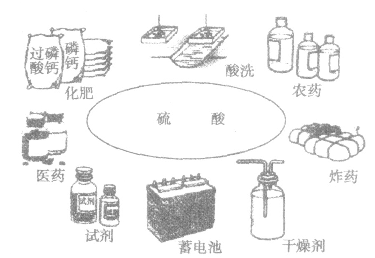
①利用其酸性可制磷肥、氮肥,可除锈,可制实用价值较高的硫酸盐等。
②利用其吸水性,在实验室浓H2SO4常用作干燥剂。
③利用其脱水性,浓H2SO4常作精炼石油的脱水剂、有机反应的脱水剂等。
④利用浓H2SO4的高沸点和难挥发性,常用于制取各种挥发性酸。
⑤浓H2SO4常作有机反应的催化剂。
(2)浓硫酸的安全使用
①浓H2SO4的稀释稀释浓硫酸时应特别注意:将浓硫酸沿器壁慢慢地注入水中,并不断搅拌,使产生的热量迅速地扩散出去。切不可把水倒人浓硫酸里。两种液体混合时,要把密度大的加到密度小的液体中,如浓H2SO4、浓HNO3-混合酸的配制方法是把浓H2SO4沿器壁慢慢地注入浓HNO3中。
②万一不小心将浓硫酸溅到皮肤上、衣服上或桌面上,应分别怎样处理?
皮肤上:用干布迅速拭去,再用大量水冲洗,最后涂上3%~5%的碳酸氢钠溶液。
衣服上:用大量水冲洗。
桌面上:大量时,用适量。NaHCO3,溶液冲洗,后用水冲洗,再用抹布擦干;少量时用抹布擦即可。
碳:
①元素符号:C
②原子结构示意图: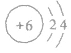
③电子式: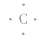
④周期表中位置:第二周期ⅣA族
⑤含量与存在:在地壳中的含量为0.087%,在自然界中既有游离态,又有化合态
⑥同素异形体:金刚石、石墨、C60、活性炭
碳(活性炭):
①金刚石:纯净的金刚石是无色透明、正八面体形状的固体,硬度大,熔点高,不导电,不溶于水
石墨:深灰色的鳞片状固体,硬度小,质软,有滑腻感,熔点高,具有导电性
活性炭:黑色粉末状或颗粒状的无定形碳,疏松多孔,有吸附性
②碳的化学性质:
a.稳定性:在常温下碳的化学性质稳定,点燃或高温的条件下能发生化学反应
b.可燃性:氧气充足的条件下:C+O2 CO2 氧气不充分的条件下:2C+O2
CO2 氧气不充分的条件下:2C+O2 2CO
2CO
c.还原性:
木炭还原氧化铜:C+2CuO 2Cu+CO2↑
2Cu+CO2↑
焦炭还原氧化铁:3C+2Fe2O3 4Fe+3CO2↑
4Fe+3CO2↑
焦炭还原四氧化三铁:2C+Fe3O4 3Fe+2CO2↑
3Fe+2CO2↑
木炭与二氧化碳的反应:C+CO2 CO
CO
二氧化碳:
①物理性质:常温下,二氧化碳是一种无色无味的气体,密度比空气大,能溶于水。固态的二氧化碳叫做干冰。
②化学性质:
a.一般情况下,二氧化碳不能燃烧,也不支持燃烧,不供给呼吸,因此当我们进入干枯的深井,深洞或久未开启的菜窖时,应先做一个灯火实验,以防止二氧化碳浓度过高而造成危险
b.二氧化碳和水反应生成碳酸,使紫色石蕊试液变红:CO2+H2O===H2CO3,碳酸不稳定,很容易分解成水和二氧化碳,所以红色石蕊试液又变回紫色:H2CO3===H2O+CO2↑
c.二氧化碳和石灰水反应:Ca(OH)2+CO2====CaCO3↓+H2O
d.二氧化碳可促进植物的光合作用:6CO2+6H2O C6H12O6+6O2
C6H12O6+6O2
③用途:
a.二氧化碳不支持燃烧,不能燃烧,比空气重,可用于灭火
b.干冰升华时吸收大量的热,可用它做制冷剂或人工降雨
c.工业制纯碱和尿素,是一种重要的化工原料 d.植物光合作用,绿色植物吸收太阳能,利用二氧化碳和水,合成有机物放出氧气。
一氧化碳:
①物理性质:通常状况下,是一种没有颜色,气味的气体,比空气略轻难溶于水。
②化学性质
a.可燃性:2CO+O2 2CO2
2CO2
b.还原性:一氧化碳还原氧化铜:CO+CuO Cu+CO2 一氧化碳还原氧化铁:3CO+Fe2O3
Cu+CO2 一氧化碳还原氧化铁:3CO+Fe2O3 2Fe+3CO2 一氧化碳还原四氧化三铁:4CO+Fe3O4
2Fe+3CO2 一氧化碳还原四氧化三铁:4CO+Fe3O4 3Fe+4CO2
3Fe+4CO2
c.毒性:一氧化碳能与人体血液中的血红蛋白结合,使血红蛋白失去运输氧气的能力,造成机体缺氧。冬天用煤火取暖,如排气不良,就会发生煤气中毒,就CO中毒。CO重要来源是汽车尾气和煤,石油等含碳燃料的不完全燃烧。
③用途:用作燃料,冶炼金属。 ④碳酸:弱酸,不稳定,易分解H2CO3==CO2↑+H2O
碳酸盐:
1.正盐与酸式盐的比较
| 正盐 | 酸式盐 | |
| 水溶性 | 除K、Na、铵的碳酸盐易溶于水外,其余都难溶于水 | 都溶于水 |
| 热稳定性 | 较稳定 ①K2CO3、Na2CO3等碱金属的正盐受热难分解 ②CaCO3、(NH4)2CO3 等受热易分解 |
受热易分解 2NaHCO3  Na2CO3+ H2O+CO2↑ Na2CO3+ H2O+CO2↑Ca(HCO3)2  CaCO3+H2O+CO2↑ CaCO3+H2O+CO2↑ |
| 与酸反应 | CO32-+2H+== CO2↑+H2O CaCO3+2H+=Ca2+ +H2O+CO2↑ |
HCO3-+H+==H2O+ CO2↑(相同条件下,NaHCO3与酸反应放出CO2的速率比Na2CO3快) |
| 与碱反应 | Na2CO3+Ca(OH)2 ==CaCO3↓+2NaOH | NaHCO3+NaOH==Na2CO3+H2O Ca(HCO3)2+Ca(OH)2==2CaCO3↓+2H2O |
| 转化关系 |  | |
(1)在水中的溶解性:一般地,相同温度下,难溶性正盐的溶解度小于其酸式盐,可(易)溶性正盐的溶解度大于其酸式盐。如CaCO3,难溶于水,Ca(HCO3)2易溶于水;Na2CO3易溶于水,NaHCO3的溶解度比 Na2CO3的小。
(2)与酸或碱反应:强酸的酸式盐只与碱反应而不与酸反应;弱酸的酸式盐与足量强碱反应生成正盐,与足量强酸反应生成弱酸。
(3)热稳定性:一般地,热稳定性的大小顺序为正盐>酸式盐(盐的阳离子相同,成盐的酸相同)。
3.碳酸钙在自然界中存在广泛,是岩石的主要成分之一。不溶于水,但溶于酸。大理石、石灰石的主要成分是CaCO3,它们既是重要的化工原料,又是重要的建筑材料。其用途图示如下:
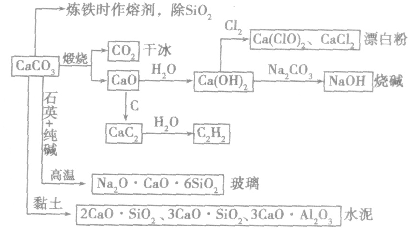
CO2气体与溶液的反应规律:
1.向某溶液中不断通入CO2气体至过量时,现象是“先产生白色沉淀,后沉淀逐渐溶解”
(1)向澄清石灰水中不断通入CO2气体的反应为:
Ca(OH)2+CO2==CaCO3↓+H2O
CaCO3+CO3+H3O==Ca(HCO3)2
(2)向氧氧化钡溶液中不断通入CO2气体的反应为:
Ba(OH)2+CO2==BaCO3↓+H2O
BaCO3+CO2+H2O==Ba(HCO3)2
(3)向漂白粉溶液中不断通入CO2气体的反应为:
Ca(ClO)2+CO2+H2O==CaCO3↓+2HClO
CaCO3+CO2+H2O==Ca(HCO3)2
2.向某溶液中不断通入CO2气体至过量时,现象为“产生白色沉淀或浑浊,沉淀或浑浊不消失”
(1)在NaAlO2溶液中不断通入CO2气体至过量时,反应为:
2AlO2-+CO2(少量)+3H2O==2Al(OH)3↓ +CO32-
2AlO2-+CO2(过量)+2H2O==Al(OH)3↓ +HCO3-
(2)向Na2SiO3溶液中不断通入CO2气体至过量时,反应为:
SiO32-+CO2+H2O==H2SiO3↓+CO32-
SiO32-+2CO2+2H2O==H2SiO3↓+2HCO3-
(3)向饱和Na2CO3溶液中不断通入CO2气体,反应为:
2Na++CO32-+CO2+H2O==2NaHCO3↓
3.CO2与NaOH溶液反应后,溶液中溶质的判断将CO2气体逐渐通入NaOH溶液中,先后发生化学反应:
①CO2+2NaOH==Na2CO3+H2O
②CO2+Na2CO3+H2O==2NaHCO3
向一定量的NaOH溶液中通入CO2气体后,溶液中溶质的成分要根据NaOH与CO2的物质的量之比进行讨论。
当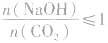 时,发生反应①和②,溶液中的溶质为NaHCO3;
时,发生反应①和②,溶液中的溶质为NaHCO3;
当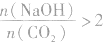 时,发生反应①,溶液中的溶质为 Na2CO3和NaOH;
时,发生反应①,溶液中的溶质为 Na2CO3和NaOH;
当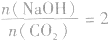 时,发生反应①,溶液中的溶质为Na2CO3;
时,发生反应①,溶液中的溶质为Na2CO3;
当 时,发生反应①和②,溶液中为Na2CO3和NaHCO3
时,发生反应①和②,溶液中为Na2CO3和NaHCO3
碳酸氢盐与碱反应的规律及CO32- HCO3-的鉴别方法:
1.酸式盐与碱反应时的产物要根据相对用量判断
如Ca(HCO3)2溶液中滴加NaOH溶液:
Ca(HCO3)2+NaOH==CaCO3↓+NaHCO3+ H2O(NaOH少量)
Ca(HCO2)2+2NaOH==CaCO3↓+Na2CO3+ 2H2O(NaOH过量)
2.CO32-和HCO3-的鉴别
(1)利用正盐和酸式盐的溶解性可区别CO32-和HCO3-,如分别和BaCl2溶液反应,生成的BaCO3不溶,生成的Ba(HCO3)2易溶;
(2)利用与H+反应产生CO2的快慢检验CO32-或HCO3-
碳族元素:
1.在元素周期表中的位置及结构碳旌死素位于第ⅣA族,包括碳(C)、硅(Si)、锗(Ge)、锡(Sn)、铅(Pb)五种元素。最外层皆有4个电子,这种结构不易得电子也不易失电子,易形成共价键,难形成离子键。
2.主要化合价碳族元素的化合价主要有+2和+4,C、Si、Ge、Sn的+4价化合物较稳定,而Pb的+2价化合物较稳定。
3.氢化物、最高价氧化物及其对应的水化物
氢化物:
最高价氧化物:RO2;
最高价氧化物对应的水化物为H2RO3、 H4RO4或R(OH)4
4.碳族元素的金属性与非金属性的递变规律由C至Pb,核电荷数逐渐增多,原子半径逐渐增大,原子核对最外层电子的吸引能力逐渐减小,失电子能力逐渐增强,得电子能力逐渐减弱,非金属性逐渐减弱,金属性逐渐增强。由碳族元素形成的单质中,碳、硅为非金属,但硅有金属光泽;锗、锡、铅为金属。
(1)基本流程:天然水+混凝剂过滤→清洁水+消毒剂→饮用水天然水中溶解的主要气体是O2、CO2、H2S。
(2)除去水中的固体杂质和悬浮物:常用混凝剂为铝盐(如硫酸铝、明矾、碱式氯化铝等)、三价铁盐等。原理为:Al3++3H2O=Al(OH)3(胶体)+3H+,Fe3++3H2O=Fe(OH)3(胶体)+3H+,生成的胶体能吸附水中的悬浮杂质而沉降,达到净水的效果。
(3)消毒:常用的消毒剂为氯气、漂白粉精、臭氧、二氧化氯等。对自来水进行暴晒是为了除去水中少量的次氯酸。水处理剂能杀菌消毒是因为它具有强氧化性。过氧化钠不能用于自来水的杀菌消毒。O3消毒的反应产物无毒无害。
(4)消除水中的异味:活性炭颗粒的比表面积大,吸附能力强,让水通过由细小的活性炭颗粒组成的滤床能够除去水中的异味。活性炭在水的净化过程中只发生物理变化。通入CO2可以除去水中的Ca离子和调节溶液的pH
污水处理:
(1)生物化学方法通常使用含有大量需氧微生物的活性污泥,在强力通入空气的条件下,微生物以水中的有机废物为养料生长繁殖,将有机物分解为二氧化碳、水等无机物,从而达到净化污水的目的。
(2)中和法酸性废水常用熟石灰中和,碱性废水常用H2SO4或CO2中和。
(3)③沉淀法 Hg2+、Pb2+、Cu2+等重金属离子可用Na2S除去,反应的离子方程式为Hg2++S2-===HgS↓,Pb2++S2-===PbS↓,Cu2++S2-===CuS↓。
注意:
①一般不采用离子交换法,因为离子交换法价格昂贵。
②过滤用到的玻璃仪器出烧杯外,还有漏斗、玻璃棒
③分离Hg是需在通风橱中进行,原因是Hg有挥发性,且有毒
④回收纯净的金属铜时应增加冷凝回流装置以防止污染。
3.水质检测的项目:BOD、有机物、N、P、重金属、pH值、悬浮物、溶解性固体、总碱度
富营养化的检测项目:水样的总铅、总铜、总铁、阴离子表面活性剂、氨氮值
与“下列推断合理的是[ ]A.明矾[KAl(SO4)2·12H2O]在水中能形成Al...”考查相似的试题有:
- 下列关于元素化合物的说法正确的是A.利用铝与氧化铁发生的铝热反应来焊接钢轨B.向某种消毒液( NaC1O)中滴加醋酸,能抑制N...
- 工业上用铝土矿(主要成分为Al2O3,含Fe2O3杂质)为原料冶炼铝的工艺流程如下:下列叙述不正确的是( )A.反应②的化学方程式...
- (2分)冶炼金属的三种常用方法是:①热分解法 ②热还原剂法 ③电解法。人类用量处在前三位的金属是铁、铝、铜。(填编号)(1)冶...
- 相同质量的铁与足量的稀H2SO4及足量的CuO制单质铜,有人设计以下两种方案:①FeH2Cu,②CuOCuSO4Cu。若实验过程中,根据一般的...
- (15分)二氧化硫是大气污染物之一,为粗略测定周围环境中二氧化硫的含量,某课外活动小组的甲、乙两位同学分别用相同实验装置...
- (10分)2.8g 铁与100 mL稀硫酸恰好完全反应,反应前后溶液体积的变化忽略不计。 求: (1)产生的气体在标准状况下的体积。 ...
- I:某兴趣小组欲在绿色环保的条件下探究大气污染物SO2的性质,设计如下图实验装置。请回答:(1)B、C、D分别用于检验SO2的漂...
- 两份不同浓度的NaOH溶液各500mL,分别吸收1120mL(标准状况下体积)SO2气体,反应后溶液中分别有5.75g和7.10g溶质。求两份NaOH...
- 如右图所示,小试管内盛有约3 mL饱和硫酸铜溶液,与锥形瓶连通的U形管内盛有少量水(为便于观察,预先染成红色),沿小试管的...
- 氮化硅是新型无机非金属材料,其中Si与N原子最外层均达到8电子结构。下列关于它的说法不正确的是A.硅与氮的原子数之比为4:3B...