本试题 “对硝基甲苯是医药、染料等工业的一种重要有机中间体,它常以浓硝酸为硝化剂,浓硫酸为催化剂,通过甲苯的硝化反应制备.一种新的制备对硝基甲苯的实验方法是...” 主要考查您对影响化学反应速率的因素
过滤
萃取
分液
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 影响化学反应速率的因素
- 过滤
- 萃取
- 分液
影响化学反应速率的因素:
1.内因:参加反应的物质的结构及性质。
2.外因:主要是指浓度、温度、压强和催化剂,另外还有光、超声波、激光、搅拌、固体表面积、形成原电池等。
(1)浓度:其他条件相同时,增大反应物浓度,化学反应速率增大;减小反应物浓度,化学反应速率减小。在一定温度下,同体、纯液体的浓度视为定值,如C与CO2的反应、Na与H2O的反应中,C的量和Na、H2O 的量减少并不意味着其“浓度”减小,即不冈其量的增减而影响反应速率,但会因固体表面积的变化而改变反应速率。
(2)温度:其他条件相同时,升高温度,可以加快反应速率,实验测得,温度每升高10℃,化学反应速率通常增大到原来的2~4倍。
经验公式为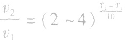
(3)压强:对于气体反应,当温度不变时,增大压强可以加快反应速率。对于气体反应体系,压强改变时有以下几种情况:

(4)催化剂:催化剂是能改变化学反应速率但在反应前后本身的质量和化学性质都不变的物质。对于某些化学反应,使用正催化剂能显著加快化学反应速率。
(5)其他因素:增大同体的表面积(如将块状改为粉末状),可增大反应速率;光照一般也可增大某些反应的速率;形成原电池可以加快反应速率;此外,超声波、放射线、电磁波等因素也能影响反应速率。
3.外因对化学反应速率影响的微观解释
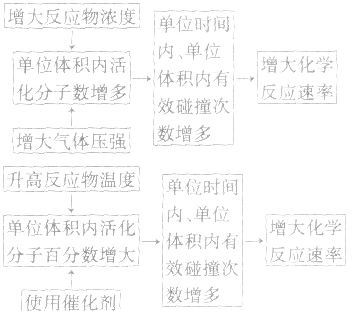
1.内因:参加反应的物质的结构及性质。
2.外因:主要是指浓度、温度、压强和催化剂,另外还有光、超声波、激光、搅拌、固体表面积、形成原电池等。
(1)浓度:其他条件相同时,增大反应物浓度,化学反应速率增大;减小反应物浓度,化学反应速率减小。在一定温度下,同体、纯液体的浓度视为定值,如C与CO2的反应、Na与H2O的反应中,C的量和Na、H2O 的量减少并不意味着其“浓度”减小,即不冈其量的增减而影响反应速率,但会因固体表面积的变化而改变反应速率。
(2)温度:其他条件相同时,升高温度,可以加快反应速率,实验测得,温度每升高10℃,化学反应速率通常增大到原来的2~4倍。
经验公式为
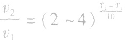
(3)压强:对于气体反应,当温度不变时,增大压强可以加快反应速率。对于气体反应体系,压强改变时有以下几种情况:

(4)催化剂:催化剂是能改变化学反应速率但在反应前后本身的质量和化学性质都不变的物质。对于某些化学反应,使用正催化剂能显著加快化学反应速率。
(5)其他因素:增大同体的表面积(如将块状改为粉末状),可增大反应速率;光照一般也可增大某些反应的速率;形成原电池可以加快反应速率;此外,超声波、放射线、电磁波等因素也能影响反应速率。
3.外因对化学反应速率影响的微观解释

过滤:
| 名称 | 用途 | 装置 | 举例 | 注意事项 |
| 过滤 | 分离固体和液体混合物 | 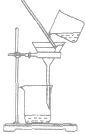 |
粗盐提纯时把粗盐溶于水,经过滤把不溶于水的杂质除去 | ①要“一贴二低三靠” 滤纸紧贴漏斗内壁;滤纸边缘低于漏斗口,漏斗里液面低于滤纸边缘;烧杯口紧靠玻璃棒,玻璃捧下端紧靠三层滤纸.漏斗下端紧靠烧杯内壁。 ②必要时洗涤沉淀物(在过滤器中加少量水),不可搅拌 |
萃取:
| 名称 | 用途 | 装置 | 举例 | 注意事项 |
| 萃取 | 分离两种互溶的液体 |  |
CCl4把溴水中的Br2萃取出来 |
①萃取后再进行分液操作 ②对萃取剂的要求:与原溶剂互不混溶,不反应;溶质在其中的溶解度比在原溶剂中大;溶质不与萃取剂反应 ③萃取后得到的仍是溶液,一般要通过分馏等方法进一步分离 |
分液:
| 名称 | 用途 | 装置 | 举例 | 注意事项 |
| 分液 | 分离两种不相混溶的液体(密度不同) | 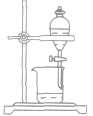 |
水、苯的分离 | 下层液体从下口放出,上层液体从上口倒出 |
发现相似题
与“对硝基甲苯是医药、染料等工业的一种重要有机中间体,它常以...”考查相似的试题有:
- 25℃时,在体积为2L的密闭容器中,气态物质A、B、C的物质的量n(mol)随时间t的变化如图1所示.已知达平衡后,降低温度,A的转...
- 设C(g)+CO2(g)2CO(g) △H>0 ,反应速率为u1,N2+3H22NH3△H<0反应速率为u2,对于上述反应,当温度升高时,u1和u2的变化情况...
- 下列措施一定能使化学反应速率加快的是( )A.增大反应物的量B.增大压强C.升高温度D.使用催化剂
- 已知分解1 mol H2O2放出热量98KJ,在含少量I-的溶液中,H2O2的分解机理为:H2O2+ I-→H2O +IO- 慢 H2O2+ IO-→H2O +O2...
- 密闭容器中发生下列反应:N2+3H22NH3△H”“
- 下列对实验现象的描述中错误的是A.向FeCl3和KSCN混合溶液中加入少量KCl固体,溶液血红色变浅B.向5mL 0.1mol/L K2Cr2O7溶液...
- 下列图象表达正确的是( )A.图①表示25℃时,用0.1mol•L-1盐酸滴定20mL0.1mol•L-1NaOH溶液B.图②表示常温下,两份足量、等浓...
- 下列实验操作中,不正确的是( )A.实验时,将水倒入浓硫酸配制稀硫酸B.焰色反应实验前,铂丝应先用盐酸洗净,在酒精灯外焰...
- 对实验Ⅰ~Ⅳ的实验现象预测正确的是( ) A.实验1:液体分层,下层呈无色 B.实验2:烧杯中先出现白色沉淀,后溶解 C.实验3...
- 下列实验装置(固定装置略去)和操作正确的是( )A. 分离CCl4和水B. 酸碱中和滴定C. 吸收HCl尾气D. 中和热的测定