本试题 “盖斯定律认为能量总是守恒的:化学反应过程一步完成或分步完成,整个过程的热效应是相同的。已知:①H2O(g)===H2O(l); ΔH=-Q1kJ/mol②C2H5OH(g)===C2H5OH(l...” 主要考查您对燃烧热
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 燃烧热
燃烧热:
在101kPa时,1mol纯物质完全燃烧生成稳定的氧化物时所放出的热量,叫做该物质的燃烧热。单位为kJ/mol
注意事项:
(1)规定是在101kPa 下测出的热量。书中提供的燃烧热数据都是在25℃、101kPa下测定出来的
(2)规定可燃物的物质的量为1mol(这样才有可比性)。因此,表示可燃物的燃烧热的热化学方程式中,可燃物的化学计量数为1,其他物质的化学计量数常出现分数
(3)规定生成稳定的氧化物,例如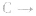
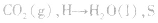
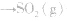 等
等
(4)叙述燃烧热时、不用“+”“-”,在热化学方程式中用△H表示时取“-”
在101kPa时,1mol纯物质完全燃烧生成稳定的氧化物时所放出的热量,叫做该物质的燃烧热。单位为kJ/mol
燃烧热和中和热的异同:
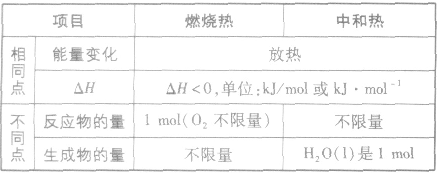
注意事项:
(1)规定是在101kPa 下测出的热量。书中提供的燃烧热数据都是在25℃、101kPa下测定出来的
(2)规定可燃物的物质的量为1mol(这样才有可比性)。因此,表示可燃物的燃烧热的热化学方程式中,可燃物的化学计量数为1,其他物质的化学计量数常出现分数
(3)规定生成稳定的氧化物,例如
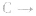
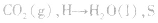
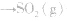 等
等 (4)叙述燃烧热时、不用“+”“-”,在热化学方程式中用△H表示时取“-”
发现相似题
与“盖斯定律认为能量总是守恒的:化学反应过程一步完成或分步完...”考查相似的试题有:
- (6分)实验室用50 mL 0.50 mol·L-1盐酸、50 mL 0.55 mol·L-1NaOH,利用如图装置进行中和热的测定,请回答下列问题:(1) 不...
- 以NA代表阿伏加德罗常数,则对下列热化学方程式C2H2(g)+5/2O2(g)=2CO2(g)+H2O(1) △H=-1300 kJ/mol的说法正确的是( )A...
- (6分,每空2分)在火箭推进器中装有还原剂肼(N2H4)和强氧化剂H2O2,当它们混合时,即产生大量的氮气和水蒸气,并放出大量...
- 盖斯定律认为能量总是守恒的,不管化学反应过程是一步完成或分几步完成,整个过程的热效应是相同的。已知:①H2O(g)=H2O(l) ΔH1=-...
- 某些化学键键能数据如下:化学键H—HCl—ClH—Cl键能/ kJ·mol-1436243431 则下列热化学方程式不正确的是 ( )A.H2(g)+Cl2(g)=HC...
- 已知:Fe2O3(s)+C(s)= CO2(g)+2Fe(s) △H=234.1kJ·mol-1C(s)+O2(g)=CO2(g) △H=-393.5kJ·mol-1, 则 2Fe(s)+O2(g)=Fe2O3(...
- 已知N≡N键的键能是945kJ﹒mol-1,N—N键的键能是159kJ﹒mol-1,H-H键的键能是436kJ﹒mol-1,N-H键的键能是391kJ﹒mol-1,则N2(...
- 氨的合成是最重要的化工生产之一。I.工业上合成氨用的H2有多种制取的方法:① 用焦炭跟水反应: C(s)+ H2O(g)CO(g)+ H2(g)...
- 根据键能数据估算CH4(g)+4F2(g)=CF4(g)+4HF(g)的反应热ΔH为A.–1940 kJ · mol-1B.1940 kJ · mol-1C.–485 kJ · mol-1D....
- 已知下列热化学方程式:Zn(s)+1/2O2(g)=ZnO(s);△H=-351.1kJ·mol-1Hg(l)+1/2O2(g)=HgO(s);△H=-90.7 kJ·m...