本试题 “对下列实验指定容器中的水,其解释没有体现水的主要作用的是[ ]A.---集气瓶中的水:吸收放出的热量B.---量筒中的水:通过水体积的变化得出O2体积C.---集气...” 主要考查您对氢气的制取和收集
空气中氧气含量的测定
S,Fe,C,P等物质在氧气中的燃烧
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 氢气的制取和收集
- 空气中氧气含量的测定
- S,Fe,C,P等物质在氧气中的燃烧
实验室里通常用稀硫酸跟金属锌起反应来制取氢气,也可以用盐酸代替硫酸,用镁或铁代替锌来制取氢气。
氢气的实验室制法:
| 化学药品 | 锌粒和稀硫酸 |
| 反应原理 | Zn + H2SO4== ZnSO4+ H2↑ |
| 发生装置 | 反应物状态为固态和液态,反应条件为室温,可选择实验室制CO2的反应装置(或用过氧化氢溶液制氧气的反应装置)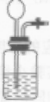 |
| 收集装置 | 向下排空气法或排水法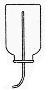  |
| 实验步骤 | ①检验装置的气密性 ②装锌粒(注意将试管横放,把锌粒放入试管口,再慢慢竖起) ③把试管固定在铁架台上 ④加入稀硫酸 ⑤收集气体 |
| 注意事项 | ①不能用浓H2SO4代替稀H2SO4,浓H2SO4具有强氧化性 ②不能用金属活动性顺序表中排在氢后面的金属,如铜,也不能用排在氢前的金属,如钠,一般常用Zn、Al、Fe、Mg等。 ③长颈漏斗末端应在液而以下,防止氢气从长颈漏斗逸出 |
氢气的工业制法:
| 制取方法 | 原理 | 优缺点 |
| 电解水 | 2H2O 2H2↑+O2 2H2↑+O2 |
优点:得到氢气纯度高 缺点:耗能高 |
| 水煤气 | C+H2O(g) CO+H2 CO+H2 |
优点:成本低 缺点:需要设备多(需要除去CO中的杂质) |
| 天然气 | CH4 C+2H2 C+2H2 |
优点:原料丰富 缺点:氢气纯度低 |
| 电解饱和食盐水 | 2NaCl+2H2O 2NaOH+H2↑+Cl2↑ 2NaOH+H2↑+Cl2↑ |
优点:是氯碱化工的副产品 缺点:纯度低 |
| 理想模式:利用太阳能、高效催化剂分解水 | 2H2O 2H2↑+O2↑ 2H2↑+O2↑ |
优点:不耗费电能、热能,环保 缺点:人类未能寻找到高效催化剂,还未能实际应用 |
空气中氧气含量的测定实验是初中化学的一个重要实验,同时也是历年各地中考命题的热点。近年来在课本实验的基础上进行拓展、创新,旨在考查同学们的实验探究能力及创新思维能力已成为中考命题的趋势。
空气中氧气含量的测定实验:
| 原理 | 利用红磷在空气中燃烧,将瓶内氧气消耗掉,生成五氧化二磷固体,使空气内压强减少,在大气压作用下,进入容器内水的体积即为减少的氧气的体积。4P + 5O2 2P2O5 2P2O5 |
| 装置 | 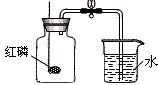 |
| 步骤 | ①连接装置,检查装置气密性 ②把集气瓶的容积分成5等份,做好记号。 ③用止水夹夹紧胶管。 ④在燃烧匙内放入过量的红磷。 ⑤点燃燃烧匙中的红磷,立即伸入集气瓶中,把塞子塞紧 ⑥待红磷熄灭并冷却后,打开止水阀 |
| 现象 | ①集气瓶中有大量的白烟生成,并放出热量 ②打开止水夹,烧杯中的水倒流到集气瓶中,并上升到约1/5处 |
| 结论 | 空气中氧气的体积分数约为1/5。 |
实验中的注意事项:
1.测定空气中氧气的体积分数时,所用物质应满足的条件:
①此物质能够在空气中中燃烧,不能用铁丝代替,铁丝在空气中不能燃烧
②此物质在空气中燃烧的时只能消耗氧气,不能消耗其他气体。不能选用镁代替红磷,因为镁不仅与空气中的氧气反应,还和二氧化碳反应。
③此物质在空气中燃烧时只能生成固体,而不能生成气体,一般不用木炭,硫代替红磷。
2.实验失败与成功的原因:
①装置不漏气是本实验成功的关键,所以实验前应检查装置的气密性。如果气密性不好,外界空气会进入容器,使测定结果低于1/5。
②实验中红磷要过量,以消耗容器内全部氧气,否则会使测定结果低于1/5.
③实验完毕,待容器冷却至室温后,再打开止水夹,观察进水的体积,避免因温度高,气体膨胀,使测定结果低于1/5.
空气中氧气含量测定实验的改进:
1.测定原理:
(1)红磷(白磷)在密闭的容器中燃烧,消耗氧气,生成白色固体五氧化二磷。密闭容器内压强减小,大气压将水压入容器,通过测定容器中的水的量测定氧气在空气中的含量。
(2)利用金属与氧气反应,消耗密闭容器中的氧气使密闭容器内压强减小,在大气压的作用下,推动刻度器上的活塞移动,测出氧气体积。
2.装置
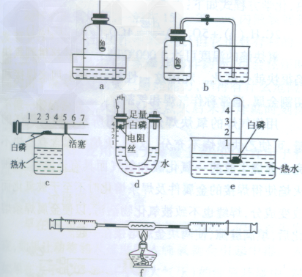
3.实验现象
(1)红磷(白磷)燃烧,产生大量白烟
(2)a中睡眠上升约占钟罩内空气体积的1/5
b中进入集气瓶中水的体积约占集气瓶液面以上容积的1/5
c中活塞移动到4处
d中U形管左侧液面上升至刻度1处
e中试管中液面上升至刻度1处
f中右侧的活塞会左移
4.结论
空气中氧气体积约占空气总体积的1/5
5.注意事项
(1)实验中红磷要过量,以消耗容器内全部氧气,否则会使测定结果低于1/5.
(2)装置不漏气是本实验成功的关键,所以实验前应检查装置的气密性。如果气密性不好,外界空气会进入容器,使测定结果低于1/5。
(3)不能用硫、木炭、铁丝等代替红磷(白磷)。因为硫或木炭燃烧后产生的气体会弥补反应所消耗的氧气,导致测得的体积不准确,而细铁丝在空气中难以燃烧,氧气体积几乎不变,因此密闭空气内水面不上升。
(4)导气管要夹紧,燃烧匙放入集气瓶时要迅速,防止空气受热膨胀,从导气管或集气瓶逸出,导致进入水的体积增多,使实验结果偏高。
氧化的化学性质很活泼,很多物质都能与氧气发生化学反应。
部分物质在空气中和氧气中反应的对比:
a)碳和氧气反应
方程式:C + O2 CO2
CO2
现象:剧烈燃烧,发白光,放热,生成使澄清石灰水变浑浊的气体
b)硫和氧气反应
方程式:S + O2 SO2
SO2
现象:发出明亮的蓝紫色火焰,放热,生成有刺激性气味的气体
注意:实验前应在瓶底放少量水,用来吸收生成的有毒气体。
c)红磷和氧气反应:
方程式:4P + 5O2 2P2O5
2P2O5
现象:发出耀眼的白光,放热,生成大量白烟
生成的P2O5是固体小颗粒,现象为白烟,不是白雾。
d)铁和氧气的反应:
方程式:3Fe + 2O2 Fe3O4
Fe3O4
现象:剧烈燃烧,火星四射,放出热量,生成黑色物质
注意:集气瓶底放一层细沙或少量水。
e)镁和氧气反应:
方程式:2Mg + O2 2MgO
2MgO
现象:剧烈燃烧,发出耀眼的白光,放出热量,生成白色粉末状固体,有白烟。
注意:不能手持镁条,应用坩埚钳夹持。
f)石蜡和氧气反应
文字表达式:石蜡+氧气 水+二氧化碳
水+二氧化碳
现象:剧烈燃烧,放出热量,发出白光,如果在火焰上方罩一个干冷烧杯,
烧杯内壁有水珠,生成使澄清石灰水变浑浊的气体。
烟和雾的区别:
a)烟:大量固体小颗粒分散在空气长产生烟。红磷燃烧产生大量白烟,是燃烧生成的固体P2O5分散在空气中形成的
b)雾:大量小液滴分散在气体中产生雾。打开盛浓盐酸的瓶塞,瓶口有白雾,是挥发的HCl气体遇到空气中的水蒸气形成了盐酸小液滴。
a)光:固体物质燃烧使发光。镁条燃烧发出耀眼的强光,木炭在氧气中燃烧产生白光
b)气体物质和容易气化的物质燃烧时产生火焰。蜡烛在氧气中燃烧产生白色的火焰,是石蜡熔化后生成的气体燃烧而产生的。
描述物质在氧气中燃烧的现象的技巧:
可按三个顺序从三个方面进行:
(1)剧烈燃烧,有什么颜色的光,火焰;
(2)放热;
(3)生成物的特性
与“对下列实验指定容器中的水,其解释没有体现水的主要作用的是[...”考查相似的试题有:
- 请按要求回答下列有关问题.(1)选择实验室制取和收集氧气、氢气和二氧化碳气体的仪器装置图.(填“√”)序号ABCD仪器装置图...
- (2011年四川广安,8题)实验室利用下列装置可以制取某些气体,请据图回答问题:(1)这五个装置示意图中,有一个装置是错误...
- 某研究性学习小组设计了如图所示的定量装置,其中B是底面积为100cm、高为20cm的圆筒状玻璃容器(带密封盖),上面标有以厘米...
- 右图是测定空气里氧气含量的实验装置图.实验时先在集气瓶中加入少量水,做上记号A.用弹簧夹夹紧乳胶管.点燃燃烧匙内的红磷...
- 常见实验操作或现象描述正确的是( )A.铁丝在空气中燃烧,火星四射B.电解水实验中,正极与负极产生的气体体积比为l:2C....
- 某化学兴趣小组为测定Fe、Cu、Ag三种金属的活动性顺序设计了四种方案,每没种方案所用试剂如下,其中你认为不可行的是A.Cu、...
- 某同学利用以下药品:长、宽和厚度均相同的锌片、铁片和铜片,稀硫酸、硫酸亚铁溶液、硫酸铜溶液、硫酸锌溶液、锌粉,验证锌...
- 下列物质在氧气中燃烧,实验现象和反应类型正确的是( )A.硫--淡蓝色火焰--化合反应B.红磷--大量白雾--氧化反应C.蜡烛--...
- 在“氧气的制取和性质”课后,某同学取一段纱窗网上的细铁丝,在自己收集到的氧气中做“细铁丝在氧气中的燃烧”实验。结果没有观...
- 碳的世界很丰富,它在生产生活中有着广泛应用。(1)如图为元素周期表中有关碳元素的信息,碳元素原子核内的质子数 ;(2)关...