本试题 “化学与人类生活的关系越来越密切.(1)我们穿的衣服通常是由纤维织成的,常见的纤维有棉花、羊毛、涤纶等,用灼烧法可初步鉴定这三种纤维,其中灼烧后产生烧...” 主要考查您对化学元素和人体健康
天然有机高分子材料
乳化和乳化作用
化学式的写法和意义
物质组成元素的质量分数
合金
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 化学元素和人体健康
- 天然有机高分子材料
- 乳化和乳化作用
- 化学式的写法和意义
- 物质组成元素的质量分数
- 合金
在人体中元素的存在形式:
①碳、氢、氧、氮主要以水、糖类、蛋白质、维生素和脂肪的形式存在。
②其他的元素主要以无机盐的形式存在于水溶液中。
③钙元素主要以羟基磷酸钙[Ca10(PO4)6(OH)2] 晶体的形式存在。
常量元素:
常量元素人体中含量较多的元素有11种,它们约占人体质量的99.95%。在人体中含量超过0.01%的元素,称为常量元素。
①人体中的常量元素
| 元素名称 | 元素符号 | 质量分数% |
| 氧 | O | 65.0 |
| 碳 | C | 18.0 |
| 氢 | H | 10.0 |
| 氮 | N | 3.0 |
| 钙 | Ca | 2.0 |
| 磷 | P | 1.0 |
| 钾 | K | 0.35 |
| 硫 | S | 0.25 |
| 钠 | Na | 0.15 |
| 氯 | Cl | 0.15 |
| 镁 | Mg | 0.05 |
②一些常量元素在人体中的作用及每天适宜摄入量
| 钙 | 使骨骼和牙街具有坚硬的结构支架 | 800—1200mg | 缺钙主要影响骨骼的发育和结构,临床症状表现为青少年的佝偻病和成年人的骨质软化症及老年人的骨质疏松症。钙是无毒的元素,但摄入过量会导致高血钙,从而引起消化系统、泌尿系统等的疾病 | 海产品、豆类、奶类、各种绿叶蔬菜等 | 其中99%存在于骨骼和牙齿中,主要以羟基磷酸钙 [Ca10(PO4)6(OH)2晶体的形式存在 |
| 钠 | 细胞外液和细胞内液中的Na+和K+各自保持一定的浓度,维持人体内的水分和体液恒定的pH | 2000—2500mg | 缺钠会引起肌肉痉挛、头痛等;过量会引起水肿、高血压、贫血等 | 食盐 | 其中一半以Na+的形式存在于细胞外液中 |
| 钾 | 1850—5600mg | 缺钾会引起肌肉不发达、心律小齐等;过量会导致恶心、腹泻等 | 香蕉、柑橘、橙子、山楂、蘑菇、豆炎及其制品等 | 主要以K+的形式萍在干细胞内液中 | |
| 镁 | 促进骨骼发育、细胞遗传物质合成等 | 300—400mg | 缺镁会引起肌肉不发达、抽搐、痉挛、心律不齐等;过量会引起神经系统紊乱、肾病等 | 坚果、大豆、牛奶等 | 70%的镁以磷酸盐和碳酸盐形式参与骨骼和牙齿的组成,25%的镁存在于软组织中 |
微量元素:
在人体中含量在0.01%以下的元素。
①一些人体必需的微量元素
| 元素名称 | 元素符号 |
| 铁 | Fe |
| 钴 | Co |
| 铜 | Cu |
| 锌 | Zn |
| 铬 | Cr |
| 锰 | Mn |
| 钼 | Mo |
| 氟 | F |
| 碘 | I |
| 硒 | Se |
②一些必需微量元素对人体的作用及14—18岁人群每天的适宜摄入量
| 元素 | 人体内的含量 | 对人体的作用 | 适宜摄入量(每天) | 摄入量过高,过低对人体健康的影响 |
| 铁 | 4—5g | 是血红蛋白的成分,能帮助氧气的运输 | 20—50mg | 缺铁会引起贫血 |
| 锌 | 2.5g | 影响人体发育 | 15.5—19mg | 缺锌会引起食欲不振,生长迟缓,发育不良 |
| 硒 | 14—21mg | 有防癌、抗癌作用 | 50μg | 缺硒可能引起表皮角质化和癌症。如摄入量过高,会使人中毒 |
| 碘 | 25—50mg | 是甲状腺激素的重要成分 | 150μg | 缺碘会引起甲状腺肿大,幼儿缺碘会影响生长发育,造成思维迟钝。过量也会引起甲状腺肿大 |
| 氟 | 2.6g | 能防治龋齿 | 1.5mg | 缺氟易产生龋齿,过量会引起氟斑牙和氟骨病 |
知识拓展:
如果人体所需的元素仅从食物中摄取还不足时,可通过食品添加剂和保健药剂来予以补充。
如在食品巾添加含钙、锌、硒、锗的化合物,或制成补钙、补锌等的保健药剂或制成加碘食盐,来增加对这些元素的摄人量。但要注意即使是人体必需的元素,也要注意适宜的摄入量,摄人量过高和过低对人体健康都有不良的影响。
含有碳元素的化合物称为有机化合物(一氧化碳、二氧化碳、碳酸钙等除外),简称有机物。
有机高分子:
有些有机物的相对分子质量比较大,通常称它们为有机高分子化合物,简称有机高分子。如淀粉、蛋白质、纤维素、塑料、橡胶等。
【有机高分子模型】
有机高分子材料:
用有机高分子化合物制成的材料就是有机高分子材料。
有机高分子材料分为:
(1)天然有机高分子材料:例如:棉花、羊毛、天然橡胶等。
(2)合成有机高分子材料:例如:塑料、合成橡胶、合成纤维等,简称合成材料。
常见的天然有机高分子材料及其特点:
1、棉花:棉花的主要成分是纤维素,纤维素含量高达90%以上。棉纤维能制成多种规格的织物,用它制成的衣服具有耐磨并能在高温下熨烫,良好的吸湿性、透气性和穿着舒适的优点。
2、羊毛:羊毛主要南蛋白质构成,是纺织工业的重要原料,织物具有弹性好、吸湿性强、保暖性好等优点。
3、蚕丝:蚕丝是蚕结茧时形成的长纤维,也是一种天然纤维,其主要成分是蛋白质。蚕丝质轻而细长,织物光泽好、穿着舒适、手感滑顺、导热性差、吸湿透气性好。中国是世界上最早使用丝织物的国家。
4、天然橡胶:天然橡胶是指从橡胶树上采集的天然胶乳,经过凝同、干燥等加工工序制成的弹性固状物。天然橡胶是一种以聚异戊二烯为主要成分的天然高分子化合物。分子式是(C5H8)n,其成分中91%~ 94%是橡胶烃(聚异戊二烯),其余为蛋白质、脂肪酸、糖类等非橡胶物质,是应用最广的通用橡胶。
1. 乳化现象:
乳浊液不稳定,静置分层,在乳浊液中加人洗涤剂以后,油虽然并没有溶解在水中,但这时形成的乳浊液却能均匀、稳定地存在而不分层,这种现象叫乳化现象。
“乳化”形成的并不是溶液,例如植物油中加入水,加入乳化剂并不是水溶解了油,只是使植物油分散成无数细小的液滴存在于水中而不聚集。
2. 乳浊液:小液滴分散到液体里形成的混合物。
3. 乳化作用:
乳蚀液的稳定剂是一类表面活性剂,阻止小液滴相互凝结。洗涤剂能把植物油分散成无数细小的液滴而不聚集成大的油珠,洗涤剂所起的作用就是乳化作用,使植物油分散成无数细小的液滴存在于水中而不聚集。
用汽油去油污与用洗涤剂洗去油污的不同:
利用汽油和洗涤剂均能除一去油污,但二者除去油污的原理不同。汽油溶解油污时形成溶液,但加了洗涤剂的水清洗油污是把油污分散成细小的液滴,使其形成乳浊液,再随着水漂走。
除去织物上污渍的方法:
| 污渍 | 清洗方法 |
| 蓝墨水 | 白色织物上,可用草酸低稀溶液和漂白剂溶液轮流擦拭,再用洗涤剂和水洗;有色织物上,小心用高锰酸钾溶液擦拭,污渍去掉后,迅速用过氧化氢稀溶液擦拭污渍处,并立即用水漂洗 |
| 圆珠笔油 | 用酒精擦拭,再用洗涤剂洗,最后用水洗 |
| 菜汤,乳汁 | 用酒精擦拭,然后用稀氨水揉搓,再用水洗 |
| 水果渍 | 用氯化钠溶液洗,或用草酸稀溶液沾湿,再用水洗;如果是白色织物,可用过氧化氢稀溶液沾湿,再用水洗 |
| 血渍 | 刚沾上时,立即用冷水洗,再用洗涤剂洗,最后用水洗;沾污时间较长的,可用氨水擦拭,片刻后用冷水洗,如不能除净,用草酸稀溶液洗涤,然后用水洗 |
| 铁锈 | 草酸稀溶液清洗,然后用水洗 |
| 沥青 | 用酒精或汽油擦拭多次,然后用水洗 |
乳化作用在生活中的应用:
①洗涤:用乳化剂(洗涤剂)可以将衣服上、餐具上的油污洗掉,如肥皂、洗洁精等。
②农药的使用:在农药中加入一定量的乳化剂后. 再溶解在有机溶剂里,混合均匀制成的透明液体叫乳油。
用元素符号和数字的组合表示物质组成的式子,叫做化学式。如可用O2,H2O,MgO分别表示氧气、水、氧化镁的化学式。
对概念的理解:
(1)混合物不能用化学式表示,只有纯净物才能用化学式表示。
(2)每一种纯净物只有一个化学式,但一个化学式有可能用来表示不同的物质。如氧气的化学式是O2,没有别的式子再能表示氧气;P既是红磷的化学式,也是白磷的化学式。
(3)纯净物的化学式不能臆造,化学式可通过以下途径确定:
①科学家通过进行精确的定量实验,测定纯净物中各元素的质量比,再经计算得出。
②已经确定存在的物质可根据化合价写出。
书写规则:
1.单质化学式的写法:
首先写出组成单质的元素符号,再在元素符号右下角用数字写出构成一个单质分子的原子个数。稀有气体是由原子直接构成的,通常就用元素符号来表示它们的化学式。金属单质和固态非金属单质的结构比较复杂,习惯上也用元素符号来表示它们的化学式。
2.化合物化学式的写法:
首先按正前负后的顺序写出组成化合物的所有元素符号,然后在每种元素符号的右下角用数字写出每个化合物分子中该元素的原子个数。一定顺序通常是指:氧元素与另一元素组成的化合物,一般要把氧元素符号写在右边;氢元素与另一元素组成的化合物,一般要把氢元素符号写在左边;金属元素、氢元素与非金属元素组成的化合物,一般要把非金属元素符号写在右边。直接由离子构成的化合物,其化学式常用其离子最简单整数比表示。
化学式的读法:
一般是从右向左叫做“某化某”,如“CuO”叫氧化铜。当一个分子中原子个数不止一个时,还要指出一个分子里元素的原子个数,如“P2O5”叫五氧化二磷。有带酸的原子团要读成“某酸某”如“CuSO4”叫硫酸铜,还有的要读“氢氧化某”,如“NaOH”叫氢氧化钠。“氢氧化某”是碱类物质,电离出来的负电荷只有氢氧根离子。
化学式的意义:
(1)由分子构成的物质
| 化学式的含义 | 以H2O为例 | ||
| 质的含义 | 宏观 | ①表示一种物质 ②表示物质的元素组成 |
①表示水 ②表示水是由氢、氧两种元素组成的 |
| 微观 | ①表示物质的一个分子 ②表示组成物质每个分子的原子种类和数目 ③表示物质的一个分子中的原子总数 |
①表示一个水分子 ②表示一个水分子是由两个氧原子和一个氧原子构成的 ③表示一个水分子中含有三个原子 | |
| 量的含义 | ①表示物质的相对分子质量 ②表示组成物质的各元素的质量比 ③表示物质中各元素的质量分数 |
①H2O的相对分子质R =18 ②H2O中氢元素和氧元素质量比为1:8 ③H2O中氢元素的质量分数= 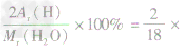 100%=11.1% 100%=11.1% | |
(2)由原子构成的物质(以Cu为例)
宏观:
表示该物质:铜
表示该物质由什么元素组成:铜由铜元素组成
微观:表示该物质的一个原子—一个铜原子。
化学式和化合价的关系:
(1)根据化学式求化合价
①已知物质的化学式,根据化合价中各元素的正负化合价代数和为0的原则确定元素的化合价。
标出已知、未知化合价: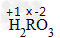
列出式子求解:(+1)×2+x×1+(-2)×3=0 x=+4
②根据化合价原则,判断化学式的正误,如判断化学式KCO3是否正确
标出元素或原子团的化合价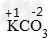
计算正负化合价代数和是否为0:(+1)×1+(-2)×1=-1≠0,所以给出的化学式是错误的,正确的为K2CO3。
③根据化合价原则,计算原子团中某元素的化合价,如计算NH4+中氮元素的化合价和H2PO4-(磷酸二氢根)中磷元素的化合价。
由于NH4+带一个单位的正电荷,不是电中性的,因此各元素的化合价代数和不为多,而是等于+1. 设氮元素的化合价为x
x+(+1)×4=+1 x=-3
所以在NH4+中,氮元素的化合价为-3. 同理H2PO4-带一个单位的负电荷、不是电中性的、因此各元素的化合价代数和不为零,而是-1.
设磷元素的化合价为y
(+1)×2+y+(-2)×4=-1 y=+5 所以在H2PO4-中磷元素的化合价为+5.
④根据化合价原则,确定物质按化合价的排序。如H2S,S,SO2,H2SO4四种物质中均含有硫元素,并且硫元素的化合价在四种物质中分别为:-2,0, +4,+6,故这四种物质是按硫元素的化合价由低到高的顺序排列的。
(2)根据化合价写化学式
根据化合物中化合价的代数和等于0的原则,已知元素的化合价可以推求实际存在物质的化学式,主要方法有两种:
①最小公倍数法
| 步骤 | 举例 | |
| 写 | 一般把正价元素的符号(或原子团)写在左边,负价元素的符号(或原子团)写在右边,并把化合价写在元素符号(或原子团)的正上方 | 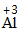 、 、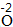 |
| 求 | 求出两种元素化合价绝对位的最小公倍数,然后求出每种元素的原子个数= |
因为|-2|×|+3|=6,所以Al原子个数为6/3=2,O原子个数=6/2=3 |
| 标 | 将原子个数写在相应元素符号的正下角 | Al2O3 |
| 验 | 检验各种元素正负化合价的代数和是否为0,确定化学式的正确性 | (+3)×2+(-2)×3=0,所以该化学式正确。 |
| 步骤 | 例1 硫酸铜 | 例2 氧化钙 | |
| 排列 | 分析名称,确定元素符号(或原子团)的顺序 | 铝 硫酸根 Al SO4 |
钙 氧 Ca O |
| 标价 | 标上化合价 | 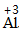 、 、 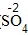 |
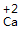 、 、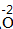 |
| 约简 | 将化合价的绝对值约成最简整数比 |  、 、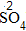 |
 、 、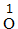 |
| 交叉 | 将整数交叉写在元素符号(或原子团)的右下角 |  |
 |
| 检验 | 根据正负化合价代数和是否为0,检验正误 | (+3)×2+(-2)×3=0 | (+2)+(-2)=0 |
确定化学式的几种方法:
1. 根据化合价规则确定化学式
例1:若A元素的化合价为+m,B元素的化合价为-n,已知m与n都为质数,求A,B两元素化合后的物质的化学式。
解析:由题意知正、负化合价的最小公倍数为m ·n,A的原子个数为(m·n)/m=n,B的原子个数为 (m·n)/n=m
答案:所求化学式为AnBm.
2. 根据质量守恒定律确定化学式
例2:根据反应方程式2XY+Y2==2Z,确定Z 的化学式
解析:根据质量守恒定律,反应前后原子种类不变,原子数目没有增减,反应前有两个X原子,四个Y原子,则两个Z分子含有两个X原子和四个Y原子。
答案:z的化学式为XY2
3. 利用原子结构特征确定化学式
例3:X元素的原子核外有17个电子,Y元素的原子最外层有2个电子,求X、Y两元素所形成的化合物的化学式。
解析:X元素的原子核外有17个电子,Y元素的原子最外层有2个电子,X原子易得1个电子,Y原子易失2个电子,根据电子得失相等可求化合物的化学式为YX2
4.利用元素质量比确定化学式:
例4:有一氮的氧化物,氮、氧两元素的质量比为7: 4,求此氧化物的化学式。
解析:设此氧化物的化学式为NxOy,根据xN:yO =7:4 得14x:16y=7:4,即x:y=2:1。
答案:所求氧化物的化学式为N2O。
5. 利用化学式中所含原子数、电子数确定化学式
例5:某氮氧化合物分子中含有3个原子,23个电子,求此化合物的化学式。
解析:设此化合物的化学式为NxOy,则
x+y=3
7x+8y=23
解得x=1,y=2
答案:所求化学式NO2。
利用化学式的变形比较元素的原子个数:
例:质量相等的SO2和SO3分子中,所含氧原子的个数比为?
解析:SO2的相对分子质量为64,SO3的相对分子质量为80,二者的最小公倍数是320,二者相对分子质量相等时物质的质量相同,转化为分子个数SO2 为320/64=5,SO3为320/80=4,即5SO2与4SO3质量相同,所以含氧原子的个数比为(5×2):(4×3)=10:12=5:6。
四、利用守恒法进行化学式计算:
例:由Na2S、Na2SO3、Na2SO4三种物质构成的混合物中,硫元素的质量分数为32%,则混合物中氧元素的质量分数为?
解析:在Na2S,Na2SO3,Na2SO4中,钠原子与硫原子的个数比是恒定的,都是2:1,因而混合物中钠、硫元素的质量比(或质量分数比)也是恒定的。设混合物中钠元素的质量分数为x,可建立如下关系式。
Na ——S
46 32
x 32%
46/32=x/32%
解得x=46%
混合物中氧元素的质量分数为1-32%-46%=22%。
利用平均值法判断混合物的组成
找出混合物中各组分的平均值(包括平均相对原子质量、平均相对分子质量、平均质量、平均质量分数等),再根据数学上的平均值原理,此平均值总是介于组成中对应值的最大值与最小值之间,由此对混合物的组分进行推理判断。
例:某气休可能由初中化学中常见的一种或多种气体组成,经测定其中只含C,O两种元素,其质量比为3:8,则该气体可能是?
解析:由题给条件知,该气体只含C,O两种元素,而这两种元素组成的气体可能是CO2、CO,O2。CO2中C,O两种元素的质量比是3:8,CO中C,O两种元素的质量比是3:4,O2中C,O两种元素的质量比是0 (因C的质量为0)。题中给出该气体中C,O两种元素的质量比是3:8,故符合题意的气体组成为:CO2或 CO,O2或CO,O2,CO2。
利用关系式法解题技巧:
关系式法是根据化学式所包含的各种比例关系,找出已知量之间的比例关系,直接列比例式进行计算的方法。
例: 多少克(NH4)2SO4与42.4g尿素CO(NH2)2所含的氮元素质量相等?
设与42.4g尿素中所含氮元素质量相等的(NH4)2SO4的质量为x
(NH4)2SO4——2N——CO(NH2)2
132 60
x 42.4g
132/x=60/42.4g
x=93.28
化学式前和化学式中数字的含义:
①化学式前面的数字表示粒子(原子、分子)数目;
②离子符号前的数字表示离子的数目;
③化学式石一下角的数字表示该粒子中对应原子或原子团的数目;
④离子符号右上角的数字表示该离子所带电荷数。

物质中某元素的质量分数,就是该元素的质量与组成物质的各元素总质量之比。
公式:
某元素的质量分数=

如AmBn中A元素的质量分数=

若题目给出物质的化学式,又同时知道物质的实际质量,则可根据物质的质量×某元素的质量分数=该元素的质量,将其中所含元素的质量求出。同理,物质的质量=某元素质量÷该元素的质量分数。
公式的理解:
计算时应先列式计算,然后代入数据算出结果。如水中氢元素的质量分数=
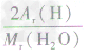 ×100%=
×100%= ×100%=
×100%= ×100%=11.1%而不能写成
×100%=11.1%而不能写成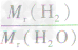 ×100%=
×100%= ×100%=
×100%= ×100%=11.1%
×100%=11.1%化学式中质量分数的应用:
①已知物质的质量求所含的某元素的质量
利用公式:元素的质量=物质的质量×该元素的质量分数
②已知元素的质量求物质的质量
利用公式:物质的质量=元素的质量÷该元素的质量分数
③根据元素的质量分数确定物质的化学式
利用化学式的变形比较元素质量分数的大小:
例:
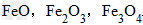 三种铁的氧化物按铁元素的质量分数由大到小排列的顺序为?
三种铁的氧化物按铁元素的质量分数由大到小排列的顺序为?解析:三种含铁的氧化物的化学式可变形为
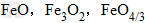 ,则三种含铁的氧化物中铁元素的质量分数分别为:
,则三种含铁的氧化物中铁元素的质量分数分别为: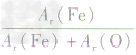 、
、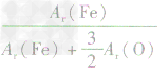 、
、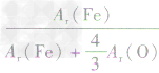 ,通过比较分母可知:
,通过比较分母可知: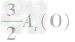 >
>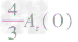 >Ar(O),故铁元素的质量分数由大到小排列的顺序为
>Ar(O),故铁元素的质量分数由大到小排列的顺序为 。
。合金是在金属中加热熔合某些金属或非金属形成的具有金属特性的物质。
①合金可以是金属与金属或金属与非金属的混合物,不一定全部由金属组成。
②合金具有金属特性,如导电性、导热性、延展性等。
③合金是几种成分熔合在一起形成的,发生的是物理变化,不是化学变化;合金不是几种成分简单地混合而成的。
④合金中各成分仍保持自己的性质。
合金与组成它们的金属的性质比较:
金属熔合了其他金属或非金属后,不仅组成上发生了变化,其内部结构也发生了改变,从而引起性质的变化。因而合金比纯金属具有更广泛的用途。 纯金属与合金性质的比较:
①合金一般比其组分金属的颜色更鲜艳。
②合金的硬度一般应工组成它的金属。
③合金的熔点一般低于成它的金属。
④合金的抗腐蚀能力一般强工组成它的金属。
⑤合金的导电性、导热隆能一般差于组成它的金属。
生铁和钢的比较:
| 含碳量 | 2%—4% | 0.03%—2% |
| 其他元素 | Si、Mn、S、P(少量) | Si、Mn等 |
| 机械性能 | 硬而脆,无韧性 | 坚硬,韧性大,塑性好,有弹性 |
| 机械加工性质 | 可铸不可锻 | 可铸,可锻,可压延 |
| 分类 | 白口铁,灰口铁,球墨铸铁 | 碳素钢,合金钢 |
知识点拨:
①生铁和熟铁:生铁是指含碳债在 2%一4.3%之间的铁合金,熟铁是用生铁精炼而成的较纯的铁,含碳量低于0.02%。
②生铁与铸铁:铸铁是生铁中的一种,是指可用来铸造的生铁,通常指球墨铸铁。
③碳素钢的性能与含碳址有关,含碳量越高,硬度越大,但韧性越差;含碳量越低,韧性越好,但硬度越小。
④纯铁与日常生活中铁的颜色差异日常生活,我们接触的铁一般不是纯铁,而是一些铁的氧化物或含铁的混合物,故我们常见的铁的颜色是黑色的,但它并不是纯铁的颜色,纯铁的颜色是银白色的。
应用广泛的合金:
(1)铁合金:铁合金包括生铁和钢,生铁和钢的主要成分是铁,钢与生铁的各种性能不同,主要是由于二者的含碳量不同。
生铁与钢的种类
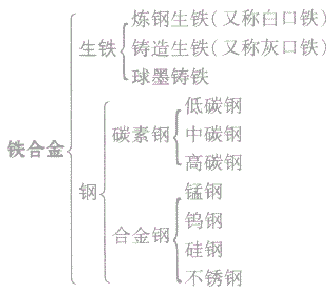
(2)生铁与钢:
生铁的含碳量为2%—4.3%
钢的含碳量为0.03%—2%
(3)钛和钛合金:钛和钛合金被认为是21世纪的重要金属材料。
①性质:优异的耐腐蚀性,对海水、空气和若干腐蚀介质都稳定,可塑性好,强度大,密度小,又称亲生物金属;
②用途:喷气发动机、飞机.机身、人造卫星外壳、火箭壳体、医学补形、人造骨、海水淡化设备、海轮和舰艇的外壳等。
与“化学与人类生活的关系越来越密切.(1)我们穿的衣服通常是由...”考查相似的试题有:
- 功能饮料可调节人体生理机能、补充营养素,按酸碱性可分为酸性与碱性两类.(1)甲基橙是一种酸碱指示剂.下表为甲基橙在不同...
- (7分)在实验课上,老师要同学们配制15%的氯化钠溶液50 g。(1)计算:配制15%的氯化钠溶液50 g,需氯化钠的质量为 g,水...
- 下列说法错误的是( )A.“洗涤剂”把“油乎乎”的菜盘洗干净,是洗涤剂乳化功能的体现B.在食盐的饱和溶液中,加入少量蔗糖,蔗...
- 高氯酸(HClO4)是最强酸.现有一种不常见的氯的化合物叫做高氯酸氯,其分子中氯的质量分数为0.526,且每个分子中含有4个氧原...
- 下列表示二个氮分子的是[ ]A. 2NB. 2N2C. N2D. 2N2O
- 下列物质的名称、俗名与化学式完全对应的是( )A.氯化钠 食盐 NaCIB.碳酸氢钠 纯碱 NaHC03C.氢氧化钠 火碱 NaOHD.氢氧化...
- 用化学符号或化学式表示:(1)3个水分子______(2)5个氮原子______(3)氢元素______(4)氧化镁______(5)地壳中含量最多...
- 我国科学家屠呦呦因为“发现青蒿素(一种用于治疗疟疾的药物),挽救了全球特别是发展中国家的数百万人的生命”而获拉斯克奖....
- 下列算式或计算结果正确的是( )A.CO中碳和氧的质量比为1:1B.NH3的式量为14+1×3=17C.“3SO2”的相对分子质量总和与“2SO3”...
- 汽车使用是人类进步的标志,但生产汽车的材料、使用的能源等是人们关注并需解决的问题。(1)制造汽车的材料以钢铁为主,钢是...