本试题 “按要求填写下列内容:实验过程或方法实验现象结论或解释Ⅰ.导管口A处有气泡冒出 Ⅱ.高锰酸钾制取氧气,用排水法收集。停止加热时,应先: 然后: ①为了防止水...” 主要考查您对装置气密性检验
氧气的制取和收集
S,Fe,C,P等物质在氧气中的燃烧
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 装置气密性检验
- 氧气的制取和收集
- S,Fe,C,P等物质在氧气中的燃烧
通过气体发生器与附设的液体构成封闭体系,依据改变体系内压强时产生的现象(如气泡的生成,水柱的形成,液面的升降等)来判断装置气密性的好坏。在实际检验过程中,由于气体发生器结构不同,因此检验方法也有一定的差异。
注意事项:
在中学化学实验及有关实验设计习题中,经常涉及装置的气密性检验问题。一般说来,无论采用那种装置制取气体,在成套装置组装完毕装入反应物之前,必须检查装置的气密性,以确保实验的顺利进行。
一些常见装置的检验方法总结如下,以供同学们参考:
1.如图1,此装置为最简易的制取气体装置,对于该装置的气密性检查,主要是通过气体受热后体积膨胀,压强增大。
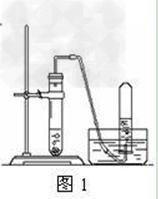
具体方法为:把导管口的下端浸入水中,用双手紧握试管。如果观察到导气管口有气泡冒出,则证明装置不漏气。
注意:若外部气温较高,实验现象不明显,我们可以使用酒精灯对试管底部微微加热,但现象一定要注意撤走酒精灯后,导管中能形成一段水柱,并且一段时间不下降,才能说明气密性好。
2.如图2所示,此装置漏斗与大气相通,无法如上例那样进行检查。要进行其气密性检查,首先要考虑的问题是如何使锥形瓶不直接通过漏斗与大气相通。要解决这一问题,显而易见的用水(或液体)做液封,从而实现这一目的。

具体方法为:从漏斗加入一定量的水,使漏斗的下端管口浸没在液面以下,夹紧弹簧夹,再加入少量的水,停止加水后,漏斗中与锥形瓶中液面差(即水柱高度)保持不变,说明该装置不漏气。
3.图3为启普发生器。该装置的原理与上图2的原理是一样的,但主要是该装置中弹簧夹被活塞代替。
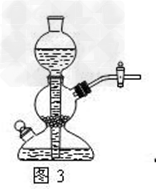
具体方法为:关闭导气管上的活塞,从球形漏斗中加入足量的水,使球形漏斗中出现水柱,水柱高度在一段时间内保持不变,则说明装置不漏气。
4.图4为利用双氧水和二氧化锰制取氧气的实验室装置,利用分液漏斗等仪器。这套装置与图2或图3不同,主要的原理与图1一样。

具体方法是:关闭分液漏斗上的活塞,把导气管的一端浸入水中,用双手紧握试管底部。如果观察到导气管口有气泡冒出,而且在松开手后,导管中形成一段水柱,则证明装置气密性好,不会漏气。
氧气的制取是初中化学的重点,也是历年中考的热点。我们不仅要学好氧气制取的知识,而且要触类旁通,逐步掌握实验室制取气体的一般思路和方法。中考对制取氧气的考查主要集中在药品选用、实验装置、操作步骤等方面。
实验室制取收集氧气:
| 过氧化氢制氧气 | 高锰酸钾制氧气 | |
| 药品和反应原理 | 2H2O2 2H2O+O2↑ 2H2O+O2↑ |
2KMnO4 K2MnO4 + MnO2 + O2↑ K2MnO4 + MnO2 + O2↑ |
| 发生装置 | 固液常温型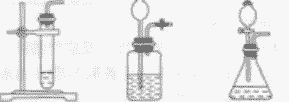 |
固体加热型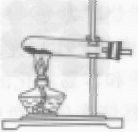 |
| 收集装置 | 氧气可用排水法收集,也可用向上排空气法收集 | |
| 整体装置图 | 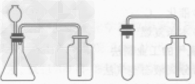 |
 |
| 操作步骤 | ①检查装置气密性 ②再锥形瓶中装入二氧化锰 ③塞好带有长颈漏斗和导管的橡皮塞(长颈漏斗的下端一定在液面以下,否则氧气会从长颈漏斗中跑出来) ④向长颈漏斗中加入过氧化氢溶液 ⑤收集氧气 |
①检查装置气密性 ②将药品平铺在试管底部,用带导管的单孔橡皮塞塞紧试管口(用高锰酸钾制取氧气,还要在管口放一小团棉花) ③将试管固定在铁架台上 ④点燃酒精灯,预热后加热试管 ⑤当导管口有连续均匀的气泡冒出时开始收集气体 ⑥收集完毕,先将导管移出水面 ⑦熄灭酒精灯。加热高锰酸钾(或氯酸钾和二氧化锰的混合物)制氧气,用排水法收集,其操作步骤可概括为:“查”“装”“定”“点”“收”“离”“熄”7个字。可用谐音记忆为“茶庄定点收利息”。 |
| 注意事项 | ①伸入试管或锥形瓶中的导管应刚刚露出橡皮塞即可,否则不利于气体的导出。 ②用排水法收集氧气时,导管应刚伸人集气瓶口即可,过长不利于水的排出,气体不易收集满。 ③用向上排空气法收集氧气时,导管要伸入集气瓶的底部,否则不利于空气的排出,收集的气体不纯。 ④用长颈漏斗时,长颈漏斗末端应在液面以下,否则氧气会从长颈漏斗中逸出。 |
①药品要平铺在试管底部,均匀受热。 ②试管口要略向下倾斜,防止药品中湿存的水分受热后变成水蒸气,遇冷凝结成水倒流回试管底部,使试管炸裂。 ③铁架台的铁夹要夹在试管的中上部(或距离试管口1/3处)。 ④试管内的导管稍伸出橡皮塞即可,这样便于气体导出。 ⑤集气瓶充满水后倒放入水槽中(瓶口要在水面下)。 ⑥加热时要先使试管均匀受热,然后酒精灯外焰要对准药品所在部位加热。 ⑦用排水法收集气体时,应注意当气泡连续均匀冒出时再收集,否则收集的气体中混有空气,当集气瓶口有大盆气泡冒出时,证明已集满。 ⑧停止加热时,应先把导管从水里撤出,再撤掉酒精灯。如果先熄灭酒精灯,试管内气体温度降低,压强减小,水槽中的水就会被倒吸入热的试管内,使试管炸裂。 ⑨用高锰酸钾制氧气时,试管口要放一小团棉花,防止加热时高锰酸钾小颗粒进人导管。 ⑩盛氧气的集气瓶应盖上玻璃片正放,因为在相同状况下氧气的密度大于空气的密度,正放可减少气体的逸散。 |
氧化的化学性质很活泼,很多物质都能与氧气发生化学反应。
部分物质在空气中和氧气中反应的对比:
a)碳和氧气反应
方程式:C + O2 CO2
CO2
现象:剧烈燃烧,发白光,放热,生成使澄清石灰水变浑浊的气体
b)硫和氧气反应
方程式:S + O2 SO2
SO2
现象:发出明亮的蓝紫色火焰,放热,生成有刺激性气味的气体
注意:实验前应在瓶底放少量水,用来吸收生成的有毒气体。
c)红磷和氧气反应:
方程式:4P + 5O2 2P2O5
2P2O5
现象:发出耀眼的白光,放热,生成大量白烟
生成的P2O5是固体小颗粒,现象为白烟,不是白雾。
d)铁和氧气的反应:
方程式:3Fe + 2O2 Fe3O4
Fe3O4
现象:剧烈燃烧,火星四射,放出热量,生成黑色物质
注意:集气瓶底放一层细沙或少量水。
e)镁和氧气反应:
方程式:2Mg + O2 2MgO
2MgO
现象:剧烈燃烧,发出耀眼的白光,放出热量,生成白色粉末状固体,有白烟。
注意:不能手持镁条,应用坩埚钳夹持。
f)石蜡和氧气反应
文字表达式:石蜡+氧气 水+二氧化碳
水+二氧化碳
现象:剧烈燃烧,放出热量,发出白光,如果在火焰上方罩一个干冷烧杯,
烧杯内壁有水珠,生成使澄清石灰水变浑浊的气体。
烟和雾的区别:
a)烟:大量固体小颗粒分散在空气长产生烟。红磷燃烧产生大量白烟,是燃烧生成的固体P2O5分散在空气中形成的
b)雾:大量小液滴分散在气体中产生雾。打开盛浓盐酸的瓶塞,瓶口有白雾,是挥发的HCl气体遇到空气中的水蒸气形成了盐酸小液滴。
a)光:固体物质燃烧使发光。镁条燃烧发出耀眼的强光,木炭在氧气中燃烧产生白光
b)气体物质和容易气化的物质燃烧时产生火焰。蜡烛在氧气中燃烧产生白色的火焰,是石蜡熔化后生成的气体燃烧而产生的。
描述物质在氧气中燃烧的现象的技巧:
可按三个顺序从三个方面进行:
(1)剧烈燃烧,有什么颜色的光,火焰;
(2)放热;
(3)生成物的特性
与“按要求填写下列内容:实验过程或方法实验现象结论或解释Ⅰ.导...”考查相似的试题有:
- 如图所示下列装置,请根据题目要求,回答下列问题.(1)写出仪器①和②的名称______、______.(2)实验室可用高锰酸钾固体或...
- 下列操作不正确的是( )A.氢气的检验B.读出液体的体积C.固体取用D.检查装置气密性
- (15分)请结合图10所示实验装置回答有关问题:(1)写出装置A中标号a和b的仪器名称:a ;b 。(2)检查装置B的气密性的方法...
- 写出下列反应的化学方程式并回答问题:(1) 过氧化氢溶液中加入二氧化锰____________,属于_________反应(填化合、分解)。(2) ...
- 为探究二氧化锰、氧化铜、氧化铁对过氧化氢溶液分解速率的影响,需要控制相关变量.其中没有必要进行控制的变量是( )A.过...
- 请结合图示回答问题:(1)实验室用A装置制取O2时,所用的药品是______.(2)实验室用B装置作为发生装置,并用图C所示的方法...
- 下列有关实验现象的描述中,正确的是A.镁条中滴加稀盐酸后,迅速产生大量气泡,同时试管壁发热B.高温加热氧化铜与木炭的混...
- (7分)2012年1月,广西河池宜州市境内龙江河发生了镉浓度超标事件。根据该事件某化学活动小组开展了一次关于金属镉与铜、银...
- 向硫酸铜溶液中加入一定量的铁粉充分反应后过滤。下列情况可能出现的是( )①滤液中有硫酸亚铁、硫酸铜,滤出的固体为铜②滤液...
- 根据下图所示实验,并阅读小资料,回答下列问题.(1)图1中反应的化学方程式为_____________________,集气瓶中加入液体的作...