本试题 “既可以通过单质与单质的化合,又可以通过溶液间的复分解反应得到的化合物是[ ]A.FeCl3B.CuSC.Fe2O3D.FeCl2” 主要考查您对氧化铁
铁盐(三价铁离子)
亚铁盐(二价铁离子)
铜盐(二价铜)
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 氧化铁
- 铁盐(三价铁离子)
- 亚铁盐(二价铁离子)
- 铜盐(二价铜)
氧化铁:
化学式Fe2O3,溶于盐酸,为红棕色粉末。其红棕色粉末为一种低级颜料,工业上称氧化铁红,用于油漆、油墨、橡胶等工业中,可做催化剂,玻璃、宝石、金属的抛光剂,可用作炼铁原料。
(1)色态:红色粉末,俗称铁锈(铁红)
(2)溶解性:溶于盐酸、稀硫酸生成+3价铁盐;难溶于水,不与水反应。
(3)氧化性:高温下被CO、H2、Al、C、Si等还原
氧化铁的化学性质:
- 铝热反应:2Al+Fe2O3=(高温)=Al2O3+2Fe
- 与强酸反应:Fe2O3+6H+==2Fe3++3H2O
- 与还原性酸(HI)反应:Fe2O3+6H++2I-==2Fe2++3H2O+I2
铁的氧化物:
| 化学式 | FeO | Fe2O3 | Fe3O4 |
| 俗称 | —— | 铁红 | 磁性氧化铁 |
| 色态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
| 铁的价态 | +2 | +3 | +2、+3 |
| 水溶性 | 不溶 | 不溶 | 不溶 |
| 与酸反应 | FeO+2H+==Fe2++H2O | Fe2O3+6H+==2Fe3++3H2O | Fe3O4+8H+==Fe2++2Fe3++4H2O |
| 用途 | 玻璃色料 | 油漆、颜料 | 做颜料和抛光剂 |
| 氧化性 | 高温时都能与C、CO、H2反应,被还原生成Fe单质 | ||
Fe3+的性质:
含Fe3+的溶液都呈黄色,具有氧化性,
(1)与还原剂反应生成二价铁 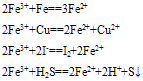
(2)与碱反应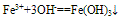
(3)Fe3+在水中易水解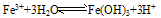
由于三价铁易水解,在保存铁盐盐溶液(FeCl3)时加入少量相应的酸(HCl),以防止Fe3+水解。
“铁三角”中的转化关系:
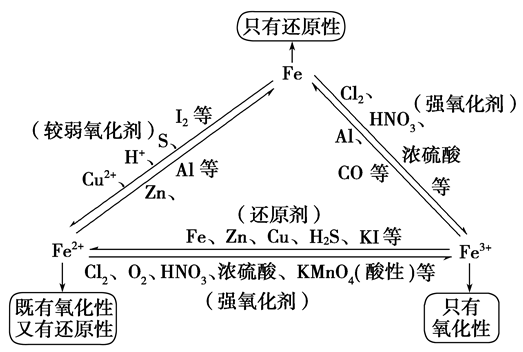
浅绿色溶液,既有氧化性性又具有还原性,主要表现还原性
(1)与氧化剂反应生成三价铁 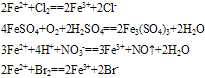
(2)与碱反应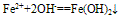
(3)Fe2+易被氧化,水溶液中易水解。亚铁盐溶液(FeCl2)在保存时加入少量铁屑以防止Fe2+被氧化,滴入少量相应的酸溶液(HCl),防止Fe2+水解。
硫酸铜:
五水合硫酸铜(CuSO4·5H2O)为天蓝色晶体,水溶液呈弱酸性,俗名胆矾或蓝矾。硫酸铜是制备其他铜化合物的重要原料。同石灰乳混合可得波尔多液,用作杀菌剂。硫酸铜也是电解精炼铜时的电解液。
硫酸铜的物理性质和化学性质:
(1)物理性质:白色粉末状固体,不溶于乙醇和乙醚,易溶于水,水溶液呈蓝色,是强酸弱碱盐,水溶液呈弱酸性。将硫酸铜溶液浓缩结晶,可得五水硫酸铜蓝色晶体,俗称胆矾、铜矾或蓝矾。
(2)化学性质:
①二价铜与碱反应生成蓝色沉淀Cu(OH)2,Cu(OH)2溶于氨水形成深蓝色溶液[Cu(NH3)4]2+,此性质可以检验Cu2+。无水硫酸铜遇水变成蓝色(CuSO4·5H2O),可作为水的检验的依据。
②胆矾在常温常压下很稳定,不潮解,在干燥的空气中会逐渐风化(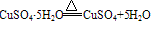 ),加热到45℃时失去2分子结晶水,110℃时失去4分子结晶水,150℃失去全部结晶水。将胆矾加热至650℃高温,可分解为黑色氧化铜、二氧化硫和氧气。
),加热到45℃时失去2分子结晶水,110℃时失去4分子结晶水,150℃失去全部结晶水。将胆矾加热至650℃高温,可分解为黑色氧化铜、二氧化硫和氧气。
(3)Cu2+的化学性质:能被活泼金属将其从盐溶液中置换出来:例:Cu2++Fe==Cu+Fe2+
硫酸铜的用途和制法:
(1)用途:硫酸铜较重要的铜盐之一,在电镀、印染、颜料、农药等方面有广泛的应用。无机农药波尔多液就是硫酸铜和消石灰的混合液,是一种良好的杀菌剂,可防止多种作物的病害。硫酸铜也常用来制备其他铜的化合物和电解精炼铜的电解液。
(2)制法:五水合硫酸铜可由铜或氧化铜与硫酸作用后,浓缩结晶而制得。在实验室中可用浓硫酸氧化金属铜来制取无水硫酸铜。
与“既可以通过单质与单质的化合,又可以通过溶液间的复分解反应...”考查相似的试题有:
- 以下物质间的每步转化通过一步反应能实现的是( )A.Al-Al2O3-Al(OH)3-NaAlO2B.Fe-FeCl3-Fe(OH)3-Fe3O4C.S-SO3-H2SO4-...
- 金属铁分别与单质Cl2和Br2反应可得无水FeCl3和FeBr3,当把铁粉与碘粉混合一起研磨时,生成相当于Fe3I8的产物,则在此产物中铁...
- FeCl3、CuCl2的混合溶液中加入铁粉,充分反应后仍有固体存在,则下列判断不正确的是A 加入KSCN溶液变红色 B 溶液中一定含Fe2+...
- 纳米是长度单位,l nm="10" -9m,当物质的颗粒达到纳米级时,会具有一些特殊的性质。例如由铜制成“纳米铜”具有非常强的化学活...
- 将12.8克由CuSO4和Fe组成的固体,加入足量的水中充分反应后,滤出固体,干燥后称得5.2克。求原混合物中CuSO4和Fe各为多少克?
- 各物质之间的转化关系如下图,部分生成物省略.A是含有四种元素的化合物,C、D是由X、Y、Z中两种元素组成的化合物,X、Y、Z的...
- 能证明Fe3+具有氧化性的微粒是( )①SCN-②Fe③Fe2+④Cu⑤I-⑥OH-. A.①②③ B.②④⑤ C.①②⑤ D.①③⑥
- I、摩尔盐制备:将绿矾(FeSO4·7H2O)硫酸铵以相等物质的量混合可制得摩尔盐晶体。根据下图回答(1)步骤1中Na2CO3的主要作用...
- 下列物质能通过化合反应直接制得的是[ ]①FeCl2②H2SO4③NH4NO3④HClA.只有①②③B.只有②③C.只有①③④D.全部
- 胆矾是一种蓝色晶体,化学式是CuSO4·5H2O,胆矾受热时易失去结晶水,成为白色的无水CuSO4粉末,无水CuSO4易吸收水份又变成蓝...