本试题 “(17分)纯碱在日常生活和工业生产中用途广泛,需求量很大,因此纯碱的制备一直是科学家工作的一个重要方面。19世纪欧洲有个吕布兰制碱法,其主要反应原理是...” 主要考查您对化学与技术
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 化学与技术
化学技术在工农业生产有重要应用:
1.应用合成氨技术生产铵态氮肥,有利于农业生产;工业上生产磷肥、钾肥等。

2.接触法制硫酸,有利于工业生产。
(1)原料:主要有黄铁矿、硫黄等。
(2)原理:以黄铁矿为原料生产硫酸为例,生产主要经过三个阶段。
(3)有关反应

工业上并不直接用水吸收三氧化硫,而是用质量分数为98.3%的浓硫酸作吸收剂,因为三氧化硫与水蒸气容易形成酸雾,从而降低三氧化硫的吸收率。同时采用逆流吸收,硫酸从塔底放出。
3.工业上制取纯碱--联合之间法
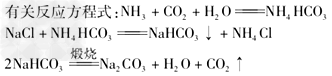
1.应用合成氨技术生产铵态氮肥,有利于农业生产;工业上生产磷肥、钾肥等。

2.接触法制硫酸,有利于工业生产。
(1)原料:主要有黄铁矿、硫黄等。
(2)原理:以黄铁矿为原料生产硫酸为例,生产主要经过三个阶段。
(3)有关反应

工业上并不直接用水吸收三氧化硫,而是用质量分数为98.3%的浓硫酸作吸收剂,因为三氧化硫与水蒸气容易形成酸雾,从而降低三氧化硫的吸收率。同时采用逆流吸收,硫酸从塔底放出。
3.工业上制取纯碱--联合之间法
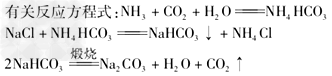
发现相似题
与“(17分)纯碱在日常生活和工业生产中用途广泛,需求量很大,...”考查相似的试题有:
- 13C—NMR(核磁共振)、15N—NMR可用于测定蛋白质、核酸等生物大分子的空间结构,库尔特·维特里希等人为此获得2002年诺贝尔化学...
- 合成氨的反应采用400~500 ℃温度的原因是( )。A.温度太低反应速率太小B.该温度时催化剂活性较高C.该温度时反应速率最大D...
- 2013年度诺贝尔化学奖再次授予计算化学领域的科学家。以下基于结构理论进行繁难计算得出的是A.天然气的热值B.合成氨的原子...
- 人们对于化学科学有各种各样的认识,其中错误的是[ ]A.化学面对日益严重的环境问题显的无能为力,升学时考不考无关大局B.化...
- 形形色色的物质是怎样构成的?它们为什么会有各种各样的性质?我们通过( )的学习就可以找到答案A.语文B.历史C.物理D.化学
- “碳捕捉技术”是指通过一定的方法将工业生产中产生的CO2分离出来并利用。如可利用NaOH溶液来“捕捉”CO2,其基本过程如下图所示...
- “碳捕捉和储存(CCS)”技术是指通过碳捕捉技术,将工业和有关能源产业所产生的二氧化碳分离出来再利用。当前,二氧化碳及其产品...
- 研究气体在固体表面反应的化学已经成为化学学科的一个重要分支,它涉及生产、生活中的许多重要领域。下列不属于气体与固体作...
- 海水资源的利用具有非常广阔的前景。(1)海水淡化的主要方法有(只写出1种即可)________。(2)海水中丰富的氯化钠是重要的...
- 2010年上海世博会的主题是“城市,让生活更美好”。下列叙述中不正确的是A.世博会前期,处理废水时加入明矾可作为混凝剂以吸附...