本试题 “(1)下列物质能导电的是______,属于电解质的是______,属于非电解质的是______.①水银 ②烧碱 ③干冰 ④氯化钠晶体 ⑤盐酸溶液 ⑥蔗糖(C12H22O11)(2)任选一...” 主要考查您对电离方程式
电解质、非电解质
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 电离方程式
- 电解质、非电解质
定义:
表示电解质电离的式子。强电解质电离用“=”,弱电解质电离用“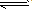 ” 。
” 。
.
表示电解质电离的式子。强电解质电离用“=”,弱电解质电离用“
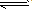 ” 。
” 。.
电离方程式的书写:
1.强电解质的电离用“ ”,弱电解质的电离用 “
”,弱电解质的电离用 “ ”。
”。
2.多元弱酸分步电离,分步持写电离方程式,一般只写第一步;多元弱碱也是分步电离的,但可按一步完全电离写出。例如:
氧硫酸: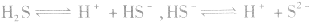
氢氧化铁:
3.强酸的酸式盐完全电离,弱酸的酸式盐中酸式酸根不完全电离。例如: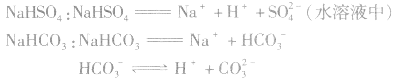
说明:在熔融状态时,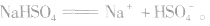
4.某些复盐能完全电离。例如:
电解质和非电解质:
1.电解质和非电解质在水溶液里或熔融状态下能导电的化合物,叫做电解质。在水溶液里和熔融状态下都不导电的化合物,叫做非电解质。
2.电解质和非电解质的比较

说明(1)电解质、非电解质均是化合物。
(2)电解质导电必须有外界条件:水溶液或熔融状态。
(3)电解质是一定条件下本身电离而导电的化合物。CO2、SO2、SO3、NH3溶于水后也导电,但是与水反应生成的新物质电离而导电的,不是本身电离而导电的,故属于非电解质。
(4)电解质的强弱由物质的内部结构决定,与其溶解度无关。某些难溶于水的化合物,如BaSO4、AgCl,虽然溶解度很小,但溶解的部分是完全电离的,所以是强电解质。
(5)电解质不一定导电,非电解质一定不导电;导电的物质不一定是电解质,不导电的物质不一定是非电解质。
1.电解质和非电解质在水溶液里或熔融状态下能导电的化合物,叫做电解质。在水溶液里和熔融状态下都不导电的化合物,叫做非电解质。
2.电解质和非电解质的比较

说明(1)电解质、非电解质均是化合物。
(2)电解质导电必须有外界条件:水溶液或熔融状态。
(3)电解质是一定条件下本身电离而导电的化合物。CO2、SO2、SO3、NH3溶于水后也导电,但是与水反应生成的新物质电离而导电的,不是本身电离而导电的,故属于非电解质。
(4)电解质的强弱由物质的内部结构决定,与其溶解度无关。某些难溶于水的化合物,如BaSO4、AgCl,虽然溶解度很小,但溶解的部分是完全电离的,所以是强电解质。
(5)电解质不一定导电,非电解质一定不导电;导电的物质不一定是电解质,不导电的物质不一定是非电解质。
发现相似题
与“(1)下列物质能导电的是______,属于电解质的是______,属于...”考查相似的试题有:
- 下列电离方程式书写正确的是( ) A.CH3COONH4═CH3COO-+NH4+ B.HI=H++I- C.H2S═2H++S2- D.NaHCO3=Na++H++CO32-
- 下列电离方程式正确的是 A.NaHS溶于水:NaHS===Na++HS-,HS-+H2OH3O++S2-B.KH2PO4溶于水:H2PO2H++POC.HF溶于水...
- 下列物质中,属于电解质的是( )A.稀盐酸B.Cu丝C.NaClD.蔗糖
- (6分).现有以下物质:①NaCl晶体 ②干冰 ③液态的醋酸 ④铜 ⑤BaSO4固体 ⑥蔗糖 ⑦酒精 ⑧熔融的KNO3 ⑨浓HNO3 回答下列问题(填序...
- 下列物质能导电且属于电解质的是( )A.石墨B.NaCl溶液C.氯化钠固体D.熔融的NaOH
- 下列物质中,属于电解质的是( )A.铜丝B.MgCl2固体C.NaCl溶液D.酒精(C2H5OH)
- 下列事实能说明氨水是弱电解质的是:A.氨水与氯化铝溶液反应产生氢氧化铝沉淀B.用氨水做导电实验,灯泡很暗C.0.1mol/L的氨...
- 下列物质中属于电解质的是( )A.硫酸铜B.氮气C.酒精D.蔗糖
- 下列物质中,属于电解质的是( )A.氯气B.二氧化碳C.氯化钠D.蔗糖
- 有关电解质的说法正确的是( )A.NaOH是电解质,所以NaOH固体能导电B.CO2水溶液能够导电,所以CO2是电解质C.蔗糖、酒精在...