本试题 “下列说法正确的是[ ]A.t°C时,某溶液的PH=6,则该溶液一定为酸性B.欲制备Fe(OH)3胶体,向盛有沸水的烧杯中滴加FeCl3饱和溶液并长时间煮沸C.由单质A转化为...” 主要考查您对吸热反应、放热反应
溶液的酸碱性
氢氧化铁(胶体)的制备
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 吸热反应、放热反应
- 溶液的酸碱性
- 氢氧化铁(胶体)的制备
吸热反应:
吸收热量的反应,即生成物的总能量大于反应物的总能量,反应需要吸收能量
放热反应:
放出热量的反应,即生成物的总能量小于反应物的总能量,反应释放出能量
放热反应和吸热反应的比较:
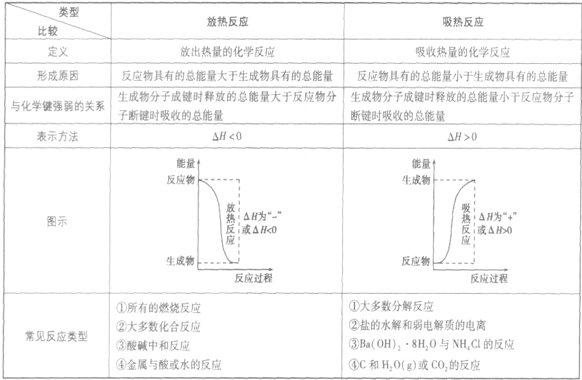
吸收热量的反应,即生成物的总能量大于反应物的总能量,反应需要吸收能量
放热反应:
放出热量的反应,即生成物的总能量小于反应物的总能量,反应释放出能量
放热反应和吸热反应的比较:

溶液的酸碱性:
(1)pH=-lg[c(H+)],在溶液的c(H+)很小时,用pH来表示溶液的酸度。
(2)pH越大,c(H+)越小,c(OH-)越大,酸性越弱,碱性越强。pH越小,c(H+)越大,c(OH-)越小,酸性越强,碱性越弱。
(3)pH的范围:0~14
(4)溶液酸碱性判断:
当c(H+)>c(OH-)时,溶液呈酸性;
当c(H+)>=c(OH-)时,溶液呈键性;
当c(H+)<c(OH-)时,溶液呈中性。
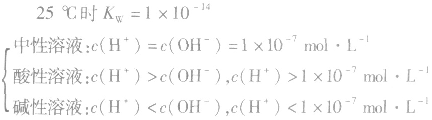
(5)关于pH相同的酸(含强酸和弱酸)
①溶液中c(H+)相等(填“相等”或“不等”)。
②溶液中溶质的物质的量的浓度:强酸<弱酸(填“>”或“<”)。
③耗碱规律:pH和溶液体积均相同的HCl、H2SO4、CH3COOH与碱完全反应时,消耗碱物质的量最多的是CH3COOH。
④稀释规律:分别加水稀释m倍时,溶液的物质的量的浓度均变为原来的1/m,强酸中c(H+)变为原来的1/m,但弱酸中c(H+)减小小于(填“大于”或“小于”)m倍,故稀释后弱酸酸性强于强酸。
(1)pH=-lg[c(H+)],在溶液的c(H+)很小时,用pH来表示溶液的酸度。
(2)pH越大,c(H+)越小,c(OH-)越大,酸性越弱,碱性越强。pH越小,c(H+)越大,c(OH-)越小,酸性越强,碱性越弱。
(3)pH的范围:0~14
(4)溶液酸碱性判断:
当c(H+)>c(OH-)时,溶液呈酸性;
当c(H+)>=c(OH-)时,溶液呈键性;
当c(H+)<c(OH-)时,溶液呈中性。
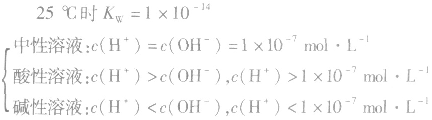
(5)关于pH相同的酸(含强酸和弱酸)
①溶液中c(H+)相等(填“相等”或“不等”)。
②溶液中溶质的物质的量的浓度:强酸<弱酸(填“>”或“<”)。
③耗碱规律:pH和溶液体积均相同的HCl、H2SO4、CH3COOH与碱完全反应时,消耗碱物质的量最多的是CH3COOH。
④稀释规律:分别加水稀释m倍时,溶液的物质的量的浓度均变为原来的1/m,强酸中c(H+)变为原来的1/m,但弱酸中c(H+)减小小于(填“大于”或“小于”)m倍,故稀释后弱酸酸性强于强酸。
溶液的pH:
1.定义:溶液里H+的物质的量浓度的负对数叫做pH。
2.表达式:
3.含义: pH越大,c(H+)越小,c(O-一)越大,酸性越弱,碱性越强。pH越小,c(H+)越大,c(OH-)越小,酸性越强,碱性越弱。
4.适用范围:
c(H+)很小时,用pH来表示溶液的酸碱度更方便。所以,pH适用于酸、碱的稀溶液
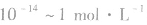 之间],pH取值范刚为0~14。
之间],pH取值范刚为0~14。
5.溶液的酸碱性和pH: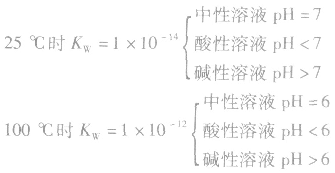
氢氧化铁胶体的制备:
(1)氢氧化铁胶体的制备:
往100mL烧杯中加入50mL水并加热至沸腾,向沸水滴加几滴饱和氯化铁溶液,继续煮沸至溶液呈红褐色,即停止加热。
注意:
(1)实验过程不能用玻璃棒搅拌,否则溶液出现浑浊;
(2)当反应体系呈现红褐色,即制得氢氧化铁胶体,应立即停止加热,否则也容易出现浑浊,产生红褐色的氢氧化铁沉淀。
(2)氢氧化铁的制备:
①原理:FeCl3+3NaOH=Fe(OH)3↓+3NaCl
②操作方法:向试管里注入少量氯化铁溶液,再逐滴滴入氢氧化钠溶液,观察现象。
③现象:有红褐色沉淀产生。
(1)氢氧化铁胶体的制备:
往100mL烧杯中加入50mL水并加热至沸腾,向沸水滴加几滴饱和氯化铁溶液,继续煮沸至溶液呈红褐色,即停止加热。
注意:
(1)实验过程不能用玻璃棒搅拌,否则溶液出现浑浊;
(2)当反应体系呈现红褐色,即制得氢氧化铁胶体,应立即停止加热,否则也容易出现浑浊,产生红褐色的氢氧化铁沉淀。
(2)氢氧化铁的制备:
①原理:FeCl3+3NaOH=Fe(OH)3↓+3NaCl
②操作方法:向试管里注入少量氯化铁溶液,再逐滴滴入氢氧化钠溶液,观察现象。
③现象:有红褐色沉淀产生。
发现相似题
与“下列说法正确的是[ ]A.t°C时,某溶液的PH=6,则该溶液一定为...”考查相似的试题有:
- 下列说法正确的是( )A.化学反应除了生成新物质外,还伴随着能量的变化B.放热反应全部不需要加热即可发生C.需要加热条件...
- 下列说法正确的是[ ]A.需加热才能发生的反应一定是吸热反应B.任何放热反应在常温条件下一定能发生C.反应物和生成物分别具...
- 关于下列图示的说法中正确的是[ ]A.图①表示可逆反应“CO(g) + H2O(g)CO2(g)+H2(g)”中的ΔH大于0B.图②为电解硫酸铜溶液的装置...
- 下列说法中,正确的一组是[ ]①是氢元素的三种核素,互称为同位素②饮用水可以用明矾、漂白粉来净化,两者的作用原理相同③化合...
- 下列说法正确的是[ ]A.焓变是指在恒压、恒温下,体系不做体积功,只做其他功的变化过程的热效应B.书写热化学方程式时若不标...
- 下列变化过程,属于放热过程的是( )①液态水变成水蒸气; ②酸碱中和反应; ③浓H2SO4稀释; ④固体氢氧化钠溶于水; ⑤H2在Cl2...
- 煤燃烧的反应热可通过以下两个途径来利用:a.利用煤在充足的空气中直接燃烧产生的反应热;b.先使煤与水蒸气反应得到氢气和...
- 在25℃时,有pH为a的盐酸和pH为b的NaOH溶液,取VaL该盐酸,同该NaOH溶液中和,需VbL NaOH溶液,填空:(1)若a+b=14,则Va:Vb=...
- 水的电离平衡曲线如图所示,若以A点表示25℃时水的电离达平衡时的离子浓度,B点表示100℃时水的电离达平衡时的离子浓度,则下列...
- 氯化铁是常见的水处理剂,无水FeCl3的熔点为555K、沸点为588K。工业上制备无水FeCl3的一种工艺如下:无水FeCl3的一种工艺如下...