本试题 “在下列物质种类中,前者包含后者的是[ ]A.单质 化合物B.电解质 化合物C.浊液 胶体D.混合物 溶液” 主要考查您对溶液
浊液
胶体
物质的简单分类
电解质、非电解质
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 溶液
- 浊液
- 胶体
- 物质的简单分类
- 电解质、非电解质
一种或几种物质分散到另一种物质中,形成均一、稳定的混合物,分散质粒子的直径d<10-9m
电中性原理:
溶液对外是不显电性的,所以,在电解质的溶液中,阳离子所带正电荷总数=阴离子所带负电荷总数。
如含K+、Al3+、H+、Cl-、SO42-的溶液中,必然存在c(K+)+3c(Al3+)+c(H+)=c(Cl-)+2c(SO42-)。
溶液的稀释定律:
- 稀释前后溶液中溶质的物质的量不变: c(浓溶液)V(浓溶液)=c(稀溶液)V(稀溶液)
- 稀释前后溶液中溶质的质量不变: ρ(浓溶液)V(浓溶液)w%(浓溶液)=ρ(稀溶液)V(稀溶液)w%(稀溶液)
容量瓶的使用:
1.容量瓶的使用及注意事项
(1)在使用前首先要检查是否漏水。
具体操作如下:
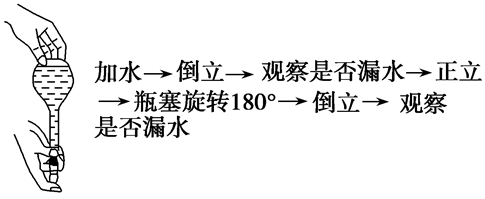
(2)检查合格后,用蒸馏水洗涤干净。
(3)四个“不能”
①不能将固体或浓溶液直接在容量瓶中溶解或稀释。
②不能作为反应容器或长期贮存溶液。
③容量瓶的容积是在瓶身所标温度下确定的,因而不能将过冷或过热的溶液转移到容量瓶中。
④只能配制容量瓶上规定容积的溶液,即不能配制任意体积的溶液。
2. 误差分析
分析依据 ,以配置NaOH溶液为例,在进行误差分析时,根据实验操作弄清是“m”还是“V”引起的误差,再具体分析,具体情况如下:
,以配置NaOH溶液为例,在进行误差分析时,根据实验操作弄清是“m”还是“V”引起的误差,再具体分析,具体情况如下:
| 能引起误差的一些操作 | 因变量 | c(mol/L) | |
| m | V | ||
| 砝码与物品颠倒(使用游码) | 减小 | —— | 偏低 |
| 称量时间过长 | 减小 | —— | |
| 用滤纸称NaOH | 减小 | —— | |
| 向容量瓶注液时少量溅出 | 减小 | —— | |
| 未洗涤烧杯和玻璃棒 | 减小 | —— | |
| 定容时,水多用滴管吸出 | 减小 | —— | |
| 定容摇匀后液面下降再加水 | —— | 增大 | |
| 定容时仰视刻度线 | —— | 增大 | |
| 砝码沾有其他物质或已生锈 | 增大 | —— | 偏高 |
| 未冷却至室温就注入容量瓶定容 | —— | 减小 | |
| 定容时俯视读数 | —— | 减小 | |
| 称量前小烧杯内有水 | —— | —— | 不变 |
| 定容后经振荡、摇匀,静置液面下降 | —— | —— | |
特别提醒:
(1)定容、摇匀后液面下降也不要补加蒸馏水,否则结果会偏低。
(2)定容时俯视、仰视对结果的影响。
①仰视刻度线(图1),导致溶液体积偏大。
②俯视刻度线(图2),导致溶液体积偏小。

为减小误差务必按:眼睛视线→刻度线→凹液面最低处的次序,做到“三点一线”。
一定物质的量浓度的溶液的配置:
1.主要仪器 (1)托盘天平:可精确至0.1g,称量前先调零,称量时物品放在左盘,砝码放在右盘。
(2)容量瓶:配制溶液的专用精确容器,瓶上标有温度、容积和刻度线。
(3)其他仪器:量筒、烧杯、玻璃棒、胶头滴管等。
2.配制过程
配制过程如下:

以配制480mL1mol·L-1NaCl溶液为例:
(1)所需容量瓶规格:500mL容量瓶。
(2)若用托盘天平应称量NaCl粉末29.3g。
(3)溶解过程中玻璃棒的作用为:搅拌加速溶解。
(4)移液
①移液前需要将溶液冷却至室温。
②移液中玻璃棒的作用为:引流。
③移液时需要进行的操作为:将烧杯中溶液注入容量瓶中,用少量蒸馏水洗涤烧杯内壁2~3次并将洗涤液也转入容量瓶中,轻轻摇动容量瓶,使溶液混合均匀。
(5)定容
①当液面距瓶颈刻度线1~2cm时改用胶头滴管滴加蒸馏水。
②定容时要平视刻度线,直到凹液面最低点与刻度线相切。
(6)摇匀,转入试剂瓶保存
假如其他操作均准确无误,分析下列情况对配制浓度的影响。
①定容时俯视观察刻度线:偏高;
②移液时,对用于溶解NaCl的烧杯没有洗涤:偏低;
③定容后,将容量瓶振荡摇匀,静置后发现液面低于刻度线,又补水至刻度线:偏低。
溶液配制过程中的“四个数据”:
(1)选择容量瓶的规格时应该与所配溶液体积相等或稍大
数据
要求或解释
药品的质量
实验室中一般用托盘天平称量药品,而托盘天平只能称准0.1g,所以记录数据时只能保留小数点后一位数字。如题中NaOH的质量为10.0,不能写为10.00g
容量瓶的规格
(2)回答补充仪器的问题时应该注明容量瓶的规格,如应该回答“500ml容量瓶”,不能只回答“容量瓶”。
洗涤烧瓶2-3次
移液时洗涤烧瓶2-3次是为了确保溶质全部转移入容量瓶中,否则会导致溶液浓度偏低
液面离容量瓶颈刻度线下1-2cm
定容时,当液面离容量瓶颈刻度线下1-2cm时,应该改用胶头滴管滴加,否则溶液导致液体体积超过刻度线,导致溶液浓度偏低
浊液:
粒子直径大于100nm的分散系,若分散质为固体小颗粒的称为悬浊液,若分散质为小液滴的称为乳浊液。
悬浊液是固体的小颗粒分散在溶剂中所形成的混合物;
乳浊液是液体的小液滴分散在溶剂中所形成的混合物。
浊液的特性:
浊液里的固体小颗粒或小液滴都是由巨大数量的分子(或原子等)集合而成的。浊液静置后,其中的固体小颗粒或小液滴会逐渐下沉或上浮。所以浊液中物质的分散是不均一、不稳定的。
分散系比较:
| 分散系 | 溶液 | 胶体 | 悬浊液 | 乳浊液 |
| 分散质粒子大小 | <1nm | 1~100nm | >100nm | >100nm |
| 分散质粒子结构 | 分子、离子 | 少量分子的结合体或大分子 | 大量分子聚集成的固体小颗粒 | 大量分子聚集成的液体小液滴 |
| 特点 | 均一、透明、稳定 | 多数均一、透明、较稳定 | 不均一、不透明、久置沉淀 | 不均一、不透明、久置分层 |
| 能否透过滤纸 | 能 | 能 | 不能 | —— |
| 实例 | 食盐水、蔗糖溶液 | Fe(OH)3(胶体)、淀粉胶体 | 泥水、石灰乳 | 牛奶、油漆 |
胶体:分散质粒子直径在10-9m~10-7m之间的分散系胶粒直径的大小是胶体的本质特征
胶体可分为固溶胶、液溶胶、气溶胶
①常见的液溶胶:Fe(OH)3、AgI、牛奶、豆浆、粥等
②常见的气溶胶:雾、云、烟等;
③常见的固溶胶:有色玻璃、烟水晶等胶体的性质:
丁达尔效应:
①当光束通过氢氧化铁胶体时,可以看到一条光亮的通路,这条光亮的通路是由于胶体粒子对光线散射(光波偏离原来方向而分散传播)形成的,即为丁达尔效应。
②布朗运动:粒子在不停地、无秩序的运动
③电泳:胶体粒子带有电荷,在电场的作用下,胶体粒子在分散剂里定向移动。一般来讲:金属氢氧化物,金属氧化物的胶粒吸附阳离子,胶体微粒带正电荷;非金属氧化物,金属硫化物的胶体胶粒吸附阴离子,胶体微粒带负电荷。
④胶体聚沉:向胶体中加入少量电解质溶液时,由于加入的阳离子(或阴离子)中和了胶体粒子所带的电荷,使胶体粒子聚集成为较大的颗粒,从而形成沉淀从分散剂里析出。该过程不可逆。
胶体的特性:
(1)丁达尔效应当一束光通过胶体时,胶体内会出现一条光亮的通路,这是由胶体粒子对光线散射而形成的,利用丁达尔效应可区分胶体和浊液。
(2)介稳性:胶体的稳定性介于溶液和浊液之间,在一定条件下能稳定存在,但改变条件就有可能发生聚沉。
(3)聚沉:给胶体加热、加入电解质或加入带相反电荷的胶体颗粒等均能使胶体粒子聚集成较大颗粒,从而形成沉淀从分散剂里析出。聚沉常用来解释生活常识,如长江三角洲的形成、明矾净水等。
(4)电泳现象:在电场作用下,胶体粒子在分散剂中作定向移动。电泳现象说明胶体粒子带电。电泳常用来分离提纯胶体,如工业上静电除尘。
分散系比较:
| 分散系 | 溶液 | 胶体 | 悬浊液 | 乳浊液 |
| 分散质粒子大小 | <1nm | 1~100nm | >100nm | >100nm |
| 分散质粒子结构 | 分子、离子 | 少量分子的结合体或大分子 | 大量分子聚集成的固体小颗粒 | 大量分子聚集成的液体小液滴 |
| 特点 | 均一、透明、稳定 | 多数均一、透明、较稳定 | 不均一、不透明、久置沉淀 | 不均一、不透明、久置分层 |
| 能否透过滤纸 | 能 | 能 | 不能 | —— |
| 实例 | 食盐水、蔗糖溶液 | Fe(OH)3(胶体)、淀粉胶体 | 泥水、石灰乳 | 牛奶、油漆 |
胶体发生聚沉的条件:
因胶粒带电,故在一定条件下可以发生聚沉:
- 向胶体中滴加电解质
- 向胶体中加入带相反电荷胶粒的胶体
- 加热
常见的胶体的带电情况:
- 胶粒带正电荷的胶体有:金属氧化物、金属氢氧化物。例如Fe(OH)3、Al(OH)3等。
- 胶粒带负电荷的胶体有:非金属氧化物、金属硫化物、硅酸胶体、土壤胶体。
- 胶粒不带电的胶体有:淀粉胶体。
- 特殊的,AgI胶粒随着AgNO3和KI相对量不同,而带正电或负电。若KI过量,则AgI胶粒吸附较多I-而带负电;若AgNO3过量,则因吸附较多Ag+而带正电。
注意:胶体不带电,而胶粒可以带电。
Fe(OH)3胶体的制备:
操作步骤:将烧杯中的蒸馏水加热至沸腾,向沸水中滴加5~6滴饱和FeCl3溶液,继续煮沸至呈红褐色为止。
离子方程式:Fe3++3H2O=(加热)=Fe(OH)3(胶体)+3H+
点拨:(1)淀粉溶液、蛋白质溶液虽叫做溶液,但属于胶体。
(2)胶体可以是液体,也可以是固体、气体,如烟、云、雾、有色玻璃等。
混合物、纯净物、单质、化合物的概念:
(1)混合物:由两种或多种物质混合而成的物质。
(2)纯净物:由单一物质组成的物质 注:由同位素原子组成的物质是纯净物,如H2O和D2O混合后仍为纯净物。
(3)单质:由同种元素组成的纯净物,可分为金属单质和非金属单质。
(4)化合物:由不同种元素组成的纯净物。从不同角度可见化合物分为离子化合物,共价化合物,电解质和非电解质,有机化合物和物质化合物,酸碱盐和氧化物等。
混合物、纯净物、单质、化合物的概念:
(1)混合物:由两种或多种物质混合而成的物质
混合物没有固定的组成,一般没有固定的熔沸点
常见特殊名称的混合物:氨水、氯水、王水、天然水、硬水、软水、盐酸、浓硫酸、福尔马林、水玻璃、爆鸣气、水煤气、天然气、焦炉气、高炉煤气、石油气、裂解气、空气、合金、过磷酸钙、漂白粉、黑火药、铝热剂、水泥、铁触媒、玻璃、煤、石油、石油的各种馏分
注:由同素异形体组成的物质为混合物,如红磷和白磷。
(2)纯净物:由单一物质组成的物质
注:由同位素原子组成的物质是纯净物,如H2O和D2O混合后仍未纯净物。
(3)单质:由同种元素组成的纯净物,可分为金属单质和非金属单质
(1)金属单质:如Fe、Al、Cu等
(2)非金属单质:如Cl2、O2、S等
(4)化合物:由不同种元素组成的纯净物。从不同角度可见化合物分为离子化合物,共价化合物,电解质和非电解质,有机化合物和物质化合物,酸碱盐和氧化物等。
(5)酸、碱、盐、氧化物
①酸:电离理论认为电解质电离出阳离子全部是H+的化合物
常见的强酸:HClO4 H2SO4 HCl HNO3等
常见的弱酸:H2SO3 H3PO4 HF H2CO3 CH3COOH等
②碱:电离理论认为电解质电离出阴离子全部是OH-的化合物
常见强碱:NaOH KOH Ba(OH)2 Ca(OH)2等
常见弱碱:NH3·H2O Al(OH)3 Fe(OH)3等
③盐:电离时生成金属阳离子(NH4+)和酸根离子的化合物,可分为:正盐、酸式盐、碱式盐、复盐
a正盐:Na2SO4 Na2CO3 (NH4)2SO4 等
b酸式盐:NaHCO3 NaHSO4 NaH2PO4 Na2HPO4等
c碱式盐:Cu(OH)2CO3 Mg(OH)2CO3等
d复盐:KAl(SO4)2·H2O (NH4)2Fe(SO4)2·6H2O等
(6)氧化物:由两种元素组成,其中一种元素是氧的化合物
①按组成分:
金属氧化物:Na2O Al2O3 Fe3O4等
非金属氧化物:NO2 SO2 CO2等
②按性质分:
不成盐氧化物:CO NO等
酸性氧化物:CO2 SO2等
碱性氧化物:Na2O CuO等
两性氧化物:Al2O3 ZnO等
过氧化物:Na2O2 H2O2等
超氧化物:KO2等
特殊例子提醒:
(1)胆矾、明矾等结晶水合物是纯净物,不是物质和水的混合物。
(2)碱性氧化物一定是金属氧化物,但金属氧化物不一定是碱性氧化物(如Mn2O7为酸性氧化物、Al2O3为两性氧化物、Na2O2为过氧化物)。
(3)酸性氧化物不一定是非金属氧化物(如Mn2O7);非金属氧化物也不一定是酸性氧化物(如CO、NO)。
(4)酸性氧化物、碱性氧化物不一定都能与水反应生成相应的酸、碱(如SiO2、CuO)。
(5)与水反应生成酸的氧化物不一定是酸性氧化物(如NO2);与水反应生成碱的氧化物不一定是碱性氧化物(如Na2O2)。
无机物分类:

氧化物的分类:
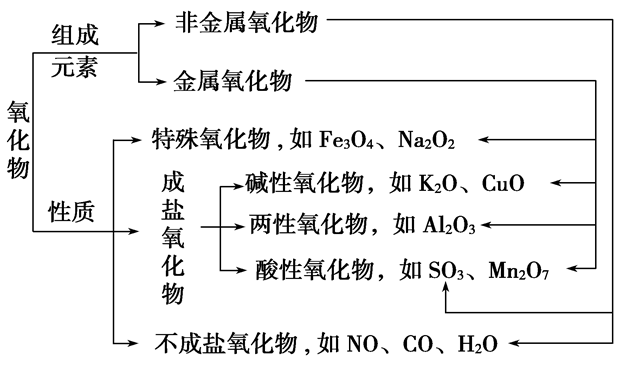
1.电解质和非电解质在水溶液里或熔融状态下能导电的化合物,叫做电解质。在水溶液里和熔融状态下都不导电的化合物,叫做非电解质。
2.电解质和非电解质的比较

说明(1)电解质、非电解质均是化合物。
(2)电解质导电必须有外界条件:水溶液或熔融状态。
(3)电解质是一定条件下本身电离而导电的化合物。CO2、SO2、SO3、NH3溶于水后也导电,但是与水反应生成的新物质电离而导电的,不是本身电离而导电的,故属于非电解质。
(4)电解质的强弱由物质的内部结构决定,与其溶解度无关。某些难溶于水的化合物,如BaSO4、AgCl,虽然溶解度很小,但溶解的部分是完全电离的,所以是强电解质。
(5)电解质不一定导电,非电解质一定不导电;导电的物质不一定是电解质,不导电的物质不一定是非电解质。
与“在下列物质种类中,前者包含后者的是[ ]A.单质 化合物B.电...”考查相似的试题有:
- 浊液区别于其它分散系最本质的特征是A.外观浑浊不清B.不稳定C.分散质粒子直径大于10-7cmD.不能发生丁达尔现象
- 朱自清先生在《荷塘月色》中写道:“薄薄的青雾浮起在荷塘里…… 月光是隔了树照过来的,高处丛生的灌木,落下参差的斑驳的黑影…...
- 下列关于胶体的说法正确的是A.胶体与其他分散系的本质区别是粒子直径的大小B.CuSO4溶液和Fe(OH)3胶体都能产生丁达尔效应C....
- “纳米材料”是粒子直径为1~100 nm(纳米)的材料,纳米碳就是其中的一种。若将纳米碳均匀地分散到蒸馏水中,所形成的物质[ ]①是...
- 下列关于分散系的说法,正确是( )A.稀硫酸不是分散系B.一种分散系里只有分散质和分散剂两种物质C.分散剂一定是液体D.按...
- Ⅰ.经常有人因误食亚硝酸钠(NaNO2)而中毒,原因是NaNO2像食盐一样既有咸味,又有很强毒性。已知亚硝酸钠能发生如下反应:2Na...
- 下列叙述正确的是A.NaHSO4溶于水,只破坏了离子键B.稀醋酸加水稀释,电离程度增大,溶液的酸性增强C.饱和石灰水中加入少量...
- 下列各组物质中,都是强电解质的是( )A.HBr、HCl、BaSO4B.NH4Cl、CH3COONa、H2SC.NaOH、Ca(OH)2、NH3•H2OD.HClO、NaF...
- 一化学兴趣小组在家中进行化学实验,按照图1连接好线路发现灯泡不亮,按照图2连接好线路发现灯泡亮,由此得出的结论正确的是[...
- 下列叙述正确的是( ) A.氯化钠在电流作用下电离成钠离子和氯离子B.溶于水后能电离出氢离子的化合物都是酸C.硫酸钡难溶于水...