本试题 “下列物质加入溴水,经振荡,不因发生化学反应而使溴水褪色的是[ ]A.Na2SB.NaOHC.甲苯D.裂化汽油” 主要考查您对氢氧化钠
金属硫化物
乙烯
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 氢氧化钠
- 金属硫化物
- 乙烯
氢氧化钠:
俗称火碱、烧碱、苛性钠
(1)与酸反应:NaOH+HCl==NaCl+H2O、2NaOH+H2SO4==Na2SO4+2H2O
(2)与非金属氧化物反应:2NaOH+CO2==Na2CO3+H2O、2NaOH+SO2==Na2SO3+H2O 、2NaOH+SO3==Na2SO4+H2O、2NaOH+SiO2==Na2SiO3+H2O
(3)与盐反应:2NaOH+CuCl2==Cu(OH)2+2NaCl
氢氧化钠的物理性质:
氢氧化钠为白色半透明,结晶状固体。其水溶液有涩味和滑腻感。密度:2.130g/cm3,熔点:318.4℃,沸点:1390℃。
溶解性:极易溶于水,溶解时放出大量的热。易溶于水醇、乙醇以及甘油。(氢氧化钠具有潮解性)
吸湿性:固碱吸湿性很强,露放在空气中,最后会完全溶解成溶液。
氢氧化钠的化学性质:
强碱性:
氢氧化钠溶液是常见的强碱,具有碱的通性:
①使酸碱指示剂变色:能使石蕊溶液变蓝,能使酚酞溶液变红;
②与酸发生中和反应生成盐和水;NaOH+HCl=NaCl+H2O
③与某些盐反应生成新盐和新碱;2NaOH+CuSO4=Cu(OH)2↓+Na2SO4
④与酸性氧化物反应生成盐和水。2NaOH+CO2====Na2CO3+H2O
腐蚀性:
氢氧化钠对玻璃制品有轻微的腐蚀性,两者会生成硅酸钠,使得玻璃仪器中的活塞黏着于仪器上。如果以玻璃容器长时间盛装热的氢氧化钠溶液,会造成玻璃容器损坏。
氢氧化钠溶液与CO2的反应规律:
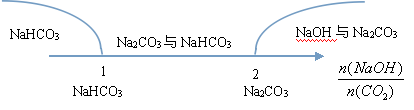
当二氧化碳少量时:2NaOH+CO2(少量)=Na2CO3+H2O
当二氧化碳过量时:Na2CO3+CO2(过量)+H2O=2NaHCO3
当二氧化碳与氢氧化钠的物质的量之比大于1小于2时,生成碳酸钠与碳酸氢钠的混合物。具体各产物的物质的量可根据钠元素守恒和碳元素守恒求算。
金属硫化物:
(1)碱金属硫化物(Li----Cs)全部易溶于水。(硫化铵在低温下0度左右易溶于水,但是在常温下会逐渐分解为氨和硫化氢)
(2)碱土金属硫化物(除了Be)(Mg----Ba)易溶于水,但是同时完全水解为氢氧化物和硫氢化物。
(3)铝,铍,铬的硫化物全部水解为硫化氢气体和氢氧化物沉淀。
(4)FeS,ZnS,MnS,NiS,CoS不溶于水但溶于稀盐酸。
(5)Bi2S3,SnS,SnS2,PbS,CdS,Bi2S5等不溶于水和稀盐酸,只溶于浓盐酸。
(6)CuS,Cu2S,Ag2S不溶于水,稀盐酸,浓盐酸,只溶于浓硝酸。
(7)Hg2S,HgS不溶于水,浓稀盐酸,浓硝酸,只溶于王水。
金属硫化物的溶解性归纳:
1.溶于水的有: 等,由于
等,由于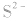 的水解,此类金属硫化物的水溶液显碱性:
的水解,此类金属硫化物的水溶液显碱性: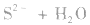
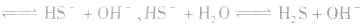 。
。
2.不溶于水但溶于稀盐酸的有:FeS、ZnS、MnS等。如: 。
。
3.不溶于稀盐酸但溶于浓盐酸的有:Cds、SnS、PbS等。
4.不溶于浓盐酸但溶于硝酸溶液的有:CuS等。
5.仅溶于王水的有:HgS等。
注意: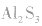 遇水后,
遇水后,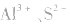 都水解,且相互促进,反应方程式为
都水解,且相互促进,反应方程式为
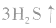 ,因而不能与水共存,只能在干态下制取。
,因而不能与水共存,只能在干态下制取。
硫的价态转化规律:
硫元素的价态比较多,常见的有-2、0、+4、+6 价,它们间的转化关系是:现将它们在化学反应中复杂的变化规律归结如下:
1.邻位价态转化规律
(1)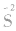 是硫元素的最低价态,只有还原性。它与氧化剂反应,其价态一般会升至相邻的价态(
是硫元素的最低价态,只有还原性。它与氧化剂反应,其价态一般会升至相邻的价态(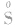 )。
)。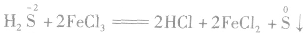
(2)S能发生自身氧化还原反应(即歧化反应),在反应时分别升至和降至与其相邻的价态。如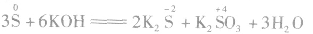
(3) 处于中间价态,既有氧化性又有还原性。与弱氧化剂作用时,被氧化成相邻的高价态;与弱还原剂作用时,被还原成相邻的低价态。如
处于中间价态,既有氧化性又有还原性。与弱氧化剂作用时,被氧化成相邻的高价态;与弱还原剂作用时,被还原成相邻的低价态。如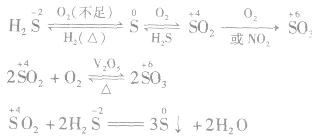
(4)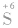 是硫元素的最高价态,只有氧化性。遇到还原剂时,其价态一般降至相邻的价态(
是硫元素的最高价态,只有氧化性。遇到还原剂时,其价态一般降至相邻的价态(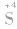 )。如
)。如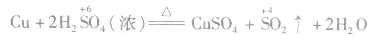
2.跳位转化规律
(1) 遇到强氧化剂时,价态会发生跳位转化。如
遇到强氧化剂时,价态会发生跳位转化。如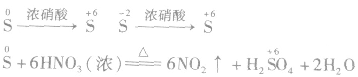
(2)反应条件改变时,硫的价态也会发生跳位转化。如
3.互不换位规律
(1) 发生氧化还原反应时,只能转化为中间价态,不可能互换位置。如
发生氧化还原反应时,只能转化为中间价态,不可能互换位置。如
(2)相邻价态的两物质问不发生氧化还原反应。 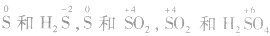 之间均不发生氧化还原反应。
之间均不发生氧化还原反应。
乙烯的结构和性质:
1.分子结构:
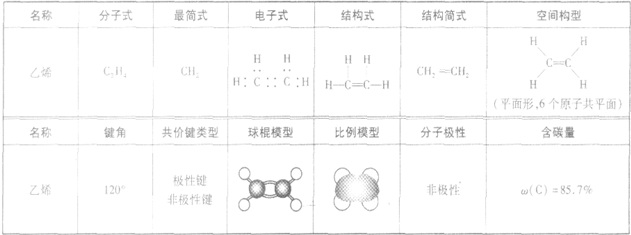
2.物理性质:
在通常状况下,乙烯是无色、稍有气味的气体,难溶于水,易溶于乙醇、乙醚等有机溶剂,密度(标准状况时为1.25g·L-1)比空气略小,因此实验室制取乙烯不用排空气法收集,而用排水法收集。
3.化学性质:
由于碳碳双键中的一个键易断裂,刚此乙烯的性质比较活泼,能发生加成、加聚反应,能使溴水和KMnO4溶液(酸性)褪色。
(1)乙烯易发生氧化反应
①乙烯的燃烧
乙烯在氧气或空气中易燃烧,完全燃烧生成CO2和H2O,反应的化学方程式为:
乙烯含碳量比较高,在一般情况下燃烧不是很充分,因此火焰明亮且伴有黑烟。
②乙烯的催化氧化

③乙烯能被酸性KMnO4溶液氧化
乙烯使酸性KMnO4溶液褪色的实质是乙烯被酸性KMnO4溶液氧化成二氧化碳和水。
(2)乙烯能发生加成反应
有机物分子中不饱和碳原子与其他原子(或原子团) 直接结合生成新的化合物的反应叫做加成反应。
乙烯使溴的四氯化碳溶液褪色的实质是乙烯与溴单质发生加成反应生成了1,2一二溴乙烷,反应的化学方程式为: 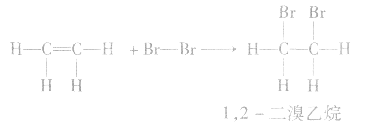
通常简写为
因此,可用溴水或溴的四氯化碳溶液鉴别乙烯和甲烷、乙烷等烷烃,也可用于除去甲烷中混有的乙烯。
(3)加聚反应在一定条件(温度、压强、催化剂)下,乙烯能发生加聚反应:
由相对分子质量小的化合物(单体)分子互相结合成相对分子质量很大的高分子的反应叫做聚合反应。由一种或多种不饱和化合物(单体)分子通过不饱和键互相加成而聚合成高分子化合物的反应叫做加成聚合反应,简称加聚反应。
乙烯的鉴别和除杂:
1.乙烯和其他物质的鉴别利用被鉴别物质性质的差异进行区分,要求操作简单、安全,现象明显,结论准确,以乙烷与乙烯的鉴别为例。操作:将两种气体分别通人酸性KMnO4溶液中。现象:一种气体使酸性KMnO4溶液褪色,一种气体不能使酸性KMnO4溶液褪色。结论:使酸性KMnO4溶液褪色者为乙烯,不能使酸性KMnO4溶液褪色者为乙烷.
2.除杂质乙烯除杂要求:将杂质除净,不能引入新杂质,小能对主要成分产生不利影响。如乙烷中混有乙烯,除杂的方法是用溴水洗气,乙烯与溴发生加成反应破除去,乙烷不反应逸出。
与“下列物质加入溴水,经振荡,不因发生化学反应而使溴水褪色的...”考查相似的试题有:
- 研究反应物的化学计量数与产物之间的关系时,使用类似数轴的方法可以收到直观形象的效果。下列表达不正确的是[ ]A.密闭容器...
- 将等物质的量的SO2气体和Cl2同时作用于湿润的红色布条.则布条的颜色A.变白B.不变C.先褪色后又复原D.变为无色
- 某同学利用下列装置进行浓硫酸和铜反应并验证二氧化硫的性质。按如图实验装置连接仪器和放置药品。加热浓硫酸约1分钟后撤去酒...
- 下列关于有机化合物的认识不正确的是( )A.油脂在空气中完全燃烧转化为水和二氧化碳B.蔗糖、麦芽糖的分子式都是C12H22O11,...
- (1)选择适当的试剂除去下列物质中的少量杂质(括号内为杂质):溴苯(溴):试剂______,反应方程式______;甲烷(乙烯):...
- 完成下列反应的化学方程式:(1)苯制备硝基苯______(2)丙烯的加聚______(3)将乙烯通入溴的四氯化碳溶液中______(4)甲...
- 下列关于有机化合物的说法正确的是A.甲烷和乙烯都可以使溴水褪色B.乙醇和乙酸都能发生取代反应C.酸性高锰酸钾可以氧化苯和...
- 乙烯是石油裂解的主要产物之一,将乙烯通入溴的四氯化碳溶液中,观察到的现象是______;其反应方程式为______.乙烯在一定条...
- (8分)写出下列相应的化学方程式(1)乙烯→乙醇: (2)丙烯→聚丙烯: (3)苯→溴苯: (4)苯→环己烷:
- 既可以用来鉴别乙稀和甲烷,又可用来除去甲烷中混有的乙烯的试剂或方法是( )A.溴水B.酸性高锰酸钾溶液C.在导管口处点燃D...