本试题 “Na2SO3固体在空气中久置容易变质。Ⅰ.请写出Na2SO3固体在空气中变质的化学方程式:_________________________Ⅱ.实验室中欲检验Na2SO3固体样品是否已经变质,...” 主要考查您对化学药品的变质
离子的检验
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 化学药品的变质
- 离子的检验
易变质的物质:
1. 由于吸水质量增加的物质:氢氧化钠固体,浓硫酸
2. 由于跟水反应质量增加的物质:氧化钙,氧化钠,硫酸铜
3. 由于和二氧化碳反应质量增加的物质:氢氧化钠,氢氧化钾,氢氧化钙
4. 由于挥发质量减少的物质:浓盐酸,浓硝酸,酒精,氨水
5. 由于风化质量减少的物质:碳酸钠晶体
氢氧化钠变质的知识归纳:
氢氧化钠变质主要考点包括:变质原因、检验变质的方法、检验变质的程度、 除去杂质得到就纯净的氢氧化钠。
1 、氢氧化钠变质的原因:
敞口放置, 与空气中的二氧化碳反应, 生成了碳酸钠。 2NaOH+CO 2 =Na 2 CO 3 +H 2 O
2 、检验氢氧化钠是否变质的方法: ( 分别滴加酸、碱、盐溶液,各为一种方法 )
①取少量样品于试管中, 滴加稀盐酸 ( 或者稀硫酸 ) , 如果产生气泡, 说明已变质。 Na 2 CO 3 +2HCl=2NaCl+H 2 O+CO 2 ↑
②取少量样品于试管中,滴加氢氧化钙溶液 ( 或者氢氧化钡溶液 ) ,如果产生白色 沉淀,说明已变质。 Na 2 CO 3 +Ca(OH) 2 =CaCO 3 ↓ +2NaOH
③取少量样品于试管中,滴加氯化钙溶液 ( 或者硝酸钙等其它可溶性钙盐、钡盐 溶液 ) Na 2 CO 3 +CaCl 2 =CaCO 3 ↓ +2NaCl
3 、检验氢氧化钠变质程度的方法:
取少量样品于试管中,滴加足量的 CaCl2 溶液,有白色沉淀生成;静置,像上层澄清液中滴加少量酚酞溶液,如果溶液变红色,说明溶液部分变质;如果溶液呈无色,说明氢氧化钠完全变质。
解释:碳酸钠溶液呈碱性,它的存在会影响到氢氧化钠的检验,所以在检验氢氧化钠前必须把碳酸钠除去。除去碳酸钠时不能用酸,因为酸会与氢氧化钠反应; 不能用碱,因为碱会与碳酸钠反应生成氢氧化钠,干扰原来氢氧化钠的检验。
4 、如何除去部分变质的氢氧化钠中的碳酸钠。 滴加适量氢氧化钙溶液至刚好无沉淀生成为止,然后过滤,就得到氢氧化钠溶液,再蒸发,就得到氢氧化钠固体。 Na 2 CO 3 +Ca(OH) 2 =CaCO 3 ↓ +2NaOH
除杂方法:除杂时为了不引入新杂质,如果除去阴离子,所选择试剂的阴离子 与主题物质一致。
氧化钙和氢氧化钙的变质:
(1)变质的原因
氧化钙在空气中敞口放置会与空气中的水蒸气反应生成氢氧化钙 CaO+H 2 O===Ca(OH) 2 , 氢氧化钙继续与空气中的二氧化碳反应生成碳酸钙。 Ca(OH) 2 +CO 2 ====CaCO 3 ↓+H 2 O
(2)检验变质后物质存在的方法:
氧化钙:
取少量变质后的固体放入烧杯中,加入水充分溶解,用手摸烧杯外壁有灼热感。
氢氧化钙:
(1)取变质后物质溶于水,向其中通入二氧化碳气体,有白色沉淀生成。
(2)取变质后物质溶于水,向其中滴加碳酸钠溶液,有白色沉淀生成。 碳酸钙:取少量变质后固体,向其中滴加稀盐酸,有气泡冒出。 CaCO3 +2HCl===CaCl2 +H2O+CO2 ↑
【特殊强调】:有氧化钙存在的情况下,初中阶段检验不出氢氧化钙的存在。因为氧化钙溶于水后会生成氢氧化钙,会干扰原来氢氧化钙的检验。
其它常见物质变质的知识小结:
NaOH在空气中变质:2NaOH+CO2==Na2CO3+H2O
检验: 取样滴加稀 HCl,若有气泡产生,则已经变质 (Na 2 CO 3 +2HCl===2NaCl+H 2 O+CO 2 ↑ )
消石灰 [Ca(OH)2] 放在空气中变质: Ca(OH) 2 +CO 2 ====CaCO 3 ↓ +H 2 O
检验: 取样滴加稀 HCl,若有气泡产生,则已经变质 (CaCO 3 +2HCl===CaCl 2 +H 2 O+CO 2 ↑ )
生石灰 (CaO) 暴露在空气中变质: CaO+H 2 O===Ca(OH) 2
检验: 取样用试管加热,若试管内壁有小水珠产生,则已变质 [Ca(OH) 2 = 加热 =CaO+H 2 O]
铁生锈:4Fe+3O 2 ===2Fe2O3
检验:观察颜色 , 若有红色粉末在表面, 则已变质
铜生锈:2Cu+O 2 +CO 2 +H 2 O===Cu 2 (OH) 2 CO 3
检验:观察颜色 , 若有绿色粉末在表面,则已变质。
离子的检验:
(1)焰色反应:Na+:黄色;K+:紫色(透过蓝色钴玻璃观察);Ca2+:砖红色;
(2)H+:H+酸性。遇紫色石蕊试液变红,遇湿润蓝色石蕊试纸变红;
(3)NH4+:在试液中加强碱(NaOH)加热,产生使湿润红色石蕊试纸变蓝的气体;NH4++OH-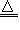 NH3↑+H2O;NH3+H2O
NH3↑+H2O;NH3+H2O
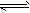 NH3?H2O
NH3?H2O NH4++OH-
NH4++OH-
(4)Fe3+:①通KSCN或NH4SCN溶液呈血红色:Fe3++SCN-==[Fe(SCN)]2+;②通NaOH溶液红褐色沉淀:Fe3++3OH-==
Fe(OH)3↓
(5)Fe2+:①遇NaOH溶液生成白色沉淀在空气中迅速转化成灰绿色最后变成红褐色沉淀:Fe3++2OH-=Fe(OH)2↓;
4Fe(OH)2+O2+2H2O==4Fe(OH)3;
②试液中加KSCN少量无明显变化再加氯水出现血红色: 2Fe2++Cl2==2Fe3++2Cl-;Fe3++SCN-==[Fe(SCN)]2+
(6)Mg2+:遇NaOH溶液有白色沉淀生成,NaOH过量沉淀不溶解:Mg2++2OH-==Mg(OH)2↓,但该沉淀能溶于NH4Cl溶液;
(7)Al3+:遇NaOH溶液(适量)有白色沉淀生成,NaOH溶液过量沉淀溶解:Al3++3OH-==Al(OH)3↓;Al(OH)3+OH-==
AlO2-+2H2O
(8)Cu2+:遇NaOH溶液有蓝色沉淀生成,加强热变黑色沉淀:Cu2++2OH-==Cu(OH)2↓;Cu(OH)2 CuO+H2O
CuO+H2O
(9)Ba2+:遇稀H2SO4或硫酸盐溶液有白色沉淀生成,加稀HNO3沉淀不溶解:Ba2++SO42-==BaSO4↓
(10)Ag+: ①加NaOH溶液生成白色沉淀,此沉淀迅速转变为棕色沉淀溶于氨水Ag++OH-==AgOH↓;2AgOH==Ag2O+H2O;AgOH+2NH3?H2O==[Ag(NO3)2]OH+2H2O
②加稀HCl或可溶性氧化物溶液再加稀HNO3生成白色沉淀:Ag++Cl-==AgCl↓
(11)OH-:OH-碱性:①遇紫色石蕊试液变蓝;②遇酚酞试液变红;③遇湿润红色石蕊试纸变蓝;
(12)Cl-:遇AgNO3溶液有白色沉淀生成,加稀HNO3沉淀不溶解:Ag++Cl-=AgCl↓
(13)Br-:加AgNO3溶液有浅黄色沉淀生成,加稀HNO3沉淀不溶解:Ag++Br-=AgBr↓
(14)I-: ①加AgNO3溶液有黄色沉淀生成,加稀HNO3沉淀不溶解:Ag++I-=AgI↓;②加少量新制氯水后再加淀粉溶液显蓝色:2I-+Cl2=I2+2Cl-;I2遇淀粉变蓝
(15)S2-:①加强酸(非强氧化性)生成无色臭鸡蛋气味气体:S2-+2H+=H2S↑;②遇Pb(NO3)2或(CH3COO)2Pb试液生成黑色沉淀,遇CuSO4试液产生黑色沉淀:Pb2++S2-=PbS↓;Cu2++S2-=CuS↓
(16)SO42-:加可溶性钡盐[BaCl2或Ba(NO3)2]溶液有白色沉淀生成后再加稀HCl或稀HNO3沉淀不溶解:Ba2++SO42-=BaSO4↓
(17)SO32-:加强酸(H2SO4或HCl)把产生气体通入品红溶液中,品红溶液褪色:SO32-+2H+=H2O+SO2↑ SO2使品红溶液褪色
(18)CO32-:加稀HCl产生气体通入澄清石灰水,石灰水变浑浊:CO32-+2H+=H2O+CO2↑;CO2+Ca(OH)2=CaCO3↓+H2O
(19)HCO3-:取含HCO3-盐溶液煮沸,放出无色无味、使澄清石灰水变浑浊的气体;或向HCO3-溶液里加入稀MgSO4溶液,无现象,加热煮沸有白色沉淀MgCO3生成,同时放出CO2气体。
(20)NO3-:浓缩试液加稀硫酸和铜片加热有红棕色气体产生,溶液变成蓝色:
Cu+4H++2NO3-=Cu2++2NO2↑+2H2O
(21)PO43-:加AgNO3溶液产生黄色沉淀,再加稀HNO3沉淀溶解:3Ag++PO43-=Ag3PO4↓;Ag3PO4溶于稀HNO3酸。
(1)焰色反应:Na+:黄色;K+:紫色(透过蓝色钴玻璃观察);Ca2+:砖红色;
(2)H+:H+酸性。遇紫色石蕊试液变红,遇湿润蓝色石蕊试纸变红;
(3)NH4+:在试液中加强碱(NaOH)加热,产生使湿润红色石蕊试纸变蓝的气体;NH4++OH-
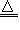 NH3↑+H2O;NH3+H2O
NH3↑+H2O;NH3+H2O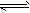 NH3?H2O
NH3?H2O NH4++OH-
NH4++OH- (4)Fe3+:①通KSCN或NH4SCN溶液呈血红色:Fe3++SCN-==[Fe(SCN)]2+;②通NaOH溶液红褐色沉淀:Fe3++3OH-==
Fe(OH)3↓
(5)Fe2+:①遇NaOH溶液生成白色沉淀在空气中迅速转化成灰绿色最后变成红褐色沉淀:Fe3++2OH-=Fe(OH)2↓;
4Fe(OH)2+O2+2H2O==4Fe(OH)3;
②试液中加KSCN少量无明显变化再加氯水出现血红色: 2Fe2++Cl2==2Fe3++2Cl-;Fe3++SCN-==[Fe(SCN)]2+
(6)Mg2+:遇NaOH溶液有白色沉淀生成,NaOH过量沉淀不溶解:Mg2++2OH-==Mg(OH)2↓,但该沉淀能溶于NH4Cl溶液;
(7)Al3+:遇NaOH溶液(适量)有白色沉淀生成,NaOH溶液过量沉淀溶解:Al3++3OH-==Al(OH)3↓;Al(OH)3+OH-==
AlO2-+2H2O
(8)Cu2+:遇NaOH溶液有蓝色沉淀生成,加强热变黑色沉淀:Cu2++2OH-==Cu(OH)2↓;Cu(OH)2
 CuO+H2O
CuO+H2O (9)Ba2+:遇稀H2SO4或硫酸盐溶液有白色沉淀生成,加稀HNO3沉淀不溶解:Ba2++SO42-==BaSO4↓
(10)Ag+: ①加NaOH溶液生成白色沉淀,此沉淀迅速转变为棕色沉淀溶于氨水Ag++OH-==AgOH↓;2AgOH==Ag2O+H2O;AgOH+2NH3?H2O==[Ag(NO3)2]OH+2H2O
②加稀HCl或可溶性氧化物溶液再加稀HNO3生成白色沉淀:Ag++Cl-==AgCl↓
(11)OH-:OH-碱性:①遇紫色石蕊试液变蓝;②遇酚酞试液变红;③遇湿润红色石蕊试纸变蓝;
(12)Cl-:遇AgNO3溶液有白色沉淀生成,加稀HNO3沉淀不溶解:Ag++Cl-=AgCl↓
(13)Br-:加AgNO3溶液有浅黄色沉淀生成,加稀HNO3沉淀不溶解:Ag++Br-=AgBr↓
(14)I-: ①加AgNO3溶液有黄色沉淀生成,加稀HNO3沉淀不溶解:Ag++I-=AgI↓;②加少量新制氯水后再加淀粉溶液显蓝色:2I-+Cl2=I2+2Cl-;I2遇淀粉变蓝
(15)S2-:①加强酸(非强氧化性)生成无色臭鸡蛋气味气体:S2-+2H+=H2S↑;②遇Pb(NO3)2或(CH3COO)2Pb试液生成黑色沉淀,遇CuSO4试液产生黑色沉淀:Pb2++S2-=PbS↓;Cu2++S2-=CuS↓
(16)SO42-:加可溶性钡盐[BaCl2或Ba(NO3)2]溶液有白色沉淀生成后再加稀HCl或稀HNO3沉淀不溶解:Ba2++SO42-=BaSO4↓
(17)SO32-:加强酸(H2SO4或HCl)把产生气体通入品红溶液中,品红溶液褪色:SO32-+2H+=H2O+SO2↑ SO2使品红溶液褪色
(18)CO32-:加稀HCl产生气体通入澄清石灰水,石灰水变浑浊:CO32-+2H+=H2O+CO2↑;CO2+Ca(OH)2=CaCO3↓+H2O
(19)HCO3-:取含HCO3-盐溶液煮沸,放出无色无味、使澄清石灰水变浑浊的气体;或向HCO3-溶液里加入稀MgSO4溶液,无现象,加热煮沸有白色沉淀MgCO3生成,同时放出CO2气体。
(20)NO3-:浓缩试液加稀硫酸和铜片加热有红棕色气体产生,溶液变成蓝色:
Cu+4H++2NO3-=Cu2++2NO2↑+2H2O
(21)PO43-:加AgNO3溶液产生黄色沉淀,再加稀HNO3沉淀溶解:3Ag++PO43-=Ag3PO4↓;Ag3PO4溶于稀HNO3酸。
发现相似题
与“Na2SO3固体在空气中久置容易变质。Ⅰ.请写出Na2SO3固体在空气...”考查相似的试题有:
- 下列实验操作或装置符合实验要求的是A.量取15.00 mLNaOH溶液B.定容C.电解食盐水制Cl2、H2D.高温煅烧石灰石
- 用下列实验装置进行相应的实验,能达到实验目的的是A.图Ⅰ用于实验室制氨气并收集干燥的氨气B.图Ⅱ用于除去CO2中含有的少量HC...
- 题下列关于实验安全的叙述中错误的是( )A.使用、制备有毒气体应在通风橱中进行,应有完全吸收处理装置B.酒精及其它易燃物...
- 在实验室中,对下列事故或药品的处理不正确的是( )A.有大量的氯气泄漏时,用氢氧化钠溶液浸湿软布蒙面,并迅速离开现场B....
- 学生设计了如图的方法对A盐进行鉴定:由此分析,下列结论中,正确的是 ( )A.A中一定有Fe3+B.C中一定有Cu2+C.B一定为AgBr...
- 下列说法不正确的是A.无论乙烯与丙烯酸以何种比例混合,只要二者总物质的量是个定值,完全燃烧时所消耗的氧气也一定是个定值...
- 下列仪器常用于物质分离的是( )①漏斗 ②试管 ③蒸馏烧瓶 ④天平 ⑤分液漏斗 ⑥研钵A.①③④B.①②⑥C.①③⑤D.①③⑥
- 欲检验只含一种阴离子的溶液中是否含有SO42-,下列操作中正确的是( )A.先加入稀硝酸,没有产生沉淀,然后再加硝酸钡,产生...
- [实验化学]3,5-二甲氧基苯酚是重要的有机合成中间体,可用于天然物质白柠檬素的合成。一种以间苯三酚为原料的合成反应如下:...
- 下列除杂质选用试剂和主要操作都正确的是 物质杂质试剂主要操作ASiO2Fe2O3盐酸过滤BNaHCO3NH4Cl—加热C铁粉铜粉稀硫酸过滤D甲...