本试题 “下列说法不正确的是[ ]A.能够发生化学反应的碰撞是有效碰撞B.升高温度会加快化学反应速率,其原因是增加了活化分子的百分数C.化学平衡发生移动,平衡常数...” 主要考查您对活化分子、活化能、有效碰撞
化学平衡常数
中和热的测定
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 活化分子、活化能、有效碰撞
- 化学平衡常数
- 中和热的测定
有效碰撞与活化分子:
1.化学反应过程就是反应物分子分裂成原子,原子重新组合成生成物分子的过程,也就是反应物分子中化学键断裂、生成物分子中化学键形成的过程。
2.旧键的断裂和新键的形成都是通过反应物分子 (或离子)的相互碰撞来实现的。反应物分子(或离子)问的碰撞是化学反应发生的先决条件,但并不是反应物分子的每次碰撞都能发生化学反应。
3.能够发生化学反应的分子碰撞叫做有效碰撞,把能够发生有效碰撞的分子叫做活化分子。活化分子具有比普通分子(非活化分子)更高的能量。活化分子在碰撞后有可能使原子问的化学键断裂,从而导致化学反应的发生。但并不是活化分子的每次碰撞都能引起化学反应。
4.分子间的自由碰撞必然会有不同的碰撞取向。研究发现,有效的分子碰撞,分子除了要有足够的能量以外,还要有合适的碰撞取向。从分子能量的方面来看,活化分子具备发生有效碰撞的条件。从分子碰撞取向的方向来看,活化分子的某次碰撞并不一定能引发化学反应。若活化分子碰撞取向合适,才能发生化学反应;若活化分子碰撞取向不合适,则化学反应不能发生。也就是说,只有活化分子以合适的取向发生碰撞,才能使分子内的化学键断裂,从而引发化学反应。或者说,具有较高能量的活化分子按照合适的取向所发生的有效碰撞才能引发化学反应。
5.为了把“有效碰撞”概念具体化,人们把能够发生有效碰撞的分子叫做活化分子,同时把活化分子所多出来的那部分能量叫做活化能,因此活化能是活化分子平均能量与普通反应物分子平均能量的差值。
6.活化能相当于化学反应的“门槛”,对于同一化学反应,其活化能越低,反应速率越快。催化剂就是通过参与反应,改变反应历程,降低反应的活化能来提高反应速率的。
1.化学反应过程就是反应物分子分裂成原子,原子重新组合成生成物分子的过程,也就是反应物分子中化学键断裂、生成物分子中化学键形成的过程。
2.旧键的断裂和新键的形成都是通过反应物分子 (或离子)的相互碰撞来实现的。反应物分子(或离子)问的碰撞是化学反应发生的先决条件,但并不是反应物分子的每次碰撞都能发生化学反应。
3.能够发生化学反应的分子碰撞叫做有效碰撞,把能够发生有效碰撞的分子叫做活化分子。活化分子具有比普通分子(非活化分子)更高的能量。活化分子在碰撞后有可能使原子问的化学键断裂,从而导致化学反应的发生。但并不是活化分子的每次碰撞都能引起化学反应。
4.分子间的自由碰撞必然会有不同的碰撞取向。研究发现,有效的分子碰撞,分子除了要有足够的能量以外,还要有合适的碰撞取向。从分子能量的方面来看,活化分子具备发生有效碰撞的条件。从分子碰撞取向的方向来看,活化分子的某次碰撞并不一定能引发化学反应。若活化分子碰撞取向合适,才能发生化学反应;若活化分子碰撞取向不合适,则化学反应不能发生。也就是说,只有活化分子以合适的取向发生碰撞,才能使分子内的化学键断裂,从而引发化学反应。或者说,具有较高能量的活化分子按照合适的取向所发生的有效碰撞才能引发化学反应。
5.为了把“有效碰撞”概念具体化,人们把能够发生有效碰撞的分子叫做活化分子,同时把活化分子所多出来的那部分能量叫做活化能,因此活化能是活化分子平均能量与普通反应物分子平均能量的差值。
6.活化能相当于化学反应的“门槛”,对于同一化学反应,其活化能越低,反应速率越快。催化剂就是通过参与反应,改变反应历程,降低反应的活化能来提高反应速率的。
定义:
在一定温度下,可逆反应无论从正反应开始,还是从逆反应开始,也不管反应物起始浓度大小,最后都达到平衡,这时各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值是个常数,用K表示,这个常数叫化学平衡常数。
化学表平衡达式:
对于可逆反应mA(g)+nB(g)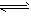 pC(g)+qD(g)来说,化学平衡表达式:
pC(g)+qD(g)来说,化学平衡表达式: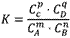
化学平衡常数的意义:
①表示该反应在一定温度下,达到平衡时进行的程度,K值越大,正反应进行的越彻底,对反应物而言转化率越高。
②某一温度下的K′与K比较能够判断反应进行的方向
K′>K,反应正向进行;K′<K,反应逆向进行;K′=K,反应处于平衡状态
(3)化学平衡常数与浓度、压强、催化剂无关,与温度有关,在使用时必须指明温度。
(4)在计算平衡常数时,必须是平衡状态时的浓度。
(5)对于固体或纯液体而言,其浓度为定值,可以不列入其中。
(6)化学平衡常数是指某一具体反应的平衡常数,若反应方向改变,则平衡常数改变,且互为倒数关系。如:在一定温度下,
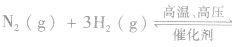


化学平衡常数的应用:
1.K值越大,说明平衡体系中生成物所占的比例越大,正向反应进行的程度越大,反应物转化率越大;反之,正向反应进行的程度就越小,反应物转化率就越小,即平衡常数的大小可以衡量反应进行的程度,判断平衡移动的方向,进行平衡的相关计算。
2.若用浓度商(任意状态的生成物浓度幂之积与反应物浓度幂之积的比值,符号为Qc)与K比较,可判断可逆反应是否达到平衡状态和反应进行的方向。
3.利用K值可判断反应的热效应若升高温度,K值增大,则正反应为吸热反应;若升高温度,K值减小,则正反应为放热反应。
4.计算转化率及浓度依据起始浓度(或平衡浓度)和平衡常数可以计算平衡浓度(或起始浓度),从而计算反应物的转化率。
在一定温度下,可逆反应无论从正反应开始,还是从逆反应开始,也不管反应物起始浓度大小,最后都达到平衡,这时各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值是个常数,用K表示,这个常数叫化学平衡常数。
化学表平衡达式:
对于可逆反应mA(g)+nB(g)
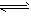 pC(g)+qD(g)来说,化学平衡表达式:
pC(g)+qD(g)来说,化学平衡表达式: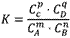
化学平衡常数的意义:
①表示该反应在一定温度下,达到平衡时进行的程度,K值越大,正反应进行的越彻底,对反应物而言转化率越高。
②某一温度下的K′与K比较能够判断反应进行的方向
K′>K,反应正向进行;K′<K,反应逆向进行;K′=K,反应处于平衡状态
(3)化学平衡常数与浓度、压强、催化剂无关,与温度有关,在使用时必须指明温度。
(4)在计算平衡常数时,必须是平衡状态时的浓度。
(5)对于固体或纯液体而言,其浓度为定值,可以不列入其中。
(6)化学平衡常数是指某一具体反应的平衡常数,若反应方向改变,则平衡常数改变,且互为倒数关系。如:在一定温度下,
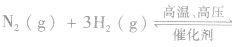


化学平衡常数的应用:
1.K值越大,说明平衡体系中生成物所占的比例越大,正向反应进行的程度越大,反应物转化率越大;反之,正向反应进行的程度就越小,反应物转化率就越小,即平衡常数的大小可以衡量反应进行的程度,判断平衡移动的方向,进行平衡的相关计算。
2.若用浓度商(任意状态的生成物浓度幂之积与反应物浓度幂之积的比值,符号为Qc)与K比较,可判断可逆反应是否达到平衡状态和反应进行的方向。
3.利用K值可判断反应的热效应若升高温度,K值增大,则正反应为吸热反应;若升高温度,K值减小,则正反应为放热反应。
4.计算转化率及浓度依据起始浓度(或平衡浓度)和平衡常数可以计算平衡浓度(或起始浓度),从而计算反应物的转化率。
中和热测定:
(1)目的:①用量热法测定HCl与NaOH的中和热。②了解化学标定法,并掌握其操作。
(2)原理:在298K、溶液足够稀的情况下,1molOH-与1molH+中和,可放出57.3.kJ的热量。即:H+(aq)+OH-(aq) =H2O(aq) △H=-57.3kJ/mol
(3)仪器和实验:大烧杯(500 mL)、小烧杯(100 mL)、温度计、量筒(50mL)两个、泡沫塑料或纸条、泡沫塑料板或硬纸板(中心有两个小孔)、环形玻璃搅拌棒。0.50 mol/L 盐酸、0.55 mol/L NaOH溶液。
(4)步骤:
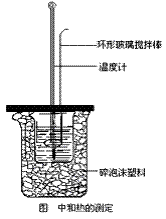
①在大烧杯底垫泡沫塑料(或纸条),使放入的小烧杯杯口与大烧杯杯口相平。然后再在大、小烧杯之间填满碎泡沫塑料(或纸条),大烧杯上用泡沫塑料板(或硬纸板)作盖板,在板中间开两个小孔,正好使温度计和环形玻璃搅拌棒通过,以达到保温、隔热、减少实验过程中热量损失的目的,如图所示。该实验也可在保温杯中进行。
②用一个量筒量取50mL0.50mol/L盐酸,倒入小烧杯中,并用温度计测量盐酸的温度,记入下表。然后把温度计上的酸用水冲洗干净。
③用另一个量筒量取50mL 0.55 mol/L NaOH溶液,并用温度计测量NaOH溶液的温度,记入下表。
④把温度计和环形玻璃搅拌棒放入小烧杯的盐酸中,并把量筒中的NaOH溶液一次倒入小烧杯(注意不要洒到外面)。用环形玻璃搅拌棒轻轻搅动溶液,并准确读取混合溶液的最高温度,记为终止温度,记入下表。
⑤重复实验两次,取测量所得数据的平均值作为计算依据。
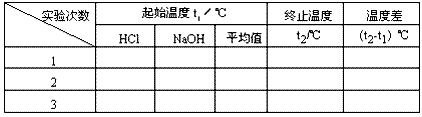
⑥根据实验数据计算中和热。
(1)目的:①用量热法测定HCl与NaOH的中和热。②了解化学标定法,并掌握其操作。
(2)原理:在298K、溶液足够稀的情况下,1molOH-与1molH+中和,可放出57.3.kJ的热量。即:H+(aq)+OH-(aq) =H2O(aq) △H=-57.3kJ/mol
(3)仪器和实验:大烧杯(500 mL)、小烧杯(100 mL)、温度计、量筒(50mL)两个、泡沫塑料或纸条、泡沫塑料板或硬纸板(中心有两个小孔)、环形玻璃搅拌棒。0.50 mol/L 盐酸、0.55 mol/L NaOH溶液。
(4)步骤:
①在大烧杯底垫泡沫塑料(或纸条),使放入的小烧杯杯口与大烧杯杯口相平。然后再在大、小烧杯之间填满碎泡沫塑料(或纸条),大烧杯上用泡沫塑料板(或硬纸板)作盖板,在板中间开两个小孔,正好使温度计和环形玻璃搅拌棒通过,以达到保温、隔热、减少实验过程中热量损失的目的,如图所示。该实验也可在保温杯中进行。

②用一个量筒量取50mL0.50mol/L盐酸,倒入小烧杯中,并用温度计测量盐酸的温度,记入下表。然后把温度计上的酸用水冲洗干净。
③用另一个量筒量取50mL 0.55 mol/L NaOH溶液,并用温度计测量NaOH溶液的温度,记入下表。
④把温度计和环形玻璃搅拌棒放入小烧杯的盐酸中,并把量筒中的NaOH溶液一次倒入小烧杯(注意不要洒到外面)。用环形玻璃搅拌棒轻轻搅动溶液,并准确读取混合溶液的最高温度,记为终止温度,记入下表。
⑤重复实验两次,取测量所得数据的平均值作为计算依据。

⑥根据实验数据计算中和热。
发现相似题
与“下列说法不正确的是[ ]A.能够发生化学反应的碰撞是有效碰撞B...”考查相似的试题有:
- I2在KI溶液中存在下列平衡:I2(aq) + I-(aq) I3一(aq)。测得不同温度下该反应的平衡常数值如下表:t/℃515253550K110084168053...
- 下列措施或事实能用勒沙特列原理解释的是 A.在合成氨(正反应是放热)的反应中,升温有利于氨的合成B.钢铁在潮湿的空气中生...
- (12分)在不同温度下,反应CO2(g)+H2(g)CO(g)+H2O(g)的平衡常数K如下表:温度/℃70080085010001200平衡常数K2.61.710.90.6...
- 下列反应体系中,不属于可逆反应的是A.Cl2溶解于水B.氨气溶解于水C.工业合成氨D.水电解生成H2和O2与H2在O2中燃烧生成H2O
- 可逆反应aA(g)+bB(s)cC(g)+dD(g)在反应过程中,其他条件不变,C的物质的量分数和T或P关系如图所示,下列叙述中正确的...
- 在密闭容器中,对于可逆反应2A+3 B 2C(g) 平衡时C的体积分数与温度和压强的关系如图所示,下列说法不正确的是
- (14分) 某化学兴趣小组,专门研究了氧族元素及其某些化合物的部分性质。查得的资料如下:①常温下,硒(Se)和碲(Te)为固体,H2S...
- (6分)在通常状况下,NO2与SO2很容易发生反应生成NO和SO3,该反应为不可逆反应。现将NO和SO2的混合气体通入容积为100 mL的容...
- (7分)为了除去工业废气中的SO2,将“SO2转化为(NH4)2SO4”的资料摘录如下:“一个典型的实例:初步处理后的废气中含0.2%的S...
- (6分)在溶液中,反应A+2BC分别在三种不同实验条件下进行,它们的起始浓度均为c(A)="0.100" kJ·mol-1、c(B)="0.200" kJ·mol-...