本试题 “已知16.0 g CH4完全燃烧生成CO2和液态水时,放出890kJ热量。现有CH4和CO混合气体共0.75 mol,完全燃烧后生成CO2和18 g液态水,并放出516 kJ热量。求:(1)混...” 主要考查您对燃烧热
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 燃烧热
燃烧热:
在101kPa时,1mol纯物质完全燃烧生成稳定的氧化物时所放出的热量,叫做该物质的燃烧热。单位为kJ/mol
注意事项:
(1)规定是在101kPa 下测出的热量。书中提供的燃烧热数据都是在25℃、101kPa下测定出来的
(2)规定可燃物的物质的量为1mol(这样才有可比性)。因此,表示可燃物的燃烧热的热化学方程式中,可燃物的化学计量数为1,其他物质的化学计量数常出现分数
(3)规定生成稳定的氧化物,例如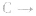
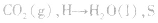
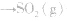 等
等
(4)叙述燃烧热时、不用“+”“-”,在热化学方程式中用△H表示时取“-”
在101kPa时,1mol纯物质完全燃烧生成稳定的氧化物时所放出的热量,叫做该物质的燃烧热。单位为kJ/mol
燃烧热和中和热的异同:
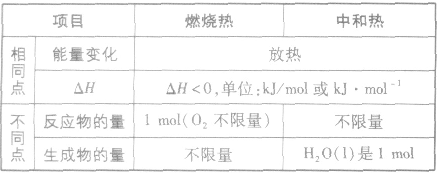
注意事项:
(1)规定是在101kPa 下测出的热量。书中提供的燃烧热数据都是在25℃、101kPa下测定出来的
(2)规定可燃物的物质的量为1mol(这样才有可比性)。因此,表示可燃物的燃烧热的热化学方程式中,可燃物的化学计量数为1,其他物质的化学计量数常出现分数
(3)规定生成稳定的氧化物,例如
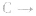
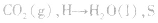
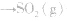 等
等 (4)叙述燃烧热时、不用“+”“-”,在热化学方程式中用△H表示时取“-”
发现相似题
与“已知16.0 g CH4完全燃烧生成CO2和液态水时,放出890kJ热量。...”考查相似的试题有:
- 下图是煤化工产业链的一部分,试运用所学知识,解决下列问题:I.已知该产业链中某反应的平衡表常数达式为:K=,它所对应反...
- 1,3-丁二烯和2-丁炔分别与氢气反应的热化学方程式如下:CH2=CH-CH=CH2(g)+2H2(g)→CH3CH2CH2CH3(g)+236.6kJCH3-C≡C-CH3...
- 硫酸盐主要来自地层矿物质,多以硫酸钙、硫酸镁的形态存在。(1)已知:①Na2SO4(s)=Na2S(s)+2O2(g) ; ΔH1=" +1011.0" kJ · m...
- 已知:2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-12H2O(g)=2H2(g)+O2(g) ΔH=+483.6 kJ·mol-1现有1g液态H2O,蒸发时吸收...
- 氮是一种地球上含量丰富的元素,氮及其化合物的研究在生产、生活中有着重要意义。(1)下图是1 mol NO2和1 mol CO反应生成CO2...
- 含有NaOH 20.0 g的稀溶液与足量的稀盐酸反应,放出28.7 kJ的热量。能正确表示该反应中和热的热化学方程式是 ( )A.NaOH +HC...
- (6分)依据下列事实,写出下列反应的热化学方程式。(1)在25℃、101kPa下,1g甲醇(CH3OH)燃烧生成CO2和液态水时放热22.68k...
- 已知16g硫变成硫蒸汽需要吸收akJ的热量,而2mol硫蒸汽完全燃烧会放出bkJ的热量,则下列热化学方程式正确的是A.S(s)+ O2(g)=...
- A.C+H2OCO+H2;△H=+10.94kJ/molB.C(s)+H2O(g)CO(g)+H2(g); △H=+10.94kJ/molC.C(s)+H2O(g)CO(g)+H2(g); △H=-131.3kJ/molD...
- 电离平衡常数(用Ka表示)的大小可以判断电解质的相对强弱。25℃时,有关物质的电离平衡常数如下表所示:化学式HFH2CO3HClO电离...