本试题 “对水的处理包括水的净化、软化、杀菌、消毒、去离子、蒸馏等.其中常见的杀菌消毒剂包括氯气、臭氧、漂粉精等.2008年北京奥运会曾拟用臭氧、活性炭对游泳池...” 主要考查您对氯气
臭氧
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 氯气
- 臭氧
氯气:
①化学式:Cl2
②氯元素在周期表中的位置:第三周期ⅦA族
③氯原子的电子式: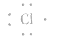
④氯的原子结构示意图: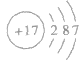
⑤氯原子的外围电子排布式:
⑥化学键类型:非极性共价键
⑦氯分子的电子式:
⑧氯分子的结构式:
氯气的物理性质和化学性质:
(1)物理性质:黄绿色,有刺激性气味,有毒,密度比空气大,能溶于水(1:2)。
(2)化学性质:氯气(Cl2)是双原子分子,原子的最外层有七个电子,是典型的非金属元素,单质是强氧化剂。
①氯气与金属反应: 2Na+Cl2
 2NaCl(反应剧烈,产生大量白烟) 2Fe+3Cl2
2NaCl(反应剧烈,产生大量白烟) 2Fe+3Cl2 2FeCl3(反应剧烈,产生大量棕褐色烟,溶于水成黄色溶液) Cu+Cl2
2FeCl3(反应剧烈,产生大量棕褐色烟,溶于水成黄色溶液) Cu+Cl2 CuCl2(反应剧烈,产生大量棕色的烟,溶于水成蓝色或绿色溶液)氯气能与绝大数金属都能发生反应,表明氯气是一种活泼的非金属单质。
CuCl2(反应剧烈,产生大量棕色的烟,溶于水成蓝色或绿色溶液)氯气能与绝大数金属都能发生反应,表明氯气是一种活泼的非金属单质。 ②与非金属的反应 H2+Cl2
 2HCl(纯净的氢气在氯气中安静的燃烧,芒白色火焰,在瓶口处有白雾产生)H2+Cl2
2HCl(纯净的氢气在氯气中安静的燃烧,芒白色火焰,在瓶口处有白雾产生)H2+Cl2 2HCl(发生爆炸) 2P+3Cl2
2HCl(发生爆炸) 2P+3Cl2 2PCl3(液态) PCl3+Cl2==PCl5(固态)磷在氯气中剧烈燃烧,产生大量的烟、雾。雾是PCl3,烟是PCl5。氯气能有很多非金属单质反应,如S、C、Si等。
2PCl3(液态) PCl3+Cl2==PCl5(固态)磷在氯气中剧烈燃烧,产生大量的烟、雾。雾是PCl3,烟是PCl5。氯气能有很多非金属单质反应,如S、C、Si等。 ③与碱反应 Cl2+2NaOH==NaCl+NaClO+H2O 2Cl2+2Ca(OH)2==CaCl2+Ca(ClO)2+2H2O
④与某些还原性物质反应:Cl2+2FeCl2===2FeCl3 Cl2+SO2+2H2O==2HCl+H2SO4
⑤有机反应(参与有机反应的取代和加成反应)
CH4+Cl2→CH3Cl+HCl
CH3Cl+Cl2→CH2Cl2+HCl
CH2Cl2+Cl2→CHCl3+HCl
CHCl3+Cl2→CCl4+HCl
Cl2+CH2=CH2→CH2Cl-CH2Cl(加成反应)
⑥与水反应 Cl2+H2O
 HCl+HClO
HCl+HClO 臭氧:
在常温常压下,臭氧是一种有特殊臭味的淡蓝色气体,它的密度比氧气的大。液态臭氧呈深蓝色,沸点为-112.4摄氏度,固态臭氧呈紫黑色,熔点为-251摄氏度。
化学:不稳定,具有极强的氧化性,可用于漂白和消毒
氧气和臭氧的性质比较:
| 名称 | 氧气 | 臭氧 |
| 化学式 | O2 | O3 |
| 相对分子质量 | 32 | 48 |
| 分子空间构型 | 直线型 | V形 |
| 物理性质 | 通常为无色、无味的气体,液态氧为淡蓝色,固态氧为雪花状、淡蓝色。不易溶于水,在常温下 1L水中只能溶解约30mL的氧气。在标准状况下的密度为1.43g/L。熔点54.6K,沸点90K | 通常为有特殊臭味的淡蓝色气体,在水中的溶解度比氧气大。在标准状况F的密度为 2.143g/L。熔点22K,沸点160。6K。液态臭氧呈深蓝色,固态臭氧呈紫黑色 |
| 相互转化 |  |
 |
| 化学性质 | 氧的电负性仅次于氟,但由于O2的分子结构稳定,O2的化学性质不太活泼。在加热或点燃等条件下,O2能氧化除稀有气体、卤素和某些贵重金属以外的金属、非金属单质,众多的还原性化合物 | O3不稳定,在常温下缓慢分解生成氧气,加热可加快O,的分解,MnO2、PbO2、铂黑、氯原子等也能促进O3的分解;O3是极强的氧化剂,煤气、松节油等在O3中能自燃,许多有机色素能被O3氧化,使发色基团遭到破坏变为无色物质。在室温时,O3可将PbS等氧化: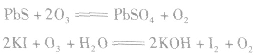 |
| 制法 | O2的工业制法是分离液态空气和电解水。分离液态空气是工业上制取O2最重要的方法。液态氧的沸点(90K)比液态氮的沸点(77K)高,因此氮气首先从液态空气中蒸发出来,剩下的主要就是液态氧了 | 一般使O2通过无声放电的O3发生器来制取O3 |
| 用途 | O2是人类赖以生存的最重要的一种物质。O2在工业上有重要用途,例如利用乙炔在O2中燃烧产生的高温能熔化金属,达到焊接或切割金属的目的;利用纯O2代替空气不但可以加快化学反应速率,还可降低能耗;用纯O2冶炼钢铁,用富氧空气生产氮肥,都取得了很好的效果。另外,O2在医疗中常用来抢救缺氧或呼吸困难的危重病人 | O3的用途主要是利用它的氧化性。近年来,O3在环境保护、漂白等方面日益显示它的作用,例如 O3能使有毒的氰化物、酚等变为无毒物质;能杀死许多细菌;用O3代替Cl2对饮用水消毒,不但杀菌效果好,而且不会带入异昧,且能避免水中产生有副作用的有机氯 |
氧族元素:

发现相似题
与“对水的处理包括水的净化、软化、杀菌、消毒、去离子、蒸馏等...”考查相似的试题有:
- 将氯气缓缓通入含有0.02mol亚硫酸和0.02molHBr的混合溶液中,在此过程中,溶液中的c(H+)与氯气用量的关系示意图正确的是(溶...
- 甲、乙、丙、丁四个集气瓶中装有Cl2、H2、HCl、HBr中的任意一种气体。若将甲和丁两瓶气体混合,见强光则发生爆炸;若将甲和乙...
- 取含MnO2的软锰矿石11.6 g跟足量浓盐酸反应(杂质不参与反应),制得2.24 L Cl2(标准状况),求:(1)这种软锰矿石中MnO2的...
- NaCl是一种化工原料,可以制备一系列物质(如图).下列说法正确的是( )A.工业上常用电解熔融NaCl制备金属钠B.石 灰乳与C...
- 下列说法正确的是A.向久置的氯水中滴入紫色石蕊试液,溶液将先变红后褪色B.漂白粉的有效成分是CaCl2和Ca(ClO)2,应密封保...
- 下图装置可用于收集气体并验证其化学性质,下列对应关系完全正确的是选项气体试剂现象结论ANO紫色石蕊试液溶液变红NO与水反应...
- 某同学利用下图装置,研究氯气的性质.请据图回答:(1)该同学制取氯气的反应原理是:______(写离子方程式).(2)实验过...
- 临沂市的自来水是采用氯气消毒的,为了检验Cl一的存在,最好选用下列物质中的A.石蕊溶液B.四氯化碳C.氢氧化钠溶液D.硝酸...
- 下列关于氯的说法正确的是A.Cl2在化学反应中既能作氧化剂,又能作还原剂B.新制氯水显酸性,向其中滴加少量紫色石蕊试液,充...
- 下列A ~ I九种物质之间的转化关系如图所示;其中部分生成物或反应条件已略去。已知A为固态单质,常温下C、E、F都是无色气体。...