本试题 “化学中质量守恒定律是一个非常重要的定量定律.(1)图1为托盘天平,使用托盘天平称物品的正确操作顺序为(填序号)________.①调游码②放称量纸③称量物放左盘...” 主要考查您对称量器—天平
质量守恒定律
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 称量器—天平
- 质量守恒定律
定义:
天平是用于称量物体质量,狭义上也叫托盘天平(实验室中多用托盘天平)。
常用的精确度不高的天平,由托盘、指针、横梁、标尺、游码、砝码、平衡螺母、分度盘等组成。分度值一般为0.1或0.2克。
一种衡器:由支点(轴)在梁的中心支着天平梁而形成两个臂每个臂上挂着一个盘,其中一个盘里放着已知重量的物体另一个盘里放待称重的物体,固定在梁上的指针在不摆动且指向正中刻度时的偏转就指示出待称重物体的重量。

托盘天平的使用方法:
(1)要放置在水平的地方。游码要归零。
(2)调节平衡螺母(天平两端的螺母)调节零点直至指针对准中央刻度线。
(3)左托盘放称量物,右托盘放砝码(左物右码)。根据称量物的性状应放在玻璃器皿或洁净的纸上,事先应在同一天平上称得玻璃器皿或纸片的质量,然后称量待称物质。
(4)添加砝码从估计称量物的最大值加起,逐步减小。托盘天平只能称准到0.1克。加减砝码并移动标尺上的游码,直至指针再次对准中央刻度线。
(5)过冷过热的物体不可放在天平上称量。应先在干燥器内放置至室温后再称(或在特殊器皿中称量)。
(6)物体的质量=砝码重量+游码所显示的度数
(7)取用砝码必须用镊子轻拿轻放,取下的砝码应放在砝码盒中,称量完毕,应把游码移回零点。
(8)称量干燥的固体药品时,应在两个托盘上各放一张相同质量的纸,然后把药品放在纸上称量。
(9)易潮解的药品,必须放在玻璃器皿上(如:小烧杯、表面皿)里称量。
(10)砝码若生锈,测量结果偏小;砝码若磨损,测量结果偏大。
解题技巧:
1、定物称量:是指对某一物质,用托盘天平称量其质量,例如要称出一铁块的质量。
方法:
①先将游码归零,再调节托盘天平左、右的平衡螺母,至平衡。
②在左盘上放铁块。
③向右盘添加砝码,先加质量大的砝码,再加质量小的砝码,最后移动游码,直至天平平衡。砝码和游码的示数和即为铁块的质量。
2、定量称量:是指用托盘天平称量出一定质量的某物质。例如要称量5.5gNaCl。
方法:
①调节托盘天平平衡螺母至天平平衡。
②在左、右两盘各放一张质量相同的纸。
③向右盘添加5g砝码,再移动游码至0.5g处。
④向左盘不断地加入NaCl.
天平的分类:
有狭义和广义之分。
狭义的天平专指双盘等臂机械天平,是利用等臂杠杆平衡原理,将被测物与相应砝码比较衡量,从而确定被测物质量的一种衡器。
广义的天平则包括双盘等臂机械天平、单盘不等臂机械天平和电子天平3类。
双盘等臂机械天平,一般按结构分为普通标牌天平、微分标牌天平和架盘天平3种。
也可按用途分为检定天平、分析天平、精密天平和普通天平4种。
①检定天平:是计量部门、商检部门或其他有关部门或工厂专门用来检查或校准砝码的天平。
②分析天平:是用于化学分析和物质精确衡量的高准确度天平。在大多数情况下,这类天平的最小分度值都小于最大称量的 10-5。分析天平可按衡量范围和最小分度值分为常量天平(称量和最小分度值分别为100~200g和0.01~1mg)、半微量天平(30~100g和1~10g)、微量天平(3~30g和0.1~1g)和超微量天平(3~5g和0.1g以下)。
③精密天平:广泛应用于各种物质的精密衡量,其最小分度值通常为最大称量的10-5~10-4。
④普通天平:用作物质的一般衡量。最小分度值等于或大于最大称量的10-4。
质量守恒定律的概念及对概念的理解:
(1)概念:参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。这个规律就叫做质量守恒定律。
(2)对概念的理解:
①质量守恒定律只适用于化学反应,不能用于物理变化例如,将2g水加热变成2g水蒸气,这一变化前后质量虽然相等,但这是物理变化,不能说它遵守质量守恒定律。
②质量守恒定律指的是“质量守恒”,不包括其他方面的守恒,如对反应物和生成物均是气体的反应来说,反应前后的总质量守恒,但是其体积却不一定守恒。
③质量守恒定律中的第一个“质量”二字,是指“参加”化学反应的反应物的质量,不是所有反应物质量的任意简单相加。
例如,2g氢气与8g氧气在点燃的条件下,并非生成10g水,而是1g氢气与8g氧气参加反应,生成9g水
④很多化学反应中有气体或沉淀生成,因此“生成的各物质质量总和”包括了固态、液态和气态三种状态的物质,不能把生成的特别是逸散到空气中的气态物质计算在“总质量”之外而误认为化学反应不遵循质量守恒定律
质量守恒定律的微观实质:
(1)化学反应的实质在化学反应过程中,参加反应的各物质(反应物) 的原子,重新组合而生成其他物质(生成物)的过程。由分子构成的物质在化学反应中的变化过程可表示为:

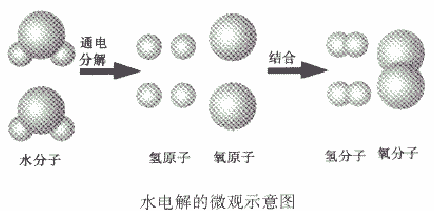
(2)质量守恒的原因在化学反应中,反应前后原子的种类没有改变,数目没有增减,原子本身的质量也没有改变,所以,反应前后的质量总和必然相等。例如,水通电分解生成氢气和氧气,从微观角度看:当水分子分解时,生成氢原子和氧原子,每两个氢原子结合成一个氢分子,每两个氧原子结合成一个氧分子。
质量守恒定律的延伸和拓展理解:
质量守恒定律要抓住“六个不变”,“两个一定变”“两个可能变”。
如从水电解的微观示意图能得出的信息:
①在化学反应中,分子可以分成原子,原子又重新组合成新的分子;
②一个水分子是由两个氢原子和一个氧原子构成的,或一个氧分子由两个氧原子构成、一个氧分子由两个氢原子构成。或氢气、氧气是单质,水是化合物
③原子是化学变化中的最小粒子。
④水是由氢、氧两种元素组成的。
⑤在化学反应,氧元素的种类不变。
⑥在化学反应中,原子的种类、数目不变。
⑦参加反应的各物质的质量总和等于反应后生成的各物质的质量总和。
质量守恒定律的发现:
1. 早在300多年前,化学家们就对化学反应进行定量研究。1673年,英国化学家波义耳(RobertBoyle, 1627-1691)在一个敞口的容器中加热金属,结果发现反应后容器中物质的质量增加了。
2. 1756年,俄国化学家罗蒙诺索夫把锡放在密闭的容器里锻烧,锡发生变化,生成白色的氧化锡,但容器和容器里物质的总质量,在锻烧前后并没有发生变化。经过反复实验,都得到同样的结果,于是他认为在化学变化中物质的质量是守恒的。
3. 1774年,法国化学家拉瓦锡用精确的定量实验法,在密封容器中研究氧化汞的分解与合成中各物质质量之间的关系,得到的结论是:参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和。
4. 后来.人们用先进的测址仪器做了大量精度极高的实验,确认拉瓦易的结论是正确的。从此,质量守恒定律被人们所认识。
质量守恒定律的应用:
(1)解释问题
①解释化学反应的本质—生成新物质,不能产生新元素(揭示伪科学的谎言问题)。
②解释化学反应前后物质的质量变化及用质量差确定某反应物或生成物。
(2)确定反应物或生成物的质量
确定反应物或生成物的质量时首先要遵循参加反应的各种物质的质量总量等于生成的各种物质的质量总和;其次各种物质的质量比等于相对分子质量与化学计量数的乘积之比。
(3)确定物质的元素组成
理解在化学反应前后,元素的种类不发生改变。可通过计算确定具体的元素质量。
(4)确定反应物或生成物的化学式
比较反应前后各种原子个数的多少,找出原子个数的差异。但不能忘记化学式前的化学计量数。
(5)确定某物质的相对分子质量(或相对原子质量)
运用质量守恒定律确定某物质的相对分子质量 (或相对原子质量)时,首先寻找两种已知质量的物质,再根据化学方程式中各物质间的质量成正比即可计算得出。注意观察物质化学式前面的化学计量数。
(6)确定化学反应的类型
判定反应的类型,首先根据质量守恒定律判断反应物、生成物的种类和质量(从数值上看,反应物质量减少,生成物质最增加)。如果是微观示意图,要对比观察减少的粒子和增加的粒子的种类和数目再进行判断。
(7)判断化学方程式是否正确
根据质量守恒定律判断化学方程式的对与否关键是看等号两边的原子总数是否相等,同时注意化学式书写是否有误。
(1)概念:参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。这个规律就叫做质量守恒定律。
(2)对概念的理解:
①质量守恒定律只适用于化学反应,不能用于物理变化例如,将2g水加热变成2g水蒸气,这一变化前后质量虽然相等,但这是物理变化,不能说它遵守质量守恒定律。
②质量守恒定律指的是“质量守恒”,不包括其他方面的守恒,如对反应物和生成物均是气体的反应来说,反应前后的总质量守恒,但是其体积却不一定守恒。
③质量守恒定律中的第一个“质量”二字,是指“参加”化学反应的反应物的质量,不是所有反应物质量的任意简单相加。
例如,2g氢气与8g氧气在点燃的条件下,并非生成10g水,而是1g氢气与8g氧气参加反应,生成9g水
④很多化学反应中有气体或沉淀生成,因此“生成的各物质质量总和”包括了固态、液态和气态三种状态的物质,不能把生成的特别是逸散到空气中的气态物质计算在“总质量”之外而误认为化学反应不遵循质量守恒定律
质量守恒定律的微观实质:
(1)化学反应的实质在化学反应过程中,参加反应的各物质(反应物) 的原子,重新组合而生成其他物质(生成物)的过程。由分子构成的物质在化学反应中的变化过程可表示为:

(2)质量守恒的原因在化学反应中,反应前后原子的种类没有改变,数目没有增减,原子本身的质量也没有改变,所以,反应前后的质量总和必然相等。例如,水通电分解生成氢气和氧气,从微观角度看:当水分子分解时,生成氢原子和氧原子,每两个氢原子结合成一个氢分子,每两个氧原子结合成一个氧分子。

质量守恒定律的延伸和拓展理解:
质量守恒定律要抓住“六个不变”,“两个一定变”“两个可能变”。
| 六个不变 | 宏观 | 反应前后的总质量不变 |
| 元素的种类不变 | ||
| 元素的质量不变 | ||
| 微观 | 原子的种类不变 | |
| 原子的数目不变 | ||
| 原子的质量不变 |
| 两个一定变 | 物质的种类一定变 |
| 构成物质的分子种类一定变 |
| 两个可能变 | 分子的总数可能变 |
| 元素的化合价可能变 |
如从水电解的微观示意图能得出的信息:
①在化学反应中,分子可以分成原子,原子又重新组合成新的分子;
②一个水分子是由两个氢原子和一个氧原子构成的,或一个氧分子由两个氧原子构成、一个氧分子由两个氢原子构成。或氢气、氧气是单质,水是化合物
③原子是化学变化中的最小粒子。
④水是由氢、氧两种元素组成的。
⑤在化学反应,氧元素的种类不变。
⑥在化学反应中,原子的种类、数目不变。
⑦参加反应的各物质的质量总和等于反应后生成的各物质的质量总和。
质量守恒定律的发现:
1. 早在300多年前,化学家们就对化学反应进行定量研究。1673年,英国化学家波义耳(RobertBoyle, 1627-1691)在一个敞口的容器中加热金属,结果发现反应后容器中物质的质量增加了。
2. 1756年,俄国化学家罗蒙诺索夫把锡放在密闭的容器里锻烧,锡发生变化,生成白色的氧化锡,但容器和容器里物质的总质量,在锻烧前后并没有发生变化。经过反复实验,都得到同样的结果,于是他认为在化学变化中物质的质量是守恒的。
3. 1774年,法国化学家拉瓦锡用精确的定量实验法,在密封容器中研究氧化汞的分解与合成中各物质质量之间的关系,得到的结论是:参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和。
4. 后来.人们用先进的测址仪器做了大量精度极高的实验,确认拉瓦易的结论是正确的。从此,质量守恒定律被人们所认识。
质量守恒定律的应用:
(1)解释问题
①解释化学反应的本质—生成新物质,不能产生新元素(揭示伪科学的谎言问题)。
②解释化学反应前后物质的质量变化及用质量差确定某反应物或生成物。
(2)确定反应物或生成物的质量
确定反应物或生成物的质量时首先要遵循参加反应的各种物质的质量总量等于生成的各种物质的质量总和;其次各种物质的质量比等于相对分子质量与化学计量数的乘积之比。
(3)确定物质的元素组成
理解在化学反应前后,元素的种类不发生改变。可通过计算确定具体的元素质量。
(4)确定反应物或生成物的化学式
比较反应前后各种原子个数的多少,找出原子个数的差异。但不能忘记化学式前的化学计量数。
(5)确定某物质的相对分子质量(或相对原子质量)
运用质量守恒定律确定某物质的相对分子质量 (或相对原子质量)时,首先寻找两种已知质量的物质,再根据化学方程式中各物质间的质量成正比即可计算得出。注意观察物质化学式前面的化学计量数。
(6)确定化学反应的类型
判定反应的类型,首先根据质量守恒定律判断反应物、生成物的种类和质量(从数值上看,反应物质量减少,生成物质最增加)。如果是微观示意图,要对比观察减少的粒子和增加的粒子的种类和数目再进行判断。
(7)判断化学方程式是否正确
根据质量守恒定律判断化学方程式的对与否关键是看等号两边的原子总数是否相等,同时注意化学式书写是否有误。
发现相似题
与“化学中质量守恒定律是一个非常重要的定量定律.(1)图1为托...”考查相似的试题有:
- 下列仪器中,能在酒精灯火焰上直接加热的是 A.烧杯B.试管C.集气瓶D.量筒
- 有些化学实验必须严格遵循操作的顺序,请你举出两个这样的实验,并仿照示例填写下表必须遵循操作顺序的实验先做什么再做什么...
- 如图是某反应的微观示意图,若○表示氧原子,●表示氢原子,有关说法正确的是( )A.图中甲、乙、丙三种物质都是氧化物B.该反...
- 某同学用高锰酸钾制取氧气,收集到他所需要的氧气后停止加热,高锰酸钾未完全分解.剩余固体混合物中锰元素和氧元素的质量之...
- 氯气(C12)和氧气一样,都是活泼的非金属单质.在一定条件下,甲烷和充足的氯气反应,推测其产物是( )A.CCl4和HClB.CCl4...
- 已知在一定条件下,反应物甲3g跟反应物乙14g恰好完全反应,生成新物质丙17g,则下列数据符合质量守恒定律的组号是( )组号反...
- 煤是重要的化工原料,也是居民在冬天取暖的主要能源之一.煤中含有少量的硫,硫在燃烧时生成二氧化硫气体而造成大气污染.小...
- 在化学反应A+2B=3C+D中,6gA恰好与8gB完全反应,有9gD生成.若要生成15gC,则参加反应的B的质量为( )A.8gB.24gC.12gD.16g
- 将A,B,C,D四种物质放在密闭容器中加热,化学反应前后四种物质的质量关系如下:处理数据后结论正确的是( ) ABCD反应前质...
- 化学物质及其变化同日常生活密切相关.(1)检验市场上销售的食盐中是否有碘元素(元素符号为I)的一种方法,是在酸性条件下...