本试题 “某校两个生物兴趣小组的同学打算用车前草和酵母菌完成一些高中生物实验,有些问题需要你的帮助。(1)甲组选用车前草作材料进行如下实验:①取其叶片进行《观察...” 主要考查您对实验:使用高倍显微镜观察几种细胞
探究:植物细胞的吸水和失水
探究:培养液中酵母菌种群数量的变化
细胞和酶的固定化
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 实验:使用高倍显微镜观察几种细胞
- 探究:植物细胞的吸水和失水
- 探究:培养液中酵母菌种群数量的变化
- 细胞和酶的固定化
高倍镜的使用步骤(尤其要注意第1和第4步)
(1)在低倍镜调节(粗准焦螺旋和细准焦螺旋)下找到物象,将物象移至(视野中央)。
(2)转动(转换器),换上高倍镜。
(3)调节(光圈)和(反光镜),使视野亮度适宜。
(4)调节(细准焦螺旋),使物象清晰。
显微镜使用方法总结:
1、一取二放,三安装,四转低倍,五对光,六上玻片,七下降,八升镜筒,细观赏,看完低倍,转高倍,九退!
2、在使用高倍镜时应先用低倍镜找到所要观察的目标,观察的标本应选择没有细胞重叠的区域。
3、若镜头脏了,不能用手擦,也不能用布擦,应用专门的擦镜纸来擦。
4、标本切的厚薄不均匀导致物像一部分清晰,另一部分较模糊。反光镜调整不好,会导致视野一半明亮,一半黑暗。
知识点拨:
(1)进行显微镜对光时,应转动反光镜或是光圈,使视野明亮,便于使用高倍镜观察。
(2)制作临时装片时,如果观察的是植物细胞,在载玻片上滴加清水;如果观察人的口腔上皮细胞,需要滴加质量分数为0.9%的NaCl溶液。
(3)无论选取动物组织细胞还是植物组织细胞,一定要量少,并且要在载玻片上将观察材料展开,以便于观察。
(4)观察时,要遵循先在低倍镜下观察清楚,将物像移至视野中央,再转换高倍镜进行观察的顺序。在使用高倍镜进行观察时,不能转动粗准焦螺旋。
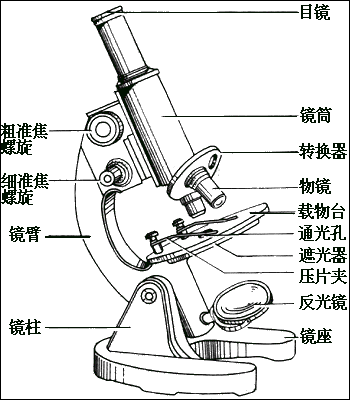
显微镜的结构图:
植物细胞和动物细胞的简图:
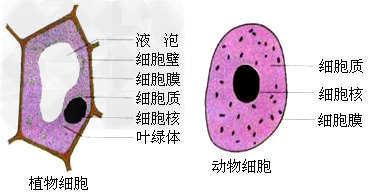
知识拓展:
1、低倍镜换高倍镜后细胞数目的计算:
(1)放大倍数问题 放大倍数是指物像的大小与物体大小的比例。显微镜的放大倍数=物镜倍数×目镜倍数。放大倍数指的是物体的宽度或长度的放大倍数,而不是面积或体积的放大倍数。
(2)放大倍数的变化与视野中细胞数目的变化关系:
①若视野中细胞成单行,计算时只考虑长度,可根据看到的细胞数量与放大倍数成反比的规律进行计算。如:在显微镜放大倍数为40倍时看到m个细胞,放大倍数变成400倍时看到的细胞数日=m÷(400÷40)=m/10(个)。
②若视野中细胞均匀分布,可根据看到的细胞数目与放大倍数的平方成反比的规律进行计算。如:在显微镜放大倍数为40倍时看到m个均匀分布的细胞,放大倍数变为400倍时看到的细胞数日=m÷(400÷40)2=m/100(个)。
2、显微镜的放大径向放大,放大倍数是目镜与物镜放大倍数的乘积,且放大的是长和宽不是面积。
3、目镜和物镜的比较:
(1)目镜越长,放大倍数越小,反之放大倍数越大;
(2)物镜上有螺纹,物镜越长放大倍数越大,物象清晰时距离装片越近。
4、污点位置分析:
(1)污点的位置可能有三个:物镜、目镜或装片。
(2)判断方法:先移动装片,若污点移动说明污点在装片上。若不移动,再转动目镜,若污点也转动说明污点在目镜上。若污点不转动,在转动转换器换用其他物镜,若污点消失,说明污点在物镜上。
5、成像:
(1)显微镜的成像特点是倒像,相当于把标本水平转180度后所呈现的状态。如“b”成的物象是“q”。
(2)将物象移到视野中央时,物象在“左下方”就将装片向“左下方”移动,即在哪往哪移。
6、高倍镜、低倍镜与视野大小、明暗的关系:
| 高倍镜 | 大 | 少 | 暗 | 近 | 小 |
| 低倍镜 | 小 | 多 | 亮 | 远 | 大 |
一、实验目的:
(1)学会观察植物细胞质壁分离与复原的方法。
(2)了解植物细胞发生渗透作用的原理。
二、实验原理:
1、原生质层的伸缩性比细胞壁的伸缩性大。
2、当外界溶液浓度大于细胞液浓度时,细胞失水,原生质层收缩进而质壁分离。
3、当细胞液浓度大于外界溶液浓度时,细胞渗透吸水,使质壁分离复原。
三、实验步骤:
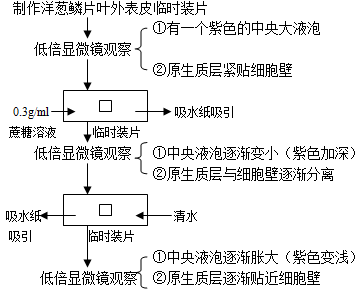
四、实验现象
知识点拨:
1、实验注意问题:
(1)盖盖玻片应让盖玻片的一侧先触及载玻片,然后轻轻放平。防止装片产生气泡。
(2)液泡含花青素,所以液泡呈紫色。
(3)先观察正常细胞与后面的“质壁分离”起对照作用。
(4)蔗糖溶液浓度大于细胞液浓度,细胞通过渗透作用失水,细胞壁伸缩性小原生质层的伸缩性大,液泡和原生质层不断收缩,所以发生质壁分离。为了使细胞完全浸入蔗糖溶液中。否则,细胞严重失水死亡,看不到质壁分离的复原。
(5)发生质壁分离的装片,不能久置,要马上滴加清水,使其复原。重复几次。细胞液的浓度高于外界溶液,细胞通过渗透作用吸水,所以发生质壁分离复原现象。因为细胞失水过久,也会死亡。为了使细胞完全浸入清水中。
2、质壁分离复原需要将发生质壁分离的植物细胞再置于低浓度的溶液或清水中,但如果所用外界溶液为葡萄糖、KNO,、NaCI、尿素、乙二醇等,质壁分离后因细胞主动或被动吸牧溶质微粒而使细胞液浓度增大,植物细胞会吸水引起质壁分离后的自动复原。
3、植物细胞发生质壁分离后,在原生质层和细胞壁之间充斥的液体为外界溶液(如蔗糖溶液)。
4、质壁分离过程中,外界溶液浓度大于细胞液浓度,质壁分离程度越大,植物细胞吸水能力越强;质壁分离复原过程中,外界溶液浓度小于细胞液浓度。
5、原核生物不会发生质壁分离,这要从两方面考虑。“质壁分离”的内因:要有细胞壁、大液泡和一定的细胞液浓度;“质壁分离”的外因:外界溶液的浓度>细胞液的浓度。相当多的“原核生物”虽然有细胞壁,但通常无大液泡。
知识拓展:

3、细胞发生质壁分离的判断与应用
在判断细胞是否发生质壁分离及其复原时有如下规律
(l)从细胞角度分析
①死细胞、动物细胞、原核细胞及未成熟的植物细胞不发生质壁分离现象。
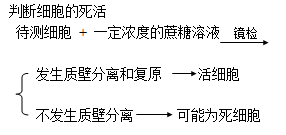
②具中央大液泡的成熟植物细胞才可发生质壁分离现象。
(2)从溶液角度分析
①在一定浓度(溶质不能穿膜)的溶液中细胞只会发生质壁分离现象,不能自动复原。
②在一定浓度(溶质可穿膜)的溶液中细胞先发生质壁分离后自动复原,如甘油、尿素、乙醇、KN03等。 ③在高浓度溶液中细胞可发生质壁分离现象,但不会发生质壁分离复原。
即:




(1)酵母菌可以用液体培养基来培养,培养液中的酵母菌种群的增长情况与培养液中的成分、空间、pH、温度等因素有关,我们可以根据培养液中的酵母菌数量和时间为坐标轴做曲线,从而掌握酵母菌种群数量的变化情况。
(2)利用血球计数板在显微镜下直接计数是一种常用的细胞计数法,这种方法可以直接测定样品中全部的细胞数目,所以一般用于单细胞微生物数量的测定,由于血球计数板上的计数室盖上盖玻片后的容积是一定的,所以可根据在显微镜下观察到的细胞数目来计算单位体积的细胞的总数目。
二、探究问题
培养液中酵母菌种群的数量是怎样随时间变化的?
三、作出假设:在有限的环境条件下,酵母菌种群的数量随时间呈什么型增长变化。
四、材料用具
酵母菌菌种,无菌马铃薯培养液或肉汤培养液,无菌水,试管,棉塞,恒温培养箱,显微镜,无菌滴管,无菌移液管,小烧杯或小试管,血球计数板(2mm×2mm)、纱布、滤纸、镊子、盖玻片等。五、探究思路
怎样进行酵母菌的计数。对一支试管中的培养液(可定为10ml)中的酵母菌逐个计数是非常困难的,可以采用抽样检测的方法:先将盖玻片放在计数室上,用吸管吸取培养液,滴于盖玻片边缘,让培养液自行渗入,多余培养液用滤纸吸去,稍待片刻,待酵母菌细胞全部沉降到计数室底部,将计数板放在载物台的中央,计数一个小方格内的酵母菌数量,再以此为根据,估算试管中的酵母菌总数。盖玻片下,培养液厚度为0.1mm,可算出10ml培养液中酵母菌总数的公式:2.5×104x(x为小方格内酵母菌数)
1、概念:使用固定化酶技术,将这种酶固定在一种颗粒状的载体上,再将这些酶颗粒装到一个反应柱内,柱子底端装上分布着许多小孔的筛板。酶颗粒无法通过筛板的小孔,而反应溶液却可以自由出入。生产过程中,将葡萄糖溶液从反应柱的上端注入,使葡萄糖溶液流过反应柱,与固定化葡萄糖异构酶接触,转化成果糖,从反应柱的下端流出。反应柱能连续使用半年,大大降低了生产成本,提高了果糖的产量和质量。
2、固定方法:
| 名称 | 原理 | 图示 | 适用范围 |
| 包埋法 | 将微生物细胞均匀地包埋在不溶于水的多孔性载体中 |  |
多用于细胞的固定 |
| 化学结合法 | 利用共价链、离子键将酶分子或细胞相互结合,或将其结合到载体上 |  |
多用于酶的固定 |
| 物理吸附法 | 欧诺个过物理吸附作用,把酶固定在纤维素、琼脂糖、多孔玻璃和离子交换树脂等载体上 |  |
3、载体:包埋法 固定化细胞常用的是不容于水的多孔性载体材料,如明胶、琼脂糖、海藻酸钠、醋酸纤维素和聚丙烯酰胺等。
4、优点:
(1)固定化酶优点:使酶既能与反应物接触,又能与产物分离,还可以被反复利用。
(2)固定化细胞优点:成本更低,操作更容易,可以催化一系列的化学反应。
5、固定化没的反应实例——生产高果糖浆
(1)高果糖浆的生产原理
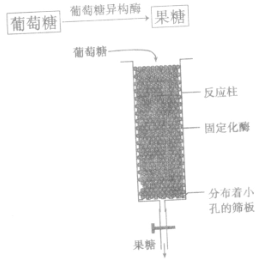
(2)葡萄糖异构酶的固定:将葡萄糖异构酶固定在颗粒状载体上,装入反应柱中。
(3)高果糖浆的生产操作:(如图)从反应柱上端注入葡萄糖溶液,从下端流出果糖溶液,一个反应拄可连续使用半年。
6、固定化细胞的应用实例——固定化酵母细胞

知识点拨:
1、注意事项
(1)配制海藻酸钠溶液:小火、间断加热、定容,如果加热太快,海藻酸钠会发生焦糊。
(2)海藻酸钠溶液与酶母细胞混合:冷却后再混合,注意混合均匀,不要进入气泡
(3)制备固定化酵母细胞:高度适宜,并匀速滴入
(4)刚形成的凝胶珠应在CaCl2溶液中浸泡一段时间,以便Ca2+与Na+充分交换,形成的凝胶珠稳定。检验凝胶珠是否形成,可用下列方法:用镊子夹起一个凝胶珠放在实验桌上用手挤压,如果不容易破裂,没有液体流出就表明成功地制成了凝胶珠,还可以用手将凝胶珠在实验桌上用力摔打,如果凝胶珠很容易弹起,也表明制备的凝胶珠是成功的。
(5)凝胶珠的颜色和形状
如果制作的凝胶珠颜色过浅、呈白色,说明海藻酸钠的浓度偏低,固定的酵母细胞数目较少;如果形成的凝胶珠不是圆形或椭圆形,则说明海藻酸钠的浓度偏高,制作失败,需要再作尝试。
(6) 海藻酸钠在水中溶解的速度较慢,需要通过加热促进其溶解。溶解海藻酸钠,最好采用小火间断加热的方法。例如,加热几分钟后,从石棉网上去下烧杯冷却片刻,并不断搅拌,再将烧杯放回石棉网继续加热,如此重复数次,直至海藻酸钠完全溶化。如果加热太快,海藻酸钠会发生焦糊。
2、酵母菌活化时体积会变大,因此活化前应选择体积足够大的容器,防止酵母菌细胞的活化液溢出。
3、海藻酸钠溶液的配制是固定化酵母细胞的关键,因为如果海藻酸钠浓度过高,将很难形成凝胶珠,如果浓度过低,形成的凝胶珠所包埋的酵母细胞的数量少,也会影响实验效果。
4、溶化海藻酸钠时要用小火或间断加热,避免海藻酸钠发生焦糊。
5、将溶化后的海藻酸钠先冷却至室温,再与酵母菌混合,避免高温杀死酵母细胞。
与“某校两个生物兴趣小组的同学打算用车前草和酵母菌完成一些高...”考查相似的试题有:
- 在显微镜下能看到细胞核的是[ ]A.根尖细胞有丝分裂中期B.根尖细胞有丝分裂后期C.正在分裂的细菌D.正在分化的根尖细胞
- 回答有关“使用高倍镜观察几种细胞”操作过程中的问题。(1)首先在低倍镜下观察,找到_________。(2)要转入高倍镜观察,正确的操...
- 观察紫色洋葱表皮细胞质壁分离和质壁分离复原实验中,证明质壁分离现象的是[ ]A.液泡由小变大,紫色变浅B.液泡由小变大,紫...
- 下列关于生物学实验操作、实验结果、实验现象及原理的描述中,正确的是[ ]A.用纸层析法分离菠菜滤液中的色素时,橙黄色的色...
- 实验室利用洋葱、菠菜等实验材料可进行下列实验:A.观察植物细胞的有丝分裂 B.观察植物细胞的质壁分离与复原 C.观察植物细...
- “检测生物组织中的糖类、脂肪和蛋白质”“植物细胞的吸水和失水”“叶绿体中色素的提取和分离”“观察DNA和RNA在细胞中的分布”四个...
- 下图表示一个细胞的亚显微结构立体模式图的一部分。请据图回答。(1)图中标号2参与__________的形成。与自然界碳循环关系最密...
- 下面是制备固定化酵母细胞的步骤,正确的是①配制CaCl2溶液 ②海藻酸钠溶化 ③海藻酸钠与酵母细胞混合 ④酵母细胞的活化 ⑤固定化...
- (附加题)制备固定化酵母细胞,常用的包埋材料和包埋方法依次是[ ]A.海藻酸钠,化学结合法B.氯化钙,物理吸附法C.海藻酸钠...
- 下列关于固定化酶中的酶,说法正确的是[ ]A.酶的种类多样,可催化一系列的酶促反应B.酶被固定在不溶于水的载体上,可反复利...