本试题 “某同学设计了以下操作流程来除去混在氯化钠固体中的少量硫酸钠和氯化钙。(1)试剂A是__________,试剂A需要过量的原因是___________。(2)操作a得到的滤渣...” 主要考查您对电解饱和氯化钠溶液
粗盐的提纯
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 电解饱和氯化钠溶液
- 粗盐的提纯
电解饱和氯化钠溶液:
在小烧杯(或U型管)里装入饱和食盐水,滴入几滴酚酞试液。用导线把碳棒、电池、电流表和铁钉相连(如图)。接通直流电源后,注意观察电流表的指针是否偏转,以及小烧杯内发生的现象,并用湿润的碘化钾淀粉试纸检验阳极放出的气体。
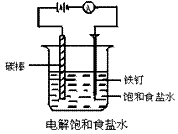
注:粗铁钉要与直流电源的阴极相连,碳棒与阳极相连。
用玻璃棒沾湿润的KI淀粉试纸检验阳极气体。
(1)饱和食盐水电解时,电流表指针发生偏转,阴、阳极均有气体放出,阳极气体有刺激性气味,并能使湿润的KI淀粉试纸变蓝,且阴极区溶液变红。
(2) 阳极:2Cl--2e-==Cl2↑
阴极:2H++2e-==H2↑(或2H2O+2e-==2OH-+H2↑)
总反应式:2NaCl+2H2O 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑
(3)阴极区溶液变红的原因:这是由于饱和食盐水中,水所电离出的H+在阴极放电,破坏了水的电离平衡
(H2O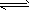 H++OH-)致使阴极区附近溶液中的OH-相对较多,溶液呈碱性,故酚酞变红。
H++OH-)致使阴极区附近溶液中的OH-相对较多,溶液呈碱性,故酚酞变红。
(4)例用电解饱和食盐水溶液可制取氢气、氯气和烧碱。
在小烧杯(或U型管)里装入饱和食盐水,滴入几滴酚酞试液。用导线把碳棒、电池、电流表和铁钉相连(如图)。接通直流电源后,注意观察电流表的指针是否偏转,以及小烧杯内发生的现象,并用湿润的碘化钾淀粉试纸检验阳极放出的气体。

注:粗铁钉要与直流电源的阴极相连,碳棒与阳极相连。
用玻璃棒沾湿润的KI淀粉试纸检验阳极气体。
(1)饱和食盐水电解时,电流表指针发生偏转,阴、阳极均有气体放出,阳极气体有刺激性气味,并能使湿润的KI淀粉试纸变蓝,且阴极区溶液变红。
(2) 阳极:2Cl--2e-==Cl2↑
阴极:2H++2e-==H2↑(或2H2O+2e-==2OH-+H2↑)
总反应式:2NaCl+2H2O
 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑ (3)阴极区溶液变红的原因:这是由于饱和食盐水中,水所电离出的H+在阴极放电,破坏了水的电离平衡
(H2O
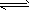 H++OH-)致使阴极区附近溶液中的OH-相对较多,溶液呈碱性,故酚酞变红。
H++OH-)致使阴极区附近溶液中的OH-相对较多,溶液呈碱性,故酚酞变红。 (4)例用电解饱和食盐水溶液可制取氢气、氯气和烧碱。
粗盐的提纯:
(1)实验仪器和药品
药品:粗盐,水
器材:托盘天平,量筒,烧杯,玻璃棒,药匙,漏斗,铁架台(带铁圈),蒸发皿,酒精灯,坩埚钳,胶头滴管,滤纸,剪刀,火柴,纸片
(2)实验原理:粗盐中含有泥沙等不溶性杂质,以及可溶性杂质如:Ca2+、Mg2+等不溶性杂质可以用溶解、过滤的方法除去,然后蒸发水分得到较纯净的精盐
(3)实验操作
①溶解:用托盘天平称取5克粗盐(精确到0.1克)。用量筒量取10毫升水倒入烧杯里.用药匙取一匙粗盐加入水中,观察发生的现象。用玻璃棒搅拌,并观察发生的现象(玻璃棒的搅拌对粗盐的溶解起什么作用?)。接着再加入粗盐,边加边用玻璃棒搅拌,一直加到粗盐不再溶解时为止。观察溶液是否浑浊。
在天平上称量剩下的粗盐,计算在10毫升水中大约溶解了多少克粗盐.
②过滤:按照过滤的操作进行过滤,仔细观察滤纸上的剩余物及滤液的颜色。滤液仍浑浊时,应该再过滤一次。如果经两次过滤滤液仍浑浊,则应检查实验装置并分析原因,例如:滤纸破损,过滤时漏斗里的液面高于滤纸边缘,仪器不干净等,找出原因后,要重新操作。
③蒸发:把得到的澄清滤液倒入蒸发皿,把蒸发皿放在铁架台的铁圈上,用酒精灯加热,同时用玻璃棒不断搅拌滤液。等到蒸发皿中出现较多量固体时,停止加热。利用蒸发皿的余热使滤液蒸干。
④用玻璃棒把固体转移到纸上,称量后,回收到教师指定的容器,比较提纯前后食盐的状态并计算精盐的产率。
(1)实验仪器和药品
药品:粗盐,水
器材:托盘天平,量筒,烧杯,玻璃棒,药匙,漏斗,铁架台(带铁圈),蒸发皿,酒精灯,坩埚钳,胶头滴管,滤纸,剪刀,火柴,纸片
(2)实验原理:粗盐中含有泥沙等不溶性杂质,以及可溶性杂质如:Ca2+、Mg2+等不溶性杂质可以用溶解、过滤的方法除去,然后蒸发水分得到较纯净的精盐
(3)实验操作
①溶解:用托盘天平称取5克粗盐(精确到0.1克)。用量筒量取10毫升水倒入烧杯里.用药匙取一匙粗盐加入水中,观察发生的现象。用玻璃棒搅拌,并观察发生的现象(玻璃棒的搅拌对粗盐的溶解起什么作用?)。接着再加入粗盐,边加边用玻璃棒搅拌,一直加到粗盐不再溶解时为止。观察溶液是否浑浊。
在天平上称量剩下的粗盐,计算在10毫升水中大约溶解了多少克粗盐.
②过滤:按照过滤的操作进行过滤,仔细观察滤纸上的剩余物及滤液的颜色。滤液仍浑浊时,应该再过滤一次。如果经两次过滤滤液仍浑浊,则应检查实验装置并分析原因,例如:滤纸破损,过滤时漏斗里的液面高于滤纸边缘,仪器不干净等,找出原因后,要重新操作。
③蒸发:把得到的澄清滤液倒入蒸发皿,把蒸发皿放在铁架台的铁圈上,用酒精灯加热,同时用玻璃棒不断搅拌滤液。等到蒸发皿中出现较多量固体时,停止加热。利用蒸发皿的余热使滤液蒸干。
④用玻璃棒把固体转移到纸上,称量后,回收到教师指定的容器,比较提纯前后食盐的状态并计算精盐的产率。
发现相似题
与“某同学设计了以下操作流程来除去混在氯化钠固体中的少量硫酸...”考查相似的试题有:
- 关于下列四个图像的说法中正确的是[ ]A.图④表示可逆反应“CO(g)+H2O(g)CO2(g)+H2(g)” 中的△H大于0B.图②是以石墨为电极电解氯化...
- (8分)某同学为了验证海带中含有碘,拟进行如下实验,请回答相关问题。(1)第1步:灼烧。操作是将足量海带灼烧成灰烬。该过...
- 下列实验方法正确的是A.用分液漏斗分离乙酸和乙酸乙酯B.用品红溶液鉴别SO2和CO2两种气体C.用Ca(OH)2溶液鉴别Na2CO3溶液和N...
- 某课外活动小组根据Mg与CO2的反应原理,探究Mg与NO2的反应及固体产物。该小组通过实验确认Mg能在NO2中燃烧,并对固体产物提出...
- 可以一次鉴别出乙酸、乙醇、乙酸乙酯、葡萄糖四种物质的试剂是A.溴水B.Na2CO3溶液C.石蕊试液D.碱性Cu(OH)2悬浊液
- 下列物质中可用来干燥NH3的是A.浓H2SO4B.碱石灰C.P2O5D.无水CaCl2
- 某综合实践活动小组到自来水厂进行参观,了解到源水处理成自来水的工艺流程示意图如下:⑴源水中含Ca2+、Mg2+、HCO3-、Cl-等...
- (14分)在浓CaCl2溶液中通入NH3和CO2,可以制得纳米级碳酸钙(粒子直径在1~100nm之间)。下图所示A~E为实验室常见的仪器装置...
- 物质的鉴别有多种方法。下列能达到鉴别目的的是( ) ①用水鉴别苯、乙醇、溴苯②用相互滴加的方法鉴别Ca(OH)2和NaHCO3溶液③点...
- 下列实验操作中错误的是( )。A.分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出B.蒸馏时,应使温度计水银球靠近蒸...