本试题 “氯化钠用途广泛,不但是重要的调味品,又是重要的工业原料.(1)通过晾晒海水或煮盐井水、盐湖水等均可得到含有较多杂质的氯化钠晶体:粗盐,这种方法属于__...” 主要考查您对原子结构
离子符号的意义及写法
海水“晒盐”的原理和过程
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 原子结构
- 离子符号的意义及写法
- 海水“晒盐”的原理和过程
原子的构成:

原子核的构成:

原子核相对原子来说,体积很小,但质量却很大,原子的质量主要集中在原子核上,电子的质量约为质子质量的 。
。
质子的质量为:1.6726×10-27kg
中子的质量为:1.6749×10-27kg
构成原子的粒子间的关系:

对原子构成的正确理解:
(1)原子核位于原子中心,绝大多数由质子和中构成 (有一种氢原子的原子核内只含有1个质子,无中子),体积极小,密度极大,几乎集中了原子的全部质量,核外电子质量很小,可以忽略不计。
(2)每个原子只有一个原子核,核电荷数(核内质子数)的多少,决定了原了的种类。
(3)在原子中:核电荷数二质子数二核外电子数。
(4)原子核内的质子数不一定等干中子数,如钠原子中,质子数为11,中子数为12。
(5)并不是所有的原子中都有中子,如有一种氢原子中就没有中子。
(6)在原子中,由于质子(原子核)与电子所带电荷数相等,且电性相反,因而原子中虽然存在带电的粒子,但原子在整体上不显电性。
核外电子的排布:
①电子层核外电子运动有自己的特点,在含有多个电子的原子里,有的电子通常在离核较近的区域运动,有的电子通常在离核较远的区域运动,科学家形象地将这些区域称为电子层。
②核外电子的分层排布通常用电子层来形象地表示运动着的电子离核远近的不同:离核越近,电子能量越低;离核越远,电子能量越高。电子层数、离核远近、能量高低的关系如下所示:
电子层数 1 2 3 4 5 6 7
离核远近 近→ 远
能量高低 低→ 高
③核外电子排布的规律了解一些核外电子排布的简单规律对理解原子核外电子排布的情况有很重要的作川,核外电子排布的简单规律主要有:
a.每层上的电子数最多不超过2n2(n为电子层数),如第一电子层上的电子数可能为1,也可能为2,但最多为2。
b.核外电子排布时先排第一层,排满第一层后,再排第二层,依次类推。
c.最外层上的电子数不超过8;当只有一个电子层时,最外层上的电子数不超过2。

原子的不可再分与原子的结构:
化学变化中原子不会由一种原子变成另外一种原子,即化学变化中原了的种类不变,其原因是化学变化中原子核没有发生变化。如硫燃烧生成了二氧化硫,硫和氧气中分别含有硫原子和氧原子,反应后生成的二氧化硫中仍然含硫原子和氧原子。原子不是最小粒子,只是在化学变化的范围内为“最小粒子”,它还可再分,如原子弹爆炸时的核裂变,就是原子发生了变化。原子尽管很小,但具有一定的构成,是由居于原子中心的带正电的原子核和核外带负电的电子构成的。

原子核的构成:

原子核相对原子来说,体积很小,但质量却很大,原子的质量主要集中在原子核上,电子的质量约为质子质量的
 。
。质子的质量为:1.6726×10-27kg
中子的质量为:1.6749×10-27kg
构成原子的粒子间的关系:

对原子构成的正确理解:
(1)原子核位于原子中心,绝大多数由质子和中构成 (有一种氢原子的原子核内只含有1个质子,无中子),体积极小,密度极大,几乎集中了原子的全部质量,核外电子质量很小,可以忽略不计。
(2)每个原子只有一个原子核,核电荷数(核内质子数)的多少,决定了原了的种类。
(3)在原子中:核电荷数二质子数二核外电子数。
(4)原子核内的质子数不一定等干中子数,如钠原子中,质子数为11,中子数为12。
(5)并不是所有的原子中都有中子,如有一种氢原子中就没有中子。
(6)在原子中,由于质子(原子核)与电子所带电荷数相等,且电性相反,因而原子中虽然存在带电的粒子,但原子在整体上不显电性。
核外电子的排布:
①电子层核外电子运动有自己的特点,在含有多个电子的原子里,有的电子通常在离核较近的区域运动,有的电子通常在离核较远的区域运动,科学家形象地将这些区域称为电子层。
②核外电子的分层排布通常用电子层来形象地表示运动着的电子离核远近的不同:离核越近,电子能量越低;离核越远,电子能量越高。电子层数、离核远近、能量高低的关系如下所示:
电子层数 1 2 3 4 5 6 7
离核远近 近→ 远
能量高低 低→ 高
③核外电子排布的规律了解一些核外电子排布的简单规律对理解原子核外电子排布的情况有很重要的作川,核外电子排布的简单规律主要有:
a.每层上的电子数最多不超过2n2(n为电子层数),如第一电子层上的电子数可能为1,也可能为2,但最多为2。
b.核外电子排布时先排第一层,排满第一层后,再排第二层,依次类推。
c.最外层上的电子数不超过8;当只有一个电子层时,最外层上的电子数不超过2。

原子的不可再分与原子的结构:
化学变化中原子不会由一种原子变成另外一种原子,即化学变化中原了的种类不变,其原因是化学变化中原子核没有发生变化。如硫燃烧生成了二氧化硫,硫和氧气中分别含有硫原子和氧原子,反应后生成的二氧化硫中仍然含硫原子和氧原子。原子不是最小粒子,只是在化学变化的范围内为“最小粒子”,它还可再分,如原子弹爆炸时的核裂变,就是原子发生了变化。原子尽管很小,但具有一定的构成,是由居于原子中心的带正电的原子核和核外带负电的电子构成的。
离子的定义:
带电的原子或原子团叫离子。
离子的分类:
阳离子:带正电荷的原子或原子团,如:K+、NH4+
阴离子:带负电荷的原子或原子团,如:Cl-、SO42-。
离子的形成(以Na+、Cl-的形成为例) :
①钠在氯气中燃烧生成氯化钠:2Na+Cl2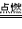 2NaCl。钠与氯气反应时,每个钠原子失去1个电子形成钠离子(Na+),每个氯原子得到1个电子形成氯离子(Cl-),Na+与Cl-由于静电作用而结合成化合物氯化钠(NaCl)
2NaCl。钠与氯气反应时,每个钠原子失去1个电子形成钠离子(Na+),每个氯原子得到1个电子形成氯离子(Cl-),Na+与Cl-由于静电作用而结合成化合物氯化钠(NaCl)

②从原子结构示意图分析Na+,Cl-的形成过程:

离子的表示方法——离子符号
在元素符号的右上角用“+”,“-”号表示离子的电性,数字表示离子所带的电荷,先写数字后写正负号,当数字为1 时,省略不谢。如Na+,Cl-,Mg2+,O2-。
原子团:
①有一些物质如Ca(OH)2,CaCO3等,它们中的一些原子集团如OH-、CO32-,常作为一个整体参加反应,这样的原子集团,叫做原子团,又叫做根。
②命名:原子团不能独立稳定地存在,它是物质 “分子”组成的一部分。
初中化学中的原子团除铵根 (NH4+)在化学式前面部分外,其他原子团在化学式的后一部分一般命名“xx根”,
如下面画线部分为原子团: NH4Cl(铵根)Na2CO3(碳酸根)K2SO4(硫酸根)NaOH(氢氧根)KNO3(硝酸根)KMnO4(高锰酸根)K2MnO4(锰酸根)KClO3(氯酸根) NH4NO3(铵根,硝酸根)
其他原子团有:SO32-(亚硫酸根)、NO2-(亚硝酸根),HSO3-(亚硫酸氢根),H2PO4-(磷酸二氢根)等。
关系式:
阳离子所带正电荷数=原子失去电子数=质子数-核外电子数
阴离子所带负电荷数=原子得到电子数=核外电子数-质子数
带电的原子或原子团叫离子。
离子的分类:
阳离子:带正电荷的原子或原子团,如:K+、NH4+
阴离子:带负电荷的原子或原子团,如:Cl-、SO42-。
离子的形成(以Na+、Cl-的形成为例) :
①钠在氯气中燃烧生成氯化钠:2Na+Cl2
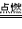 2NaCl。钠与氯气反应时,每个钠原子失去1个电子形成钠离子(Na+),每个氯原子得到1个电子形成氯离子(Cl-),Na+与Cl-由于静电作用而结合成化合物氯化钠(NaCl)
2NaCl。钠与氯气反应时,每个钠原子失去1个电子形成钠离子(Na+),每个氯原子得到1个电子形成氯离子(Cl-),Na+与Cl-由于静电作用而结合成化合物氯化钠(NaCl)
②从原子结构示意图分析Na+,Cl-的形成过程:

离子的表示方法——离子符号
在元素符号的右上角用“+”,“-”号表示离子的电性,数字表示离子所带的电荷,先写数字后写正负号,当数字为1 时,省略不谢。如Na+,Cl-,Mg2+,O2-。
原子团:
①有一些物质如Ca(OH)2,CaCO3等,它们中的一些原子集团如OH-、CO32-,常作为一个整体参加反应,这样的原子集团,叫做原子团,又叫做根。
②命名:原子团不能独立稳定地存在,它是物质 “分子”组成的一部分。
初中化学中的原子团除铵根 (NH4+)在化学式前面部分外,其他原子团在化学式的后一部分一般命名“xx根”,
如下面画线部分为原子团: NH4Cl(铵根)Na2CO3(碳酸根)K2SO4(硫酸根)NaOH(氢氧根)KNO3(硝酸根)KMnO4(高锰酸根)K2MnO4(锰酸根)KClO3(氯酸根) NH4NO3(铵根,硝酸根)
其他原子团有:SO32-(亚硫酸根)、NO2-(亚硝酸根),HSO3-(亚硫酸氢根),H2PO4-(磷酸二氢根)等。
关系式:
阳离子所带正电荷数=原子失去电子数=质子数-核外电子数
阴离子所带负电荷数=原子得到电子数=核外电子数-质子数
概述:
从海水中提取食盐的方法主要是“盐田法”这是一种古老的而至今仍广泛沿用的方法。使用该法。需要在气候温和,光照充足的地区选择大片平坦的海边滩涂,构建盐田。盐田一般分成两部分:蒸发池和结晶池。先将海水引入蒸发池,经日晒蒸发水分到一定程度时,再倒入结晶池,继续日晒,海水就会成为食盐的饱和溶液,再晒就会逐渐析出食盐来。这是得到的晶体就是我们常见的粗盐。剩余的液体称为母液,可从中提取多重化工原料。
海水→蒸发池→结晶池→粗盐和母液
海水“晒”盐:
1. 原理:海水经日晒、风吹等,使溶剂不断减少,溶质的质量分数逐渐增大,
直至形成饱和溶液,继而析出晶体。
2. 过程:先将海水引入蒸发池,经日晒蒸发水分到一定程度时,再引入结晶池,继续日晒,
海水就会成为食盐的饱和溶液,再晒,就会析出食盐来。
这时,得到的晶体就是我们常见的“粗盐”,剩余的液体称为母液(或“苦卤”)。
示意图如下: 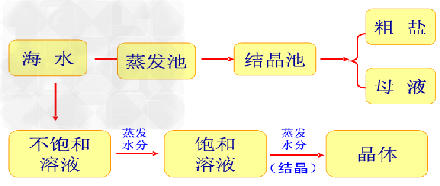
发现相似题
与“氯化钠用途广泛,不但是重要的调味品,又是重要的工业原料....”考查相似的试题有:
- 下列各项比较中,正确的是[ ]A、含碳量:生铁>钢B、熔点:铁<汞C、氢氧化钙的溶解度:80℃>20℃D、核外电子数:钠原子<钠离子
- 下列观点中正确的是( )A.在化学变化中原子的种类和个数都发生改变B.在物理变化中分子的种类和个数都发生改变C.改变物质...
- 下列说法正确的是( )A.原子都是由质子、中子、电了构成的B.决定元素化学性质的主要因素是质子数C.酸与碱共同的都含有氧...
- 已知铁原子的相对原子质量是56,核电荷数是26,则铁原子的核内质子数是______,核外电子数是______,核内中子数是______.
- 钛和钛合金被认为是21世纪的重要金属材料,它们具有熔点高、密度小、抗腐蚀性能好等优良性能,因此被广泛用于火箭、航天飞机...
- 卢瑟福的α粒子轰击金箔实验推翻了汤姆森在1903年提出的原子结构模型,为建立现代原子理论打下了基础.如图线条中,可能是α粒...
- “嫦娥一号”是我国自主研制、成功发射的第一个月球探测器.“嫦娥一号”的发射过程包括火箭发射、入轨、变轨、奔月、绕月等过程...
- 用化学符号填空:(1)2个氧原子_________;(2)正二价的镁元素________.
- 下列符号中,既能表示一种元素,又能表示一种物质,还能表示一个原子的是[ ]A.Cl2B.NC.MgD.S2-
- 下列符号中,不能表示离子的是[ ]A.OH﹣B.SO42﹣C.D.CO32﹣