本试题 “小红同学依据物质类别和物质中某种元素的化合价回忆了初中化学教材中常见的一些物质,并构建了部分物质间的转化关系坐标图,如右图所示(图中“→”表示物质间的...” 主要考查您对物质组成元素的质量分数
物质的变质
物质的推断
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 物质组成元素的质量分数
- 物质的变质
- 物质的推断
定义:
物质中某元素的质量分数,就是该元素的质量与组成物质的各元素总质量之比。
公式:
某元素的质量分数=
如AmBn中A元素的质量分数=
若题目给出物质的化学式,又同时知道物质的实际质量,则可根据物质的质量×某元素的质量分数=该元素的质量,将其中所含元素的质量求出。同理,物质的质量=某元素质量÷该元素的质量分数。
公式的理解:
计算时应先列式计算,然后代入数据算出结果。如水中氢元素的质量分数=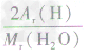 ×100%=
×100%= ×100%=
×100%= ×100%=11.1%而不能写成
×100%=11.1%而不能写成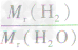 ×100%=
×100%= ×100%=
×100%= ×100%=11.1%
×100%=11.1%
化学式中质量分数的应用:
①已知物质的质量求所含的某元素的质量
利用公式:元素的质量=物质的质量×该元素的质量分数
②已知元素的质量求物质的质量
利用公式:物质的质量=元素的质量÷该元素的质量分数
③根据元素的质量分数确定物质的化学式
利用化学式的变形比较元素质量分数的大小:
例: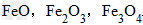 三种铁的氧化物按铁元素的质量分数由大到小排列的顺序为?
三种铁的氧化物按铁元素的质量分数由大到小排列的顺序为?
解析:三种含铁的氧化物的化学式可变形为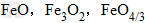 ,则三种含铁的氧化物中铁元素的质量分数分别为:
,则三种含铁的氧化物中铁元素的质量分数分别为: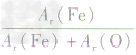 、
、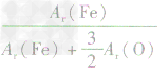 、
、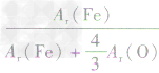 ,通过比较分母可知:
,通过比较分母可知: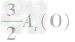 >
>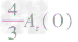 >Ar(O),故铁元素的质量分数由大到小排列的顺序为
>Ar(O),故铁元素的质量分数由大到小排列的顺序为 。
。
物质中某元素的质量分数,就是该元素的质量与组成物质的各元素总质量之比。
公式:
某元素的质量分数=

如AmBn中A元素的质量分数=

若题目给出物质的化学式,又同时知道物质的实际质量,则可根据物质的质量×某元素的质量分数=该元素的质量,将其中所含元素的质量求出。同理,物质的质量=某元素质量÷该元素的质量分数。
公式的理解:
计算时应先列式计算,然后代入数据算出结果。如水中氢元素的质量分数=
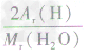 ×100%=
×100%= ×100%=
×100%= ×100%=11.1%而不能写成
×100%=11.1%而不能写成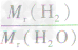 ×100%=
×100%= ×100%=
×100%= ×100%=11.1%
×100%=11.1%化学式中质量分数的应用:
①已知物质的质量求所含的某元素的质量
利用公式:元素的质量=物质的质量×该元素的质量分数
②已知元素的质量求物质的质量
利用公式:物质的质量=元素的质量÷该元素的质量分数
③根据元素的质量分数确定物质的化学式
利用化学式的变形比较元素质量分数的大小:
例:
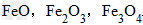 三种铁的氧化物按铁元素的质量分数由大到小排列的顺序为?
三种铁的氧化物按铁元素的质量分数由大到小排列的顺序为?解析:三种含铁的氧化物的化学式可变形为
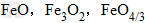 ,则三种含铁的氧化物中铁元素的质量分数分别为:
,则三种含铁的氧化物中铁元素的质量分数分别为: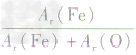 、
、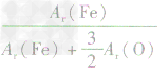 、
、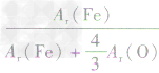 ,通过比较分母可知:
,通过比较分母可知: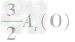 >
>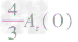 >Ar(O),故铁元素的质量分数由大到小排列的顺序为
>Ar(O),故铁元素的质量分数由大到小排列的顺序为 。
。易变质的物质:
1. 由于吸水质量增加的物质:氢氧化钠固体,浓硫酸
2. 由于跟水反应质量增加的物质:氧化钙,氧化钠,硫酸铜
3. 由于和二氧化碳反应质量增加的物质:氢氧化钠,氢氧化钾,氢氧化钙
4. 由于挥发质量减少的物质:浓盐酸,浓硝酸,酒精,氨水
5. 由于风化质量减少的物质:碳酸钠晶体
氢氧化钠变质的知识归纳:
氢氧化钠变质主要考点包括:变质原因、检验变质的方法、检验变质的程度、 除去杂质得到就纯净的氢氧化钠。
1 、氢氧化钠变质的原因:
敞口放置, 与空气中的二氧化碳反应, 生成了碳酸钠。 2NaOH+CO 2 =Na 2 CO 3 +H 2 O
2 、检验氢氧化钠是否变质的方法: ( 分别滴加酸、碱、盐溶液,各为一种方法 )
①取少量样品于试管中, 滴加稀盐酸 ( 或者稀硫酸 ) , 如果产生气泡, 说明已变质。 Na 2 CO 3 +2HCl=2NaCl+H 2 O+CO 2 ↑
②取少量样品于试管中,滴加氢氧化钙溶液 ( 或者氢氧化钡溶液 ) ,如果产生白色 沉淀,说明已变质。 Na 2 CO 3 +Ca(OH) 2 =CaCO 3 ↓ +2NaOH
③取少量样品于试管中,滴加氯化钙溶液 ( 或者硝酸钙等其它可溶性钙盐、钡盐 溶液 ) Na 2 CO 3 +CaCl 2 =CaCO 3 ↓ +2NaCl
3 、检验氢氧化钠变质程度的方法:
取少量样品于试管中,滴加足量的 CaCl2 溶液,有白色沉淀生成;静置,像上层澄清液中滴加少量酚酞溶液,如果溶液变红色,说明溶液部分变质;如果溶液呈无色,说明氢氧化钠完全变质。
解释:碳酸钠溶液呈碱性,它的存在会影响到氢氧化钠的检验,所以在检验氢氧化钠前必须把碳酸钠除去。除去碳酸钠时不能用酸,因为酸会与氢氧化钠反应; 不能用碱,因为碱会与碳酸钠反应生成氢氧化钠,干扰原来氢氧化钠的检验。
4 、如何除去部分变质的氢氧化钠中的碳酸钠。 滴加适量氢氧化钙溶液至刚好无沉淀生成为止,然后过滤,就得到氢氧化钠溶液,再蒸发,就得到氢氧化钠固体。 Na 2 CO 3 +Ca(OH) 2 =CaCO 3 ↓ +2NaOH
除杂方法:除杂时为了不引入新杂质,如果除去阴离子,所选择试剂的阴离子 与主题物质一致。
氧化钙和氢氧化钙的变质:
(1)变质的原因
氧化钙在空气中敞口放置会与空气中的水蒸气反应生成氢氧化钙 CaO+H 2 O===Ca(OH) 2 , 氢氧化钙继续与空气中的二氧化碳反应生成碳酸钙。 Ca(OH) 2 +CO 2 ====CaCO 3 ↓+H 2 O
(2)检验变质后物质存在的方法:
氧化钙:
取少量变质后的固体放入烧杯中,加入水充分溶解,用手摸烧杯外壁有灼热感。
氢氧化钙:
(1)取变质后物质溶于水,向其中通入二氧化碳气体,有白色沉淀生成。
(2)取变质后物质溶于水,向其中滴加碳酸钠溶液,有白色沉淀生成。 碳酸钙:取少量变质后固体,向其中滴加稀盐酸,有气泡冒出。 CaCO3 +2HCl===CaCl2 +H2O+CO2 ↑
【特殊强调】:有氧化钙存在的情况下,初中阶段检验不出氢氧化钙的存在。因为氧化钙溶于水后会生成氢氧化钙,会干扰原来氢氧化钙的检验。
其它常见物质变质的知识小结:
NaOH在空气中变质:2NaOH+CO2==Na2CO3+H2O
检验: 取样滴加稀 HCl,若有气泡产生,则已经变质 (Na 2 CO 3 +2HCl===2NaCl+H 2 O+CO 2 ↑ )
消石灰 [Ca(OH)2] 放在空气中变质: Ca(OH) 2 +CO 2 ====CaCO 3 ↓ +H 2 O
检验: 取样滴加稀 HCl,若有气泡产生,则已经变质 (CaCO 3 +2HCl===CaCl 2 +H 2 O+CO 2 ↑ )
生石灰 (CaO) 暴露在空气中变质: CaO+H 2 O===Ca(OH) 2
检验: 取样用试管加热,若试管内壁有小水珠产生,则已变质 [Ca(OH) 2 = 加热 =CaO+H 2 O]
铁生锈:4Fe+3O 2 ===2Fe2O3
检验:观察颜色 , 若有红色粉末在表面, 则已变质
铜生锈:2Cu+O 2 +CO 2 +H 2 O===Cu 2 (OH) 2 CO 3
检验:观察颜色 , 若有绿色粉末在表面,则已变质。
1. 由于吸水质量增加的物质:氢氧化钠固体,浓硫酸
2. 由于跟水反应质量增加的物质:氧化钙,氧化钠,硫酸铜
3. 由于和二氧化碳反应质量增加的物质:氢氧化钠,氢氧化钾,氢氧化钙
4. 由于挥发质量减少的物质:浓盐酸,浓硝酸,酒精,氨水
5. 由于风化质量减少的物质:碳酸钠晶体
氢氧化钠变质的知识归纳:
氢氧化钠变质主要考点包括:变质原因、检验变质的方法、检验变质的程度、 除去杂质得到就纯净的氢氧化钠。
1 、氢氧化钠变质的原因:
敞口放置, 与空气中的二氧化碳反应, 生成了碳酸钠。 2NaOH+CO 2 =Na 2 CO 3 +H 2 O
2 、检验氢氧化钠是否变质的方法: ( 分别滴加酸、碱、盐溶液,各为一种方法 )
①取少量样品于试管中, 滴加稀盐酸 ( 或者稀硫酸 ) , 如果产生气泡, 说明已变质。 Na 2 CO 3 +2HCl=2NaCl+H 2 O+CO 2 ↑
②取少量样品于试管中,滴加氢氧化钙溶液 ( 或者氢氧化钡溶液 ) ,如果产生白色 沉淀,说明已变质。 Na 2 CO 3 +Ca(OH) 2 =CaCO 3 ↓ +2NaOH
③取少量样品于试管中,滴加氯化钙溶液 ( 或者硝酸钙等其它可溶性钙盐、钡盐 溶液 ) Na 2 CO 3 +CaCl 2 =CaCO 3 ↓ +2NaCl
3 、检验氢氧化钠变质程度的方法:
取少量样品于试管中,滴加足量的 CaCl2 溶液,有白色沉淀生成;静置,像上层澄清液中滴加少量酚酞溶液,如果溶液变红色,说明溶液部分变质;如果溶液呈无色,说明氢氧化钠完全变质。
解释:碳酸钠溶液呈碱性,它的存在会影响到氢氧化钠的检验,所以在检验氢氧化钠前必须把碳酸钠除去。除去碳酸钠时不能用酸,因为酸会与氢氧化钠反应; 不能用碱,因为碱会与碳酸钠反应生成氢氧化钠,干扰原来氢氧化钠的检验。
4 、如何除去部分变质的氢氧化钠中的碳酸钠。 滴加适量氢氧化钙溶液至刚好无沉淀生成为止,然后过滤,就得到氢氧化钠溶液,再蒸发,就得到氢氧化钠固体。 Na 2 CO 3 +Ca(OH) 2 =CaCO 3 ↓ +2NaOH
除杂方法:除杂时为了不引入新杂质,如果除去阴离子,所选择试剂的阴离子 与主题物质一致。
氧化钙和氢氧化钙的变质:
(1)变质的原因
氧化钙在空气中敞口放置会与空气中的水蒸气反应生成氢氧化钙 CaO+H 2 O===Ca(OH) 2 , 氢氧化钙继续与空气中的二氧化碳反应生成碳酸钙。 Ca(OH) 2 +CO 2 ====CaCO 3 ↓+H 2 O
(2)检验变质后物质存在的方法:
氧化钙:
取少量变质后的固体放入烧杯中,加入水充分溶解,用手摸烧杯外壁有灼热感。
氢氧化钙:
(1)取变质后物质溶于水,向其中通入二氧化碳气体,有白色沉淀生成。
(2)取变质后物质溶于水,向其中滴加碳酸钠溶液,有白色沉淀生成。 碳酸钙:取少量变质后固体,向其中滴加稀盐酸,有气泡冒出。 CaCO3 +2HCl===CaCl2 +H2O+CO2 ↑
【特殊强调】:有氧化钙存在的情况下,初中阶段检验不出氢氧化钙的存在。因为氧化钙溶于水后会生成氢氧化钙,会干扰原来氢氧化钙的检验。
其它常见物质变质的知识小结:
NaOH在空气中变质:2NaOH+CO2==Na2CO3+H2O
检验: 取样滴加稀 HCl,若有气泡产生,则已经变质 (Na 2 CO 3 +2HCl===2NaCl+H 2 O+CO 2 ↑ )
消石灰 [Ca(OH)2] 放在空气中变质: Ca(OH) 2 +CO 2 ====CaCO 3 ↓ +H 2 O
检验: 取样滴加稀 HCl,若有气泡产生,则已经变质 (CaCO 3 +2HCl===CaCl 2 +H 2 O+CO 2 ↑ )
生石灰 (CaO) 暴露在空气中变质: CaO+H 2 O===Ca(OH) 2
检验: 取样用试管加热,若试管内壁有小水珠产生,则已变质 [Ca(OH) 2 = 加热 =CaO+H 2 O]
铁生锈:4Fe+3O 2 ===2Fe2O3
检验:观察颜色 , 若有红色粉末在表面, 则已变质
铜生锈:2Cu+O 2 +CO 2 +H 2 O===Cu 2 (OH) 2 CO 3
检验:观察颜色 , 若有绿色粉末在表面,则已变质。
概念:
物质的推断就是运用物质的特殊性质和特征反应.根据实验现象得出正确的结论。同一推断题可能存在多个突破点,可以从不同角度或不同种方法寻找解题突破口,同叫检验推断结果,保证答案的准确性。推断题题型具备考查知识面广、综合性强、题型多变、思维容量大等特点。要解好此类题口,要求大家要有扎实的元素化合物的基础知识和实验技能,还必须具备科学、严密的思维方法和良好的分析问题、解决问题的能力。
常见物质的颜色:
多数气体为无色,多数固体化合物为白色,多数溶液为无色。
黑色固体:MnO2、CuO、Fe3O4、C粉、铁粉(Fe)活性炭
蓝色固体:CuSO4·5H2O(胆矾)、Cu(OH)2(氢氧化铜)、CuCO3(碳酸铜)
红色固体:Cu(紫红色)、Fe2O3(红棕色)、红磷:P(暗红色)、Fe(OH)3(红褐色)I2碘(紫红色)
黄色固体:硫磺(单质S)
绿色固体:碱式碳酸铜(铜绿)[Cu2(OH)2CO3]
蓝色溶液:含Cu2+溶液:CuSO4(硫酸铜溶液)、CuCl2(氯化铜溶液)Cu(NO3)2(硝酸铜溶液)
黄色溶液:含Fe3+的溶液(棕黄色):FeCl3(氯化铁溶液)、Fe2(SO4)3(硫酸铁溶液)Fe(NO3)3(硝酸铁溶液)
浅绿色溶液:含Fe2+的溶液:FeCl2(氯化亚铁)FeSO4(硫酸亚铁)Fe(NO3)2(硝酸亚铁)
其他溶液:石蕊试液(紫色)、高锰酸钾溶液(紫红色)
无色气体:N2、CO2、CO、O2、H2、CH4
有色气体:Cl2(黄绿色)、NO2(红棕色)
有刺激性气味的气体:NH3(此气体可使湿润的红色石蕊试纸变蓝色)、SO2、HCl(氯化氢)
有臭鸡蛋气味:H2S硫化氢
气体的特征:
①有刺激性气味的气体:HCl、SO2、NH3
②有颜色的气体:Cl2(黄绿色)、NO2(红棕色)
③无色无味的气体:O2、H2、N2、CO、CO2。
特征反应:
推断题的解题步骤及突破口的选择:
1.解题步骤
(1)审题:认真审读原题,弄清文意和图意,理出题给条件,深挖细找.反复推敲。
(2)分析:抓住关键,找准解题的突破口,突破口也称为“题眼”,指的是关键词、特殊现象、物质的特征等等.然后从突破口出发,探求知识间的内在联系,应用多种思维方式,进行严密的分析和逻辑推理,推出符合题意的结果,
(3)解答:根据题目的要求,按照分析和推理的结果,认真而全面地解答。
(4)检验:得出结论后切勿忘记验证。其方法是将所得答案放回原题中检验,若完全符合,则说明答案正确。若出现不符,则说明答案有误,需要另行思考,推出正确答案。
2.突破口的选择
(1)颜色特征:根据物质的特殊颜色进行判断。包括常见固体、沉淀、溶液、火焰的颜色。
(2)反应特征
(3)物质状态特征
常见固体单质:Fe、Cu、C,S,P;气体单质:H2、O2、 N2;气体化合物:CO、CO2、CH4、SO2;常温下呈液态的物质:H2O、H2O2、酒精、H2SO4.
(4)反应条件特征
点燃:有O2参加的反应;通电:H2O的电解;MnO2 作催化剂:KClO3分解制O2、H2O2分解制O2;高温: CaCO3分解、C还原CuO、炼铁;加热:KClO3、KMnO4、 Cu2(OH)2CO3的受热分解。
(5)以三角关系为突破口

(6)以物质特征现象为突破口
①能使澄清石灰水变浑浊的无色无味气体是CO2。
②能使黑色CuO变红(或红色Fe2O3变黑)的气体是H2或CO,同体是C。
③能使燃烧着的小条正常燃烧的气体是空气,燃烧得更旺的气体是O2,熄灭的气体是CO2或N2;能使带火星的木条复燃的气体是O2.
④能使白色无水CuSO4。粉末变蓝的气体是水蒸气。
⑤在O2中燃烧火星四射的物质是Fe。
⑥在空气中燃烧生成CO2和H2O的物质是有机物,如CH4、C2H5OH等。
⑦能溶于盐酸或稀HNO3的白色沉淀有CaCO3、 BaCO3;不溶于稀HNO3的白色沉淀有AgCl、BaSO4。
(7)以元素或物质之最为突破口 ①地壳中含量最多的元素是O,含量最多的金属元素是Al。
②人体中含量最多的元素是O2。
③空气中含量最多的元素是N。
④形成化合物最多的元素是C。
⑤质子数最少的元素是H。
⑥相对分子质量最小、密度也最小的气体是H2.
⑦相对分子质量最小的氧化物是H2。
⑧自然界中硬度最大的物质是金刚石。
⑨空气中含量最多的气体是N2。
⑩最简单的有机物是CH4。
 最常用的溶剂是H2O。
最常用的溶剂是H2O。
 人体中含量最多的物质是H2O。
人体中含量最多的物质是H2O。
(8)以特定的实验结果为突破口
物质的推断就是运用物质的特殊性质和特征反应.根据实验现象得出正确的结论。同一推断题可能存在多个突破点,可以从不同角度或不同种方法寻找解题突破口,同叫检验推断结果,保证答案的准确性。推断题题型具备考查知识面广、综合性强、题型多变、思维容量大等特点。要解好此类题口,要求大家要有扎实的元素化合物的基础知识和实验技能,还必须具备科学、严密的思维方法和良好的分析问题、解决问题的能力。
常见物质的颜色:
多数气体为无色,多数固体化合物为白色,多数溶液为无色。
黑色固体:MnO2、CuO、Fe3O4、C粉、铁粉(Fe)活性炭
蓝色固体:CuSO4·5H2O(胆矾)、Cu(OH)2(氢氧化铜)、CuCO3(碳酸铜)
红色固体:Cu(紫红色)、Fe2O3(红棕色)、红磷:P(暗红色)、Fe(OH)3(红褐色)I2碘(紫红色)
黄色固体:硫磺(单质S)
绿色固体:碱式碳酸铜(铜绿)[Cu2(OH)2CO3]
蓝色溶液:含Cu2+溶液:CuSO4(硫酸铜溶液)、CuCl2(氯化铜溶液)Cu(NO3)2(硝酸铜溶液)
黄色溶液:含Fe3+的溶液(棕黄色):FeCl3(氯化铁溶液)、Fe2(SO4)3(硫酸铁溶液)Fe(NO3)3(硝酸铁溶液)
浅绿色溶液:含Fe2+的溶液:FeCl2(氯化亚铁)FeSO4(硫酸亚铁)Fe(NO3)2(硝酸亚铁)
其他溶液:石蕊试液(紫色)、高锰酸钾溶液(紫红色)
无色气体:N2、CO2、CO、O2、H2、CH4
有色气体:Cl2(黄绿色)、NO2(红棕色)
有刺激性气味的气体:NH3(此气体可使湿润的红色石蕊试纸变蓝色)、SO2、HCl(氯化氢)
有臭鸡蛋气味:H2S硫化氢
气体的特征:
①有刺激性气味的气体:HCl、SO2、NH3
②有颜色的气体:Cl2(黄绿色)、NO2(红棕色)
③无色无味的气体:O2、H2、N2、CO、CO2。
特征反应:
| 特征反应 | 常见反应 |
| 在催化剂作用下发生的反应 | 双氧水或氯酸钾分解 |
| 通电发生的反应 | 电解水 |
| 产生大量白烟的燃烧 | 磷燃烧 |
| 发出耀眼白光的燃烧 | 镁带在空气中燃烧,铝箔在O2中燃烧 |
| 产生明亮蓝紫色火焰并生成有刺激性气味气体的燃烧 | 硫在氧气中燃烧 |
| 产生淡蓝色火焰且罩在火焰上方的小烧杯内壁有水珠出现 | 氢气在空气中燃烧 |
| 产生蓝色火焰的燃烧 | CO和CH4在空气中燃烧 |
| 有火星四射的燃烧 | 铁在氧气中燃烧 |
| 生成蓝色沉淀的反应 | 可溶性碱+可溶性铜盐 |
| 生成红褐色沉淀的反应 | 可溶性碱+可溶性铁盐 |
| 溶液加酸放出CO2气体 | 碳酸盐(或碳酸氢盐)+酸 |
| 固体加酸放出气体 | 氢前金属或碳酸盐+酸 |
推断题的解题步骤及突破口的选择:
1.解题步骤
(1)审题:认真审读原题,弄清文意和图意,理出题给条件,深挖细找.反复推敲。
(2)分析:抓住关键,找准解题的突破口,突破口也称为“题眼”,指的是关键词、特殊现象、物质的特征等等.然后从突破口出发,探求知识间的内在联系,应用多种思维方式,进行严密的分析和逻辑推理,推出符合题意的结果,
(3)解答:根据题目的要求,按照分析和推理的结果,认真而全面地解答。
(4)检验:得出结论后切勿忘记验证。其方法是将所得答案放回原题中检验,若完全符合,则说明答案正确。若出现不符,则说明答案有误,需要另行思考,推出正确答案。
2.突破口的选择
(1)颜色特征:根据物质的特殊颜色进行判断。包括常见固体、沉淀、溶液、火焰的颜色。
(2)反应特征
(3)物质状态特征
常见固体单质:Fe、Cu、C,S,P;气体单质:H2、O2、 N2;气体化合物:CO、CO2、CH4、SO2;常温下呈液态的物质:H2O、H2O2、酒精、H2SO4.
(4)反应条件特征
点燃:有O2参加的反应;通电:H2O的电解;MnO2 作催化剂:KClO3分解制O2、H2O2分解制O2;高温: CaCO3分解、C还原CuO、炼铁;加热:KClO3、KMnO4、 Cu2(OH)2CO3的受热分解。
(5)以三角关系为突破口

(6)以物质特征现象为突破口
①能使澄清石灰水变浑浊的无色无味气体是CO2。
②能使黑色CuO变红(或红色Fe2O3变黑)的气体是H2或CO,同体是C。
③能使燃烧着的小条正常燃烧的气体是空气,燃烧得更旺的气体是O2,熄灭的气体是CO2或N2;能使带火星的木条复燃的气体是O2.
④能使白色无水CuSO4。粉末变蓝的气体是水蒸气。
⑤在O2中燃烧火星四射的物质是Fe。
⑥在空气中燃烧生成CO2和H2O的物质是有机物,如CH4、C2H5OH等。
⑦能溶于盐酸或稀HNO3的白色沉淀有CaCO3、 BaCO3;不溶于稀HNO3的白色沉淀有AgCl、BaSO4。
(7)以元素或物质之最为突破口 ①地壳中含量最多的元素是O,含量最多的金属元素是Al。
②人体中含量最多的元素是O2。
③空气中含量最多的元素是N。
④形成化合物最多的元素是C。
⑤质子数最少的元素是H。
⑥相对分子质量最小、密度也最小的气体是H2.
⑦相对分子质量最小的氧化物是H2。
⑧自然界中硬度最大的物质是金刚石。
⑨空气中含量最多的气体是N2。
⑩最简单的有机物是CH4。
 最常用的溶剂是H2O。
最常用的溶剂是H2O。  人体中含量最多的物质是H2O。
人体中含量最多的物质是H2O。(8)以特定的实验结果为突破口
| 实验结果 | 可能情况分析 |
| 固体混合物加水后出现不溶物 | a.源混合物中有不溶物.如CaCO、、 Al(OH)3等 b.混合物中物质反应生成沉淀,如 Na2SO4和BaCl2、Na2CO3和Ca(OH)2等 |
| 向固体混合物中加水得到无色溶液 | 混合物中一定不含含Fe2+、Fe3+ 、Cu2+、MnO4- |
| 生成有色沉淀 | a.生成红褐色Fe(OH)3,是Fe3+的盐与碱溶液反应,如FeCl3+3NaOH== Fe(OH)3↓+3NaCl b.生成蓝色沉淀.是Cu2+的盐与碱溶液反应,如2NaOH+CuSO4==Cu(OH)2↓ +Na2SO4 |
| 常见沉淀的性质 ①既不溶于水义不溶于酸 ②能溶于酸但不生成气体 ③能溶于酸且生成气体 ④加足量酸沉淀部分溶解 |
①如BaSO4和AgCl ②不溶的碱,如Mg(OH)2 ③不溶的碳酸盐,如CaCO3 ④沉淀为混合物,既含BaSO4或AgCl中的至少一种,又含有CaCO3、Mg(OH)2等不溶物 |
发现相似题
与“小红同学依据物质类别和物质中某种元素的化合价回忆了初中化...”考查相似的试题有:
- (6分)食品保鲜可以防止食品腐坏,保持食品的营养和味道。食品保鲜的措施有添加防腐剂、充填气体、放置干燥剂和脱氧保鲜剂等...
- (2分)化学家TimRichard将分子结构图像小狗的某有机物取名叫“doggycene”,其分子式为C26H26,计算:(1)该分子中碳元素和氢...
- “三聚氰胺牛奶、苏丹红咸蛋、廋肉精猪肉、牛肉膏、染色馒头、墨汁薯粉、地沟油…”中国的食品安全问题已成为众多媒体关注的焦点...
- 2009年2月某市发生的“瘦肉精”中毒事件造成几十人住院治疗.“瘦肉精”(化学式为C12H19Cl3N2O)能提高猪的瘦肉率,但对人体有危...
- 从化学实验现象中可以推断物质的性质,如从酸与碱的实验中就能找出一些实例:例:在实验中不慎将盐酸撒到试剂标签上,不久试...
- 老师整理药品时,意外发现实验桌上有瓶敞口放置的NaOH溶液,他让同学们对这瓶NaOH溶液进行探究.【提出问题】这瓶NaOH溶液是...
- 根据下图所示的转化关系,推断物质X可能是[ ]A.CuOB.Cu(OH)2C.Na2CO3D.Fe2O3
- A、B、C、D、E、F、G六种物质.A与C是无色气体(化合物);B与D均是黑色粉末.相互间能发生如图反应:请回答:(1)化学式:A...
- 下列各组溶液,不用其它试剂就无法鉴别的是( )A.CuSO4KCl KOH BaCl2B.NaOH FeCl3KCl H2SO4C.KOH NaNO3Na2SO4Ba(NO3)2D...
- B、G是工业上分别以大理石和赤铁矿为原料制得的一种主要产品,其转化关系如图所示.已知D是一种单质.试回答下列问题:(1)...