本试题 “某学生设计如图所示实验装置利用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应,反应后温度将升高),A中盛浓盐酸,C中盛潮湿的消石灰,据此回答...” 主要考查您对氯气
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 氯气
氯气:
①化学式:Cl2
②氯元素在周期表中的位置:第三周期ⅦA族
③氯原子的电子式: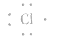
④氯的原子结构示意图: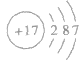
⑤氯原子的外围电子排布式:
⑥化学键类型:非极性共价键
⑦氯分子的电子式:
⑧氯分子的结构式:
氯气的物理性质和化学性质:
(1)物理性质:黄绿色,有刺激性气味,有毒,密度比空气大,能溶于水(1:2)。
(2)化学性质:氯气(Cl2)是双原子分子,原子的最外层有七个电子,是典型的非金属元素,单质是强氧化剂。
①氯气与金属反应: 2Na+Cl2
 2NaCl(反应剧烈,产生大量白烟) 2Fe+3Cl2
2NaCl(反应剧烈,产生大量白烟) 2Fe+3Cl2 2FeCl3(反应剧烈,产生大量棕褐色烟,溶于水成黄色溶液) Cu+Cl2
2FeCl3(反应剧烈,产生大量棕褐色烟,溶于水成黄色溶液) Cu+Cl2 CuCl2(反应剧烈,产生大量棕色的烟,溶于水成蓝色或绿色溶液)氯气能与绝大数金属都能发生反应,表明氯气是一种活泼的非金属单质。
CuCl2(反应剧烈,产生大量棕色的烟,溶于水成蓝色或绿色溶液)氯气能与绝大数金属都能发生反应,表明氯气是一种活泼的非金属单质。 ②与非金属的反应 H2+Cl2
 2HCl(纯净的氢气在氯气中安静的燃烧,芒白色火焰,在瓶口处有白雾产生)H2+Cl2
2HCl(纯净的氢气在氯气中安静的燃烧,芒白色火焰,在瓶口处有白雾产生)H2+Cl2 2HCl(发生爆炸) 2P+3Cl2
2HCl(发生爆炸) 2P+3Cl2 2PCl3(液态) PCl3+Cl2==PCl5(固态)磷在氯气中剧烈燃烧,产生大量的烟、雾。雾是PCl3,烟是PCl5。氯气能有很多非金属单质反应,如S、C、Si等。
2PCl3(液态) PCl3+Cl2==PCl5(固态)磷在氯气中剧烈燃烧,产生大量的烟、雾。雾是PCl3,烟是PCl5。氯气能有很多非金属单质反应,如S、C、Si等。 ③与碱反应 Cl2+2NaOH==NaCl+NaClO+H2O 2Cl2+2Ca(OH)2==CaCl2+Ca(ClO)2+2H2O
④与某些还原性物质反应:Cl2+2FeCl2===2FeCl3 Cl2+SO2+2H2O==2HCl+H2SO4
⑤有机反应(参与有机反应的取代和加成反应)
CH4+Cl2→CH3Cl+HCl
CH3Cl+Cl2→CH2Cl2+HCl
CH2Cl2+Cl2→CHCl3+HCl
CHCl3+Cl2→CCl4+HCl
Cl2+CH2=CH2→CH2Cl-CH2Cl(加成反应)
⑥与水反应 Cl2+H2O
 HCl+HClO
HCl+HClO 发现相似题
与“某学生设计如图所示实验装置利用氯气与潮湿的消石灰反应制取...”考查相似的试题有:
- A~D为短周期元素,其性质或结构信息如下表所示请根据表中信息回答下列问题:(1)A元素在元素周期表中的位置是___________,能...
- 下列叙述Ⅰ和Ⅱ均正确并且有因果关系的是( )选项叙述I叙述ⅡA氯气具有强还原性可用于自来水的消毒杀菌BSiO2导电能力强可用于制...
- 下列变化过程不能直接实现的是( )①HCl ②Cl2 ③Ca(ClO)2 ④HClO ⑤CO2A.①→②B.②→③C.③→④D.④→⑤
- 将新制氯水分别滴加到下列溶液中至过量,对所观察到的现象描述合理的一组是( ) AgNO3溶液加有酚酞的NaOH溶液石蕊溶液品红溶...
- Ⅰ 下图所示A-H为实验室常见的仪器、装置(部分固定夹持装置略去),请根据要求回答下列问题。(1)A仪器的名称是____________...
- (1)(6分)卤素元素包括______、______、______ 、______(填元素符号),随核电荷数递增,它们的原子半径依次_______,单...
- 某化学活动小组设计如图所示装置(部分夹持装置 已略去)实验,以探究潮湿的Cl2与Na2CO3反应的产物。(1)写出装置A中发生反应...
- 氯的含氧酸根离子有ClO-、ClO2-、ClO3-、ClO4-等,关于它们的说法正确的是A.ClO-中Cl-显+1价B.ClO2-的空间构型为直...
- 某同学用下列装置制备并检验Cl2的性质。下列说法正确的是A.实验室制氯气中除去尾气用澄清石灰水B.吸收了氯气的NaOH溶液中滴...
- 生活中难免会遇到一些突发事件,我们要善于利用学过的知识,采取科学、有效的方法保护自己。如果发生了氯气泄漏,以下自救方...