本试题 “下列说法正确的是( )A.由不同种元素组成的物质一定是化合物B.由同种元素组成的物质一定是纯净物C.分子是保持物质性质的一种微粒D.原子是化学变化中的最...” 主要考查您对灭火的原理和方法
分子的定义
分子的特点
单质和化合物
纯净物和混合物
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 灭火的原理和方法
- 分子的定义
- 分子的特点
- 单质和化合物
- 纯净物和混合物
破坏燃烧的条件,即可达到灭火的目。
①清除可燃物或使可燃物与其他物品隔离;②隔绝氧气(或空气);③使可燃物的温度降到着火点以下。破坏燃烧的三个条件中任何一个即可达到灭火的目的。
灭火原理的实验探究:
| 实验方案 | 现象 | 分析 |
点燃三支蜡烛,在其中一支蜡烛上扣一只烧杯.将另两支蜡烛放在烧杯中,然后向其中只烧杯中加适量碳酸钠和稀盐酸如下图: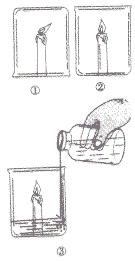 |
①在倒扣烧杯中的蜡烛熄灭 ②正放在烧杯中的蜡烛正常燃烧 ③加入适量碳酸钠和稀盐酸的烧杯中的蜡烛很快熄灭 |
①在倒扣烧杯中的蜡烛因钮气不足而熄灭 ②正放存烧杯中的蜡烛与氧气接触,温度保持在蜡烛的着火点以上,因此能正常燃烧 ⑧稀盐酸与碳酸钠迅速反应产生大量的二氧化碳气体,二氧化碳既不燃烧也不支持燃烧,所以蜡烛很快熄灭。 |
灭火方法:
①将可燃物撤离燃烧区.与火源隔离.如液化气、煤气起火,首先要及时关闭阀门,以断绝可燃物的来源;扑灭森林火灾,可用设置隔离带的方法使森林中的树木与可燃烧区隔离
②将燃着的可燃物与空气隔离,如厨房油锅起火,盖上锅盖就能灭火;二氧化碳灭火器能火火的原因之一是灭火器喷出的大量二氧化碳在燃烧物表面形成一层二氧化碳气体层,使燃烧物与在空气隔绝,达到灭火的目的
③用大量的冷却剂(如水、干冰等)冷却可燃物,使温度降低到可燃物的着火点以下,如建筑物起火时,用高压水枪灭火等。
易错点:
灭火时降低温度不是降低着火点,着火点是物质的固有属性,一般情况下不能改变。
几种常见灭火器的灭火原理和适用范围:
| 灭火器 | 灭火原理 | 适用范围 |
| 泡沫灭火器 | 灭火时.能喷射出大量二氧化碳及泡沫,它们能黏附在可燃物上,使可燃物与空气隔绝,达到灭火的目的 | 可用来扑灭木材、棉布等燃烧引起的灭火 |
| 利用压缩的二氧化碳吹出干粉(主要含有碳酸氧钠)来灭火 | 具有流动性好,喷射率高、不腐蚀容器和不易变质等优良性能,除可用来扑灭一般失火外,还可用来扑灭油、气等燃烧引起的失火 | |
| 在加压时将液态二氧化碳压缩在小钢瓶中,灭火时再将其喷出,有降温和隔绝空气的作用 | 火火时不会因留下任何痕迹而使物体损坏.因此可用来扑灭图书、档案、贵重设备、精密仪器等处的失火.使用时,手一定要先握在钢瓶的木柄上,否则.会把手冻伤。 |
泡沫灭火器的灭火原理:
1. 泡沫灭火器的灭火原理:
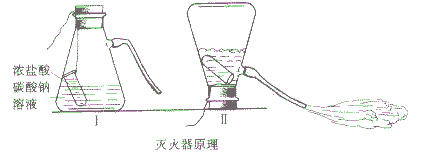
现象:当把吸滤瓶倒置后,浓HCl与Na2CO3溶液剧烈反应,产生大量CO2气体夹带着水从导管喷出。
方程式:Na2CO3+HCl==2NaCl+H2O+CO2↑(泡沫灭火原理)
2. 实际使用的泡沫灭火器,常用硫酸铝来代替盐酸(或硫酸),用碳酸氢钠来代替碳酸钠,为了产生泡沫,常放入甘草或皂角等原来制取液体。把泡沫灭火器倒转时,两种药液相互混合,发生如下反应:Al2(SO4)2+6NaHCO3==3Na2SO4+2Al(OH)3↓+6CO2↑
大量的二氧化碳跟发泡剂形成泡沫,从喷嘴中喷射出来,覆盖在燃烧物上,使燃烧物隔绝空气和降低温度,达到灭火的目的。但是,因为泡沫中含有水分,不宜用于扑救遇水发生燃烧或爆炸的物质(如钾、钠、电石等)引起的火灾;对于电器火灾,要在切断电源后才能使用泡沫灭火器。
由分子构成的物质:
物质是由粒子构成的,构成物质的粒子有多种,分子是其中的一种。世界上许多物质是由分子构成的,分子可以构成单质,也可以构成化合物。如:氧气、氢气、C60等单质是由分子构成的;水、二氧化碳等化合物也是由分子构成的。
分子的定义:
分子是保持物质化学性质的最小粒子。
概念的理解:
①分子是保持物质化学性质的“最小粒子”、不是“唯一粒子”。
②“保持”的含义是指构成该物质的每一个分子与该物质的化学性质是一致的。
③分子只能保持物质的化学物质,而物质的物理性质(如:颜色、状态等)需要大量的集合体一起来共同体现,单个分子无法体现物质的物理性质。
④“最小”不是绝对意义上的最小,而是”保持物质化学性质的最小”。如果不是在“保持物质化学性质” 这层含义上,分子还可以分成更小的粒子。
用分子的观点解释问题:
物理变化和化学变化的区别
由分子构成的物质,发生物理变化时分子本身未变,分子的运动状态、分子间的间隔发生了改变;发生化学变化时分子本身发生了变化,分子分成原子,原子重新组合变成了共他物质的分子。如:水变成水蒸气,水分子本身没有变,只是分子间的问隔变大,这是物理变化;水通直流电.水分子发生了变化,生成了氢原子和氧原子,氢.原子构成氢分子,氧原子构成氧分子,这是化学变化。
分子的表示方法:
分子可用化学式表示:如O:既可表示氧气,也可表示1个氧分子。
分子的构成:

分子的基本性质:
(1)分子的体积和质量都很小,如1个水分子的质量约为3×1026kg,1滴水中大约有1.67×1021个水分子。
(2)分子在不断运动着。能闻到远处的花香,品红在水中的扩散都是分子运动的结果。分子的运动速率随温度升高而加快。
(3)分子间具有一定的间隔。最好的证明就是:取50毫升酒精和50毫升水,混合之后,体积却小于100毫升。物质的热胀冷缩就是因为物质分子间的间隔受热增大,遇冷缩小。
(4)不同种物质的分子性质不同。
(5)在化学反应中分子可以再分。
(1)概念:由同种元素组成的纯净物。
(2)单质的分类:依据组成单质元素的性质把一单质分为三类。
金属单质:由金属元素组成的单质,如铁、铜、银等
非金属单质:由非金属元素组成的单质,如碳、磷、氧气等
稀有气体单质:由稀有气体元素组成的单质,如氦、氖、氛等单质
化合物:
(1)概念:由不同种元素组成的纯净物。
(2)化合物的分类:化合物分为有机化合物和无机化合物。
单质和化合物的区别和联系:
| 单质 | 化合物 | ||
| 区别 | 宏观组成 | 同种元素 | 不同种元素 |
| 微观构成 | 有同种原子构成 | 由不同种原子构成 | |
| 化学性质 | 不能发生分解反应 | 一定条件下发生分解反应 | |
| 联系 | 相互转变 | 它们均属于纯净物。单质发生化合反应可以生成化合物,化合物发生分解反应可以生成单质 | |
| 质子数 | 同一种元素的原子,不论在一单质里还是在化合物里,原子核内质子数保持不变 | ||
化合物与氧化物的区别和联系:
| 化合物 | 氧化物 | |
| 区别 | ①由不同种元素组成的纯净物叫化合物 ②由两种或两种以上元素组成 ③不一定含有氧元素 ④属于纯净物中的一类 |
①由两种元素组成的化合物中,如果有一种元素是氧元素,这种化合物叫氧化物 ②一定由两种元素组成 ③一定含有氧元素 ④属于化合物中的一类 |
| 联系 | 氧化物和化合物是个体与总体的关系,氧化物属于化合物中的一类 | |
同种元素组成的物质一定是单质吗?
由同种元素组成的纯净物叫做单质。理解单质的概念必须抓住两点:①由同种元素组成;②必须是纯净物,如氧气是一单质。由同种元素组成的物质不一定是单质,也可能是混合物,但绝不可能是化合物,如氧气 (O2)、臭氧(O3)两种物质混在一起是一种混合物,但是只有一种氧元素;同样的例子还有红磷和白磷,金刚石和石墨等。
对单质和化合物概念的理解:
(1)单质的概念:
①理解一单质的概念不仅要关注它是由一种元素组成,还应注意它首先是一种纯净物。如:氧气、氮气、碳、硫、铁、铜、各种稀有气体等都属于单质。
②由同种元素组成的物质不一定是单质,还可能是混合物:如:氧气与臭氧的混合物、白磷与红磷的混合物、金刚石与石墨的混合物等都只含一种元素,但都属于混合物。
(2)化合物的概念:理解化合物的概念同样不仅要关注它是由两种或两种以上的元素组成,还应注意它首先是一种纯净物。如二氧化碳,氯化钠、高锰酸钾等都属于化合物。
共价化合物与离子化合物的区别:
1. 共价化合物
(1)概念:像HCl、CO2这样以共用电子对结合在一起的化合物为共价化合物。
(2)共价化合物的类型:
①两种非金属原子结合成的化合物,如HCl、CO2等。
②非金属与酸根构成的化合物,如H2SO4、HNO3等。
2. 离子化合物与共价化合物的区别:
离子化合物是由阴、阳离子相互作用形成的化合物;共价化合物是原子间全部以共用电子对结合形成的化合物。离子化合物由离子构成,共价化合物大多数由分子构成。
混合物:
(1)概念:由两种或多种物质混合而成的物质,没有有固定的组成,各成分保持自己原有的化学性质。
(3)常见的混合物:空气、合金、矿石、溶液等。
(4)混合物的提纯:混合物经过物理或化学的方法可以提纯。
纯净物:
(1)概念:只由一种物质组成的物质。
(3)纯净物的分类:纯净物根据物质组成的元素种类,分为两大类:单质和化合物。
纯净物和氧化物的区别:
| 纯净物 | 混合物 | |
| 概念 | 宏观:由一种物质组成的物质 微观:由同种分子构成(对于由分子构成的物质而言) |
宏观:由两种或多种物质组成的物质 微观:由不同种分子构成(对于由分子构成的物质而言) |
| 区别 | 由同种物质组成(对于由分子构成的物质,是由同种分子构成的),组成是固定的 | 由不同种物质组成(对于由分子构成的物质. 是由不同种分子构成的),组成是不固定的 |
| 特点 | ①具有固定的组成 ②具有一定的性质 ③有专门的化学符号 |
①没有固定的组成和性质 ②各成分保持各自的性质 ③没有专门的化学符号 |
| 分离方法 | 组成固定,不需分离;若需将化合物分成几种单质,则必须通过化学方法才能实现 | 物理方法: 筛选 过滤 蒸馏 |
| 实例 | 氧气,二氧化碳,高锰酸钾 | 空气,粗盐,蔗糖水 |
| 联系 | 纯净物是相对而言的,自然界中绝对纯净的物质是不存在的,通常的纯净物是指含杂质很少的具有高纯度的物质。两者间的关系为 | |
对纯净物和混合物概念的理解:
(1)混合物概念:混合物可以看作是由几种纯净物混合而成的,混合物的形成过程中发生的是物理变化。由于混合物的组成一般不固定,所以往往不能用化学式表示。
(2)纯净物概念:纯净物只由一种物质组成,有固定的组成.可以用化学式表示。
常考的纯净物与混合物:
(1)混合物:石油、煤、天然气、洁净的空气、生理盐水、矿泉水、汽水、碘酒、白酒、双氧水、盐酸、合金等都是混合物。
(2)纯净物:水银、烧碱、纯碱、胆矾、液态氧、液态氮、蒸馏水(纯水)、干冰、冰水共存物、金刚石、石墨、生石灰、熟石灰、氯化钠、氧化铁等都是纯净物:
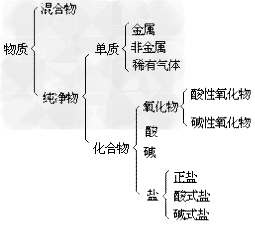
物质的分类示意图:
与“下列说法正确的是( )A.由不同种元素组成的物质一定是化合...”考查相似的试题有:
- 萝卜有很高的营养价值和药用价值,在民间有“小人参”之美称.俗语有“萝卜上市、医生没事”之说.萝卜中含有丰富的碳水化合物和...
- 建立宏观和微观之间的联系是化学学科特有的思维方式。下列对宏观事实的微观解释错误的是 【 】A.缉毒犬能根据气味发现毒品,...
- 分子的运动与温度的关系如何?请利用品红设计一个简单实验进行探究.(1)假设:______.(2)用品:______.(3)进行实验:...
- 化学知识中有很多的“相等”。请你判断下列说法中不正确的是[ ]A.溶液稀释前后,溶质的质量相等B.化合物中,元素正化合价数值等...
- 分子、原子和离子都是构成物质的粒子,下列物质由分子构成的是A.铁B.氧气C.石墨D.氯化钠
- 从分子的角度分析,下列解释不正确的是A.水结冰体积变大——分子大小发生改变B.氧气加压后贮存在钢瓶中——分子间有间隔C.水通...
- (3分)下图中A、B分别是某微粒的结构示意图,回答下列问题:(1)若A是地壳中含量最多的金属元素,则该元素的离子符号为 。 ...
- 臭氧层是地球的保护伞,臭氧(O3)属于[ ]A.单质B.化合物C.氧化物D.混合物
- 下列物质中属于纯净物的是( )A.人呼出的气体B.液氧C.洁净的空气D.自来水
- 下列常见物质中,属于纯净物的是( )A.新鲜空气B.氧气C.澄清的石灰水D.河水