本试题 “有关氢氧化钠的叙述不正确的是( )A.露置在空气中易变质B.溶于水时放出热量C.能使紫色石蕊试液变蓝色D.能做治疗胃酸过多的药物” 主要考查您对溶解过程中的放热和吸热
离子的共存
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 溶解过程中的放热和吸热
- 离子的共存
概念:
在溶解过程中发生了两种变化,一种是溶质的分子(或离子)在水分子的作用下向水中扩散,这一过程吸收热量;另一种是扩散的溶质的分子(或离子)和水分子作用,生成水和分子(或水和离子),这一过程放出热量。
物质溶解过程中的两种变化:
扩散过程:溶质的分子(或离子)向水中扩散,是物理过程,吸收热量
水合过程:溶质的分子(或离子)和水分子作用,生成水合分子(或水合离子),是化学过程,放出热量
溶解过程中的温度变化:
a.扩散过程中吸收的热量>水合过程中放出的热量,溶液温度降低,如:NH4NO3溶解于水。
b.扩散过程中吸收的热量<水合过程中放出的热摄,溶液温度升高,如:NaOH、浓硫酸溶解于水。
c.扩散过程中吸收的热量≈水合过程中放出的热量,溶液温度几乎不变,如:NaCl溶解于水。
常见冷冻混合物:
在生产、生活中常用冰作冷却剂,但冰只能提供 0℃左右的低温。一些医疗和研究单位常需要更低的温度,提供低温较方便的方法是用冷冻混合物。
下表是几种常见冷冻混合物的组成及所能达到的最低温度。
在溶解过程中发生了两种变化,一种是溶质的分子(或离子)在水分子的作用下向水中扩散,这一过程吸收热量;另一种是扩散的溶质的分子(或离子)和水分子作用,生成水和分子(或水和离子),这一过程放出热量。
物质溶解过程中的两种变化:
扩散过程:溶质的分子(或离子)向水中扩散,是物理过程,吸收热量
水合过程:溶质的分子(或离子)和水分子作用,生成水合分子(或水合离子),是化学过程,放出热量
溶解过程中的温度变化:
a.扩散过程中吸收的热量>水合过程中放出的热量,溶液温度降低,如:NH4NO3溶解于水。
b.扩散过程中吸收的热量<水合过程中放出的热摄,溶液温度升高,如:NaOH、浓硫酸溶解于水。
c.扩散过程中吸收的热量≈水合过程中放出的热量,溶液温度几乎不变,如:NaCl溶解于水。
常见冷冻混合物:
在生产、生活中常用冰作冷却剂,但冰只能提供 0℃左右的低温。一些医疗和研究单位常需要更低的温度,提供低温较方便的方法是用冷冻混合物。
下表是几种常见冷冻混合物的组成及所能达到的最低温度。
| 冷冰混合物的组成 | 最低温度 |
| 41gNH4NO3和100g冰 | -17 |
| 19NH4Cl和100g冰 | -16 |
| 23gNaCl和100g冰 | -21 |
| 22gMgCl2和100g冰 | -34 |
概念:
所谓离子共存,实质上就是看离子间是否发生反应的问题。若在溶液中发生反应,就不能共存。看能否发生反应,不仅是因为有沉淀、气体、水、难电离的物质产生,还涉及到溶液酸碱性、有色、无色,能否进行氧化还原反应等。
判断离子是否共存的方法:
复分解反应的实质就是两种化合物相互交换成分,生成两种新的化合物,所以同一溶液中的离子之间如符合下列条件之一就会发生反应,即离子不能在溶液中大量共存。
(1)生成沉淀:如Ag+和Cl-,Ba2+和SO42-,Ca2+和 CO32-,Cu2+和OH-等不能大量共存。
(2)生成气体:如H+和CO32-,HCO3-,NH4+和OH-等不能大量共存。
(3)生成水:如H+和OH-不能大量共存。
(4)可能会有附加条件,如溶液无色透明、pH=l (酸性溶液)、pH=14(碱性溶液)等。判断离子能否共存时,应先看清试题的前提条件再分析离子间的相互反应情况。
判断离子是否共存的几种情况:
①由于发生复分解反应,离子不能大量共存。
A.有气体产生。如CO32- 、SO32- 、S2- 、HCO3-、HSO3-、HS-等易挥发的弱酸的酸根与H+不能大量共存。
B.有沉淀生成。如Ba2+ 、Ca2+ 、Mg2+、Ag+等不能与SO42-、CO32-等大量共存;
Mg2+、Fe2+、Ag+、Al3+、Zn2+、Cu2+、Fe3+等不能与OH-大量共存;
Fe2+与S2-、Ca2+与PO43-、Ag+与I-不能大量共存。
C.一些酸根离子如HCO3-、HPO42-、HS-、H2PO4-、HSO3-不能与OH-大量共存;
NH4+与OH-不能大量共存。
②由于发生氧化还原反应,离子不能大量共存。
A.具有较强还原性的离子不能与具有较强氧化性的离子大量共存。
如S2-、HS-、SO32-、I-和Fe3+不能大量共存。
B.在酸性或碱性的介质中由于发生氧化还原反应而不能大量共存。
如MnO4-、NO3-、ClO-与S2-、HS-、SO32-、HSO3-、I-、Fe2+等不能大量共存;
SO32-和S2-在碱性条件下可以共存,
但在酸性条件下则由于发生2S2- +SO32- +6H+=3S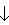 +3H2O反应不能共在。
+3H2O反应不能共在。
③溶液中能发生络合反应的离子不能大量共存。
如Fe2+ 、Fe3+与SCN-不能大量共存。
主要题目要求的限定:
①酸性溶液(H+)、碱性溶液(OH-)等不能共存的离子。
②溶液的颜色:有色离子
MnO4-(紫色)、Fe3+(棕黄)、Fe2+(浅绿)、Cu2+(蓝)等
所谓离子共存,实质上就是看离子间是否发生反应的问题。若在溶液中发生反应,就不能共存。看能否发生反应,不仅是因为有沉淀、气体、水、难电离的物质产生,还涉及到溶液酸碱性、有色、无色,能否进行氧化还原反应等。
判断离子是否共存的方法:
复分解反应的实质就是两种化合物相互交换成分,生成两种新的化合物,所以同一溶液中的离子之间如符合下列条件之一就会发生反应,即离子不能在溶液中大量共存。
(1)生成沉淀:如Ag+和Cl-,Ba2+和SO42-,Ca2+和 CO32-,Cu2+和OH-等不能大量共存。
(2)生成气体:如H+和CO32-,HCO3-,NH4+和OH-等不能大量共存。
(3)生成水:如H+和OH-不能大量共存。
(4)可能会有附加条件,如溶液无色透明、pH=l (酸性溶液)、pH=14(碱性溶液)等。判断离子能否共存时,应先看清试题的前提条件再分析离子间的相互反应情况。
判断离子是否共存的几种情况:
①由于发生复分解反应,离子不能大量共存。
A.有气体产生。如CO32- 、SO32- 、S2- 、HCO3-、HSO3-、HS-等易挥发的弱酸的酸根与H+不能大量共存。
B.有沉淀生成。如Ba2+ 、Ca2+ 、Mg2+、Ag+等不能与SO42-、CO32-等大量共存;
Mg2+、Fe2+、Ag+、Al3+、Zn2+、Cu2+、Fe3+等不能与OH-大量共存;
Fe2+与S2-、Ca2+与PO43-、Ag+与I-不能大量共存。
C.一些酸根离子如HCO3-、HPO42-、HS-、H2PO4-、HSO3-不能与OH-大量共存;
NH4+与OH-不能大量共存。
②由于发生氧化还原反应,离子不能大量共存。
A.具有较强还原性的离子不能与具有较强氧化性的离子大量共存。
如S2-、HS-、SO32-、I-和Fe3+不能大量共存。
B.在酸性或碱性的介质中由于发生氧化还原反应而不能大量共存。
如MnO4-、NO3-、ClO-与S2-、HS-、SO32-、HSO3-、I-、Fe2+等不能大量共存;
SO32-和S2-在碱性条件下可以共存,
但在酸性条件下则由于发生2S2- +SO32- +6H+=3S
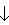 +3H2O反应不能共在。
+3H2O反应不能共在。③溶液中能发生络合反应的离子不能大量共存。
如Fe2+ 、Fe3+与SCN-不能大量共存。
主要题目要求的限定:
①酸性溶液(H+)、碱性溶液(OH-)等不能共存的离子。
②溶液的颜色:有色离子
MnO4-(紫色)、Fe3+(棕黄)、Fe2+(浅绿)、Cu2+(蓝)等
发现相似题
与“有关氢氧化钠的叙述不正确的是( )A.露置在空气中易变质B....”考查相似的试题有:
- 下列数据是硝酸钾固体在不同温度时的溶解度。(1)硝酸钾溶液中的溶剂是____。(2)观察上述表格,可以总结出的规律是___________...
- 小琪往如图所示的烧杯中加入一种物质,搅拌后,发现塑料片的水结了冰.她加入的物质是( )A.食盐B.硝酸铵C.生石灰D.氢氧...
- 下列变化后温度降低的是( )A.Mg与盐酸反应B.NaOH固体溶于水C.CO2与C反应D.NH4NO3固体溶于水
- 下列是人们在生产、生活中的一些认识。其中科学合理的是A.用洗洁精除油污属于乳化作用B.火炉旁放盆石灰水能防止煤气中毒C....
- 为了测定在一定温度时某固体物质的溶解度,待测液必须是该温度下该物质的( )A.浓溶液B.稀溶液C.不饱和溶液D.饱和溶液
- 温度不变时,向一定量的饱和硝酸钾溶液中加入少量硝酸钾固体,则此饱和溶液的质量 A.增加B.减少C.不变D.无法确定
- 下列物质放入水中,能形成溶液的是A.植物油B.面粉C.泥沙D.蔗糖
- (选做题A组)下列物质在水溶液中能共存的是[ ]A.NaCl、 AgNO3B.NaOH、FeCl3C.NaNO3、CuSO4D.H2SO4、K2CO3
- 某无色溶液中,可能含有H+、Ag+、Cu2+、Na+、OH-、Cl-、NO3-、CO32-等8种离子中的几种,取该溶液少许,滴入几滴石蕊试液,石...
- 下列离子能在同一水溶液中大量共存并形成无色溶液的是[ ]A.Mg2+、Cl-、Na+、OH- B.K+、OH-、Ba2+、Cl-C.H+、K+、CO32-、NO3-D...