本试题 “类推的思维方法在化学学习与研究中常会产生错误的结论,因此类推的结论最终要经过实践的检验才能确定其正确与否.下列几种类推结论中,正确的是( )A.由2Cu...” 主要考查您对单质钠
氧化亚铁
氧化铁
四氧化三铁
氢氧化亚铁
氢氧化铁
二氧化硫
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 单质钠
- 氧化亚铁
- 氧化铁
- 四氧化三铁
- 氢氧化亚铁
- 氢氧化铁
- 二氧化硫
钠的基本性质:
钠元素的原子序数等于11,在周期表中位于第三周期,第ⅠA族。钠的原子结构示意图为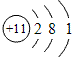 ,故钠的金属性比较强,是很活泼的金属材料。其单质很软,具有银白色金属光泽,是热和电的良导体。钠的密度比水小,比煤油大,熔点97.81℃,沸点882.9℃。
,故钠的金属性比较强,是很活泼的金属材料。其单质很软,具有银白色金属光泽,是热和电的良导体。钠的密度比水小,比煤油大,熔点97.81℃,沸点882.9℃。
钠的物理性质:
钠单质很软,具有银白色金属光泽,是热和电的良导体。钠的密度比水小,比煤油大,熔点97.81℃,沸点882.9℃。
概括为:银白软轻低,热电良导体。
钠的化学性质:
钠的原子结构示意图为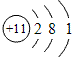 。
。
①与非金属单质的反应
A. 与氧气反应 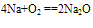 (白色固体,不稳定)(空气中,钠的切面由银白色逐渐变暗的原因)
(白色固体,不稳定)(空气中,钠的切面由银白色逐渐变暗的原因)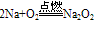 (淡黄色固体,较稳定)
(淡黄色固体,较稳定)
B. 与硫反应
2Na + S ==Na2S (研磨时发生爆炸)
C. 与氯气反应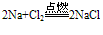
②与水反应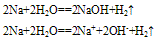
| 主要实验现象 | 对实验现象的分析 |
| 浮在水面上 | 密度比水小 |
| 熔化成闪亮的小球 | 反应放热,且钠的熔点低 |
| 迅速游动 | 反应产生气体(H2) |
| 嘶嘶作响 | 反应剧烈 |
| 溶液呈红色 | 反应生成NaOH,遇酚酞变红 |
③与盐溶液反应
钠与盐溶液反应,先考虑钠与水反应生成氢氧化钠,在考虑氢氧化钠是否与盐反应。
A. 投入NaCl溶液中,只有氢气放出。2Na+2H2O==2NaOH+H2↑
B. 投入饱和NaCl溶液中,有氢气放出,还有NaCl晶体析出(温度不变)。
C. 投入NH4Cl溶液中,有H2和NH3逸出。2Na+2NH4Cl==2NaCl+2NH3↑+H2↑
D. 投入CuSO4溶液中,有气体放出和蓝色沉淀生成。
2Na+2H2O+CuSO4==Na2SO4+Cu(OH)2↓+H2↑
如何正确取用钠?
钠具有很活泼的化学性质,易与很多物质反应,所以在取用钠时一定要注意,千万不能直接用手去拿,以免手被腐蚀,实验剩余的钠屑,绝对不可以随意丢弃,而应放回到原瓶中。
正确做法:用镊子取一小块金属钠,用滤纸吸干表面的煤油,用小刀切去一端的表层,观察表面的颜色。实验中剩余的钠必须放回原瓶。
钠露置在空气中的一系列变化:
Na→Na2O→NaOH→Na2CO3→Na2CO3·10H2O→Na2CO3
钠的保存、制取及用途 :
①保存:由于金属钠的化学性质非常活泼,易与空气中的氧气、水蒸气反应,所以钠要保存在煤油中。
②在实验室中钠块的取用:用镊子从试剂瓶中取出钠块,用滤纸吸净表面上的煤油,在玻璃片上用小刀切去表面的氧化层,再切下一小粒备用,余下的钠全部放回试剂瓶中。
③制取:
④用途:
A. 工业上用Na作还原剂,用与冶炼金属,如4Na+TiCl4 Ti+4NaCl
Ti+4NaCl
B. Na-K合金(液态)用作原子反应堆的导热剂。
C. 在电光源上,用钠制造高压钠灯。
焰色反应:
焰色反应是化学上用来测试某种金属是否存在在化合物的方法。其原理是每种元素都有其特别的光谱,显示出不同的颜色。
焰色反应的操作:
先准备一支铂丝,钴蓝玻璃及盐或其溶液。
把铂丝浸在浓盐酸中以清除先前余下的物质,再把铂丝放在酒精灯焰(蓝色火焰)中直至没有颜色的变化。
用蒸馏水或去离子水或纯水冲洗铂丝。
用铂丝接触盐或溶液,通过酒精灯焰(蓝色火焰)中加热。
当钠离子存在于所测试的溶液中,用钴蓝玻璃过滤钠离子的焰色。
最后将观察焰色。钠的焰色为明亮的金黄色火焰。
各种元素的颜色:
| 元素符号 | 离子元素 | 名称 | 焰色 |
| Ba | Ba2+ | 钡 | 黄绿 |
| Ca | Ca2+ | 钙 | 砖红 |
| Cs | Cs+ | 铯 | 浅紫 |
| Na | Na+ | 钠 | 黄 |
| Zn | Zn2+ | 锌 | 蓝绿 |
| Fe(III) | Fe3+ | 铁(III) | 金黄 |
| K | K+ | 钾 | 浅紫(透过蓝色钴玻璃) |
| Li | Li+ | 锂 | 深红 |
碱金属元素的性质:
1.氧化产物的特殊性。碱金属在空气中燃烧,只有Li氧化生成Li2O;其余的生成过氧化物(如Na2O2)或更复杂的氧化物(如KO2)。
2.碱金属单质密度都较小,其中锂的密度是所有金属中最小的。
3.碱金属单质熔点都较低,只有Li的熔点高于100℃。
4.钾、钠在常温下为固态,但钾钠合金在常温下为液态,可作为原子反应堆的导热剂。
5.碱金属单质通常保存在煤油中,但因锂的密度小于煤油而只能保存在液体石蜡中或封存在固体石蜡中。
6.一般说,酸式盐较正盐溶解度大,但NaHCO3却比Na2CO3溶解度小。
7.试剂瓶中的药品取出后,一般不能放回原瓶,但ⅠA族金属Na、K等除外。
8.一般活泼金属能从盐中置换出不活泼金属,但非常活泼的金属Na、K等除外。
9.Fr是放射性元素,所以在自然界中不存在。
氧化亚铁:
(1)色态:黑色粉末
(2)溶解性:不溶于水,不与水反应,溶于盐酸、稀硫酸生成亚铁盐。
(3)稳定性:不稳定,在空气中加热时迅速被氧化成四氧化三铁
(4)氧化性:(高温下)被CO、H2、Al、C、Si等还原
(5)还原性:在空气中加热氧化为Fe3O4
氧化亚铁:
(1)色态:黑色粉末
(2)溶解性:不溶于水,不与水反应,溶于盐酸、稀硫酸生成亚铁盐。
(3)稳定性:不稳定,在空气中加热时迅速被氧化成四氧化三铁
(4)氧化性:(高温下)被CO、H2、Al、C、Si等还原
(5)还原性:在空气中加热氧化为Fe3O4
铁的氧化物:
| 化学式 | FeO | Fe2O3 | Fe3O4 |
| 俗称 | —— | 铁红 | 磁性氧化铁 |
| 色态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
| 铁的价态 | +2 | +3 | +2、+3 |
| 水溶性 | 不溶 | 不溶 | 不溶 |
| 与酸反应 | FeO+2H+==Fe2++H2O | Fe2O3+6H+==2Fe3++3H2O | Fe3O4+8H+==Fe2++2Fe3++4H2O |
| 用途 | 玻璃色料 | 油漆、颜料 | 做颜料和抛光剂 |
| 氧化性 | 高温时都能与C、CO、H2反应,被还原生成Fe单质 | ||
氧化亚铁的化学性质:
- 铝热反应:2Al+3FeO=(高温)=Al2O3+3Fe
- 与非氧化性酸反应:FeO+2H+==Fe2++H2O
- 与氧化性酸反应:3FeO+10H++NO3-==3Fe3++NO↑+5H2O
氧化铁:
化学式Fe2O3,溶于盐酸,为红棕色粉末。其红棕色粉末为一种低级颜料,工业上称氧化铁红,用于油漆、油墨、橡胶等工业中,可做催化剂,玻璃、宝石、金属的抛光剂,可用作炼铁原料。
(1)色态:红色粉末,俗称铁锈(铁红)
(2)溶解性:溶于盐酸、稀硫酸生成+3价铁盐;难溶于水,不与水反应。
(3)氧化性:高温下被CO、H2、Al、C、Si等还原
氧化铁的化学性质:
- 铝热反应:2Al+Fe2O3=(高温)=Al2O3+2Fe
- 与强酸反应:Fe2O3+6H+==2Fe3++3H2O
- 与还原性酸(HI)反应:Fe2O3+6H++2I-==2Fe2++3H2O+I2
铁的氧化物:
| 化学式 | FeO | Fe2O3 | Fe3O4 |
| 俗称 | —— | 铁红 | 磁性氧化铁 |
| 色态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
| 铁的价态 | +2 | +3 | +2、+3 |
| 水溶性 | 不溶 | 不溶 | 不溶 |
| 与酸反应 | FeO+2H+==Fe2++H2O | Fe2O3+6H+==2Fe3++3H2O | Fe3O4+8H+==Fe2++2Fe3++4H2O |
| 用途 | 玻璃色料 | 油漆、颜料 | 做颜料和抛光剂 |
| 氧化性 | 高温时都能与C、CO、H2反应,被还原生成Fe单质 | ||
四氧化三铁:
又称磁性氧化铁,具有磁性的黑色晶体,不溶于水,具有优良的导电性。
四氧化三铁的性质:
(1)色态:具有磁性的黑色晶体
(2)别名:磁性氧化铁、氧化铁黑、磁铁、磁石、吸铁石、偏铁酸亚铁
(3)矿物:磁铁矿
(4)溶解性:不溶于水,与酸反应生成+2、+3铁盐
(5)稳定性:稳定
(6)还原性:在高温下,易氧化成三氧化二铁。4Fe3O4+O2 6Fe2O3
6Fe2O3
(7)氧化性:在高温下可与还原剂H2、CO、Al、C等反应。 


铁的氧化物:
| 化学式 | FeO | Fe2O3 | Fe3O4 |
| 俗称 | —— | 铁红 | 磁性氧化铁 |
| 色态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
| 铁的价态 | +2 | +3 | +2、+3 |
| 水溶性 | 不溶 | 不溶 | 不溶 |
| 与酸反应 | FeO+2H+==Fe2++H2O | Fe2O3+6H+==2Fe3++3H2O | Fe3O4+8H+==Fe2++2Fe3++4H2O |
| 用途 | 玻璃色料 | 油漆、颜料 | 做颜料和抛光剂 |
| 氧化性 | 高温时都能与C、CO、H2反应,被还原生成Fe单质 | ||
氢氧化亚铁:
化学式为Fe(OH)2,白色固体,难溶于水,碱性较弱,可与常见酸反应;在空气中易被氧化,白色→灰绿色→红褐色。反应方程式如下:
(1)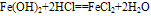
(2)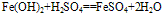
(3)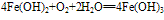
氢氧化亚铁的性质:
氢氧化亚铁极易被氧化,水中的溶解氧就可以把它氧化。
4Fe(OH)2+O2+2H2O=4Fe(OH)3
4Fe(OH)2+O2=△=2Fe2O3+4H2O
铁的氢氧化物:
| Fe(OH)2 | Fe(OH)3 | |
| 色态 | 白色固体 | 红褐色固体 |
| 与盐酸反应 | Fe(OH)2+2H+==Fe2++2H2O | Fe(OH)3+3H+==Fe3++3H2O |
| 热稳定性 | 在空气中加热迅速生成Fe3O4 | 2Fe(OH)3=(加热)=Fe2O3+3H2O |
| 二者的关系 | 在空气中Fe(OH)2能够非常迅速地被氧化成Fe(OH)3,现象是:白色迅速变成灰绿色,最后变成红褐色。反应方程式为:4Fe(OH)2+O2+2H2O===4Fe(OH)3 | |
氢氧化亚铁的制备:
因Fe(OH)2在空气中易被氧化,4Fe(OH)2+O2+2H2O===4Fe(OH)3,故Fe(OH)2在水中不能稳定存在,在实验室制取Fe(OH)2时,一定要用新制的亚铁盐和先加热驱赶掉O2的NaOH溶液,且滴管末端要插入试管内的液面以下,再滴加NaOH溶液,也可以在反应液面上滴加植物油或苯等物质进行液封,以减少Fe(OH)2与O2的接触。关于Fe(OH)2制备的方法很多,核心问题有两点,一是溶液中溶解的氧必须除去,二是反应过程必须与O2隔绝。
1、操作方法:在试管里注入少量新制备的硫酸亚铁溶液,再向其中滴入几滴煤油,用胶头滴管吸取氢氧化钠溶液,将滴管尖端插入试管里溶液液面下,逐滴滴入氢氧化钠溶液,观察现象。另外,为使氢氧化亚铁的制备成功,先将硫酸亚铁溶液加热,除去溶解的氧气。
实验现象:滴入溶液到硫酸亚铁溶液中有白色絮状沉淀生成。白色沉淀放置一段时间,振荡后迅速变成灰绿色,最后变成红褐色。
注:白色沉淀:Fe(OH)2;灰绿色沉淀:Fe(OH)2和Fe(OH)3的混合物;红褐色沉淀:Fe(OH)3
方法的改进:可在液面上滴加苯或者油进行液封,可有效防止氧的溶解。
【典例】 Ⅰ.用不含Fe3+的FeSO4溶液与不含O2的蒸馏水配制的NaOH溶液反应制备。
(1)用硫酸亚铁晶体配制上述FeSO4溶液时还需要加入________。
(2)除去蒸馏水中溶解的O2常采用________的方法。
(3)生成Fe(OH)2白色沉淀的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液,这样操作的理由是__________________________________________________________ ________________________________________________________
Ⅱ.在如图所示的装置中,用NaOH溶液、铁屑、稀H2SO4等试剂制备。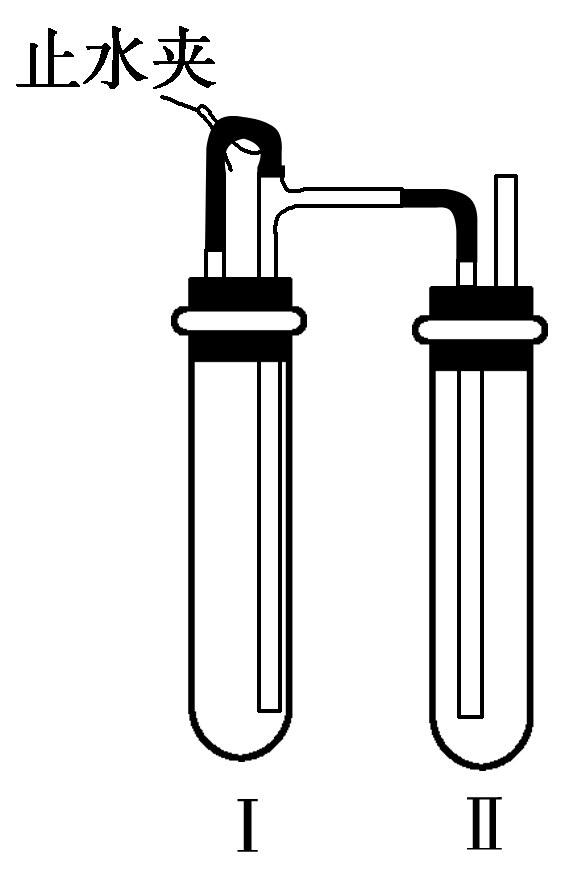
(1)在试管Ⅰ中加入的试剂是________。
(2)在试管Ⅱ中加入的试剂是________。
(3)为了制得Fe(OH)2白色沉淀,在试管Ⅰ和Ⅱ中加入试剂,打开止水夹,塞紧塞子后的实验步骤是_____________________________。
(4)这样生成的Fe(OH)2沉淀能较长时间保持白色,理由是_________________________________________________________________。
【答案】:Ⅰ.(1)稀H2SO4、铁屑 (2)煮沸 (3)避免生成的Fe(OH)2沉淀接触O2而被氧化 Ⅱ.(1)稀H2SO4和铁屑 (2)NaOH溶液 (3)检验试管Ⅱ出口处排出的H2的纯度,当排出的H2已经纯净时再夹紧止水夹 (4)试管Ⅰ中反应生成的H2充满了试管Ⅰ和试管Ⅱ,故外界O2不易进入
2、电化学制备
【典例】 由于Fe(OH)2极易被氧化,所以实验室难用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀。若用下图所法实验装置可制得纯净的Fe(OH)2沉淀。两极材料分别为石墨和铁。
①a电极材料为_______,其电极反应式为_______________。
②电解液d可以是_______,则白色沉淀在电极上生成;也可以是_______,则白色沉淀在两极之间的溶液中生成。
A.纯水 B.NaCl溶液 C.NaOH溶液 D.CuCl2溶液
③液体c为苯,其作用是______________,在加入苯之前,对d溶液进行加热处理的目的是___________。
④为了在短时间内看到白色沉淀,可以采取的措施是____________________。
A.改用稀硫酸做电解液 B.适当增大电源电压 C.适当缩小两电极间距离 D.适当降低电解液温度
⑤若d改为Na2SO4溶液,当电解一段时间,看到白色沉淀后,再反接电源,继续电解,除了电极上看到气泡外,另一明显现象为___________。
【答案】:①Fe;Fe-2e-=Fe2+ ②C;B ③隔绝空气防止Fe(OH)2被空气氧化;排尽溶液中的氧气,防止生成的Fe(OH)2在溶液中氧化 ④B、C ⑤白色沉淀迅速变成灰绿色,最后变成红褐色
氢氧化铁:
红褐色固体,难溶于水,易与酸反应;加热可分解生成氧化铁。反应方程式如下:
(1)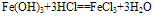
(2)
(3)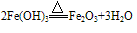
氢氧化铁胶体的制备:
操作步骤:将烧杯中的蒸馏水加热至沸腾,向沸水中滴加5~6滴饱和FeCl3溶液,继续煮沸至呈红褐色为止。
离子方程式:Fe3++3H2O=(加热)=Fe(OH)3(胶体)+3H+
铁的氢氧化物:
| Fe(OH)2 | Fe(OH)3 | |
| 色态 | 白色固体 | 红褐色固体 |
| 与盐酸反应 | Fe(OH)2+2H+==Fe2++2H2O | Fe(OH)3+3H+==Fe3++3H2O |
| 热稳定性 | 在空气中加热迅速生成Fe3O4 | 2Fe(OH)3=(加热)=Fe2O3+3H2O |
| 二者的关系 | 在空气中Fe(OH)2能够非常迅速地被氧化成Fe(OH)3,现象是:白色迅速变成灰绿色,最后变成红褐色。反应方程式为:4Fe(OH)2+O2+2H2O===4Fe(OH)3 | |
①化学式:SO2
②分子结构:SO2是由极性键形成的极性分子,因此易溶于水,其晶体为分子晶体。
二氧化硫的物理性质和化学性质:
1.物理性质:
SO2是无色、有刺激性气味的有毒气体,密度比空气大,易溶于水(常温常压下,1体积水大约溶解40体积的SO2),易液化(沸点-10℃)。
2.化学性质
(1)具有酸性氧化物的通性
①将SO2通入紫色石蕊试液中,试液变红。
②能与碱性氧化物、碱及某些盐反应。如:
(2)还原性 

(3)弱氧化性 
(4)漂白性(不能漂白酸碱指示剂) 能和某些有色物质化合生成无色物质,生成的无色物质不稳定,易分解而恢复原色,因此,SO2的漂白并不彻底。在中学化学常见试剂中,能用SO2漂白的只有品红溶液,品红溶液 无色溶液
无色溶液 恢复原色。
恢复原色。
SO2与一些物质反应的实验现象:


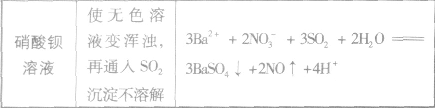
SO2与强碱反应后固体成分的确定:
SO2与强碱(如NaOH)溶液发生反应后的固体成分取决于二者的用量。遇到类似的问题,可以采用数轴分析法讨论。设SO2的物质的量为n(SO2),NaOH物质的量为n(NaOH),数轴代表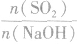 ,如下数轴所示:
,如下数轴所示: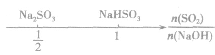
分析数轴可得:
(1)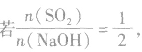 则固体物质为Na2SO3,
则固体物质为Na2SO3,
(2)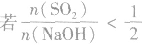 ,则固体物质为NaOH 和Na2SO3.
,则固体物质为NaOH 和Na2SO3.
(3)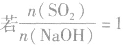 ,则同体物质为NaHSO3
,则同体物质为NaHSO3
(4)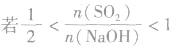 ,则固体物质为Na2SO3和NaHSO3,
,则固体物质为Na2SO3和NaHSO3,
(5)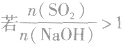 ,则固体物质为NaHSO3。
,则固体物质为NaHSO3。
二氧化硫的制备:
工业制法:

实验室制法:
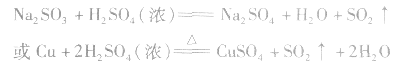
(1)收集:向上排空气法。
(2)检验:品红溶液。SO2是中学阶段学到的唯一种既能使品红褪色,加热后又能使其恢复原色的气体。
(3)尾气处理:用NaOH溶液吸收。
二氧化硫的用途:
工业上用二氧化硫漂白纸浆、毛、丝、草编制品等。此外,二氧化硫还可用于杀菌消毒,可以用作防腐剂。
二氧化硫对环境的污染及治理:

与“类推的思维方法在化学学习与研究中常会产生错误的结论,因此...”考查相似的试题有:
- 自然界中存在一种尖晶石,化学式可表示为MgAl2O4,它透明色美,可作为宝石。已知该尖晶石中混有Fe2O3。取一定量样品5.4g,恰...
- 汽车安全气囊是行车安全的重要保障.当车辆发生碰撞的瞬间,安全装置通电点火使其中的固体粉末分解释放出大量的氮气形成气囊...
- 为了除去Fe2(SO4)3溶液中混有的少量FeSO4,最好的方法是向此溶液中A.通入氯气B.加入H2O2C.加入FeD.加入KMnO4
- 向一定量的Fe,FeO,Fe2O3,Fe3O4的混合溶液中,加入150mL 4mol/L的稀硝酸,恰好使混合物完全溶解,并放出标准状况下NO气体2....
- 已知D、M、H是常见的非金属单质,其中M是无色气体,H是有色气体,J是一种金属单质(其同族的某种元素是形成化合物种类最多的...
- 油画置于空气中,天长日久就会生成黑色的PbS从而使油画的色彩变暗,若用H2O2来“清洗”,则可使PbS转变为白色的PbSO4,从而使油...
- 把一定量的SO2通入Fe(NO3)3溶液中,溶液由棕色变为浅绿色,但立即又变为棕黄色,此时若滴入BaCl2溶液,则会产生白色沉淀.在...
- 常温常压下,a、b、c、d四支相同的试管中,分别装入等体积的两种气体,a试管内是NO2与O2,b试管内为Cl2和SO2,c试管内为NO与O...
- (1)整个“固硫”反应所涉及的反应类型包括:①化合②分解③置换④复分解⑤氧化还原反应⑥非氧化还原反应⑦离子反应⑧非离子反应(分子...
- 某研究性学习小组用下图装置进行SO2与FeCl3溶液反应的相关实验。(夹持装置已略去)(1)在配制氯化铁溶液时需先把氯化铁晶体溶...