本试题 “灰锡(以粉末状存在)和白锡是锡的两种同素异形体。 已知:①Sn(s.白)+2HCl(aq)=SnCl2(aq)+H2(g) △H1②Sn(s、灰)+2HCl(aq)=SnCl2(aq)+H2(g) △H2③Sn(s、灰)Sn(s...” 主要考查您对氧化反应、还原反应
吸热反应、放热反应
焓变、反应热
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 氧化反应、还原反应
- 吸热反应、放热反应
- 焓变、反应热
氧化反应(被氧化):
反应物中某元素失电子,化合价升高的反应过程。
还原反应(被还原):
反应物中某元素得电子,化合价降低的反应过程。
反应物中某元素失电子,化合价升高的反应过程。
还原反应(被还原):
反应物中某元素得电子,化合价降低的反应过程。
氧化反应与还原反应的关系:
氧化还原反应是氧化反应与还原反应的矛盾的统一体,两者相反相成。
氧化剂 + ne- = 还原产物
还原剂 - ne- = 氧化产物
把氧化反应和还原反应分开,是构造原电池的前提。把原电池分成氧化—还原两部分,通过导线相连,就可以使电子沿导线运动,形成电流。
吸热反应:
吸收热量的反应,即生成物的总能量大于反应物的总能量,反应需要吸收能量
放热反应:
放出热量的反应,即生成物的总能量小于反应物的总能量,反应释放出能量
放热反应和吸热反应的比较:
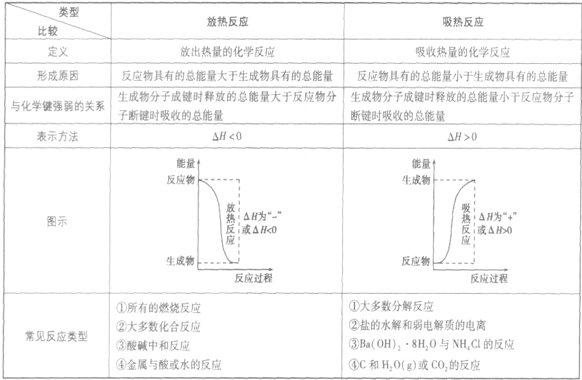
吸收热量的反应,即生成物的总能量大于反应物的总能量,反应需要吸收能量
放热反应:
放出热量的反应,即生成物的总能量小于反应物的总能量,反应释放出能量
放热反应和吸热反应的比较:

反应热,焓变:
化学能可以转化为热能、电能和光能等,化学反应中的能量变化,通常主要表现为热量的变化。
1.定义:在化学反应过程中,当生成物和反应物具有相同温度时所放出或吸收的热量,通常叫做化学反应的反应热。在恒温、恒压条件下,化学反应过程中吸收或放出的热量称为反应的焓变。
2.符号:△Ⅳ
3.单位:kJ·mol-1
4.产生原因:化学反应过程中旧键断裂吸收的总能量与新键形成释放的总能量不相等,故化学反应均伴随着能量变化——吸热或放热。
5.表示方法:放热反应的△H<0,吸热反应的△H>0.
化学能可以转化为热能、电能和光能等,化学反应中的能量变化,通常主要表现为热量的变化。
1.定义:在化学反应过程中,当生成物和反应物具有相同温度时所放出或吸收的热量,通常叫做化学反应的反应热。在恒温、恒压条件下,化学反应过程中吸收或放出的热量称为反应的焓变。
2.符号:△Ⅳ
3.单位:kJ·mol-1
4.产生原因:化学反应过程中旧键断裂吸收的总能量与新键形成释放的总能量不相等,故化学反应均伴随着能量变化——吸热或放热。
5.表示方法:放热反应的△H<0,吸热反应的△H>0.
发现相似题
与“灰锡(以粉末状存在)和白锡是锡的两种同素异形体。 已知:①S...”考查相似的试题有:
- 研究CO2的利用对促进低碳社会的构建具有重要的意义。(1)将CO2与焦炭作用生成CO,CO可用于炼铁等。①已知:Fe2O3(s) + 3C(石...
- 已知热化学方程式:H2(g)+1/2O2(g)=H2O(l) △H="-285.8KJ/mol" 当lg液态水变为水蒸汽时,其热量变化是A.吸热88kJB.吸热2.44J...
- .已知:2H2(g)+O2(g)===2H2O(l) ΔH=-571.6 kJ·mol-12CH3OH(l)+3O2(g)===2CO2(g)+4H2O(l) ΔH=-1452 kJ·mol-1H+(aq)...
- 随着大气污染的日趋严重,“节能减排”,减少全球温室气体排放,研究NOx、SO2、CO等大气污染气体的处理具体有重要意义。(1)如...
- 下列说法正确的是( )A.化学反应不一定伴随着能量的变化B.充电电池放电时,电能转变为化学能C.放在冰箱中的食品保质期较...
- (8分)(1)肼(N2H4)是发射航天飞船常用的高能燃料。将NH3和NaClO按一定物质的量比混合反应,生成肼、NaCl和水,该反应的化学方...
- (9分)(1)1 mol气态钠离子和1 mol气态氯离子结合生成1 mol氯化钠晶体释放出的热能为氯化钠晶体的晶格能。①下列热化学方程式中...
- 下列与化学反应能量变化相关的叙述正确的是( )A.生成物总能量一定低于反应物总能量B.放热反应的反应速率总是大于吸热反应...
- 固定和利用CO2,能有效地利用资源,并减少空气中的温室气体。Ⅰ.工业上正在研究利用CO2来生产甲醇燃料的方法,该方法的化学方...
- 已知化学反应的热效应只与反应物的初始状态和生成物的最终状态有关,如图(Ⅰ)所示:ΔH1=ΔH2+ΔH3根据上述原理和图(Ⅱ)所示,判...