本试题 “下列说法正确的是( )A.酸与碱发生中和反应所放出的热量称为中和热B.化学反应中能量变化的大小与反应物的质量多少无关C.由1H、2H、3H、35Cl、37Cl组成的...” 主要考查您对核素
中和热
能量的相互转化
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 核素
- 中和热
- 能量的相互转化
定义:
具有一定的质子数和中子数的一种原子叫做核素  的含义:
的含义: 表示一个质量数为A、质子数为Z的原子。
表示一个质量数为A、质子数为Z的原子。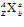 中A表示质量数,Z表示质子数,a表示粒子所带的电荷数和电性,b表示组成该粒子的原子数目。
中A表示质量数,Z表示质子数,a表示粒子所带的电荷数和电性,b表示组成该粒子的原子数目。
元素,核素与同位素的比较:
| 元素 | 同位素 | 核素 | |
| 概念 | 质子数(即核电荷数)相同的一类原子的总称 | 质子数相同而中子数不同的同一元素的不同原子互称为同位素 | 具有一定数目质子和一定数目中子的一种原子 |
| 描述对象 | 宏观物质,列同类原子而言,既有游离态,又有化合态 | 微观物质,对某种元素的原子而言,因为有同位素,所以原子种类多于元素种类 | 微观物质,指某种元素的某种原子 |
| 特征 | 以单质或化合物形式存在,性质通过形成单质或化合物来体现 | 同位素化学性质几乎相同,因为质量数不同,物理性质不同。天然存在的各种同位素所占的原子个数百分比一般不变 | 具有真实的质量,不同核素的质量不相同 |
| 实例 | H、Na、S为不同的三种元素 | 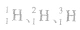 互为同位素 互为同位素 |
 是一种核素, 是一种核素, 是一种核素 是一种核素 |
中和热:
在稀溶液中,酸和碱发生中和反应生成1molH2O时的反应热。中和热的表示方法: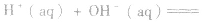
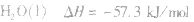
在稀溶液中,酸和碱发生中和反应生成1molH2O时的反应热。中和热的表示方法:
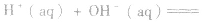
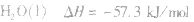
影响中和热测定的因素:
中和反应巾放出的热量为(m1+m1)·c·(t1-t2),其巾溶液的比热容c是已知的,对于给定的反应物的质量m1和m2也是定值,这样求算出的中和热是否接近 57.3kl·mol-1,取决于溶液温度的变化。
在整个实验过程中应把好两关:①隔热关。如:小烧杯周围的泡沫塑料要填满;盖板上两孔只要正好使温度计和环形玻璃搅拌棒通过即可;倒人NaOH溶液要迅速等,尽可能减少实验过程中热量的散失。②准确关。如:配制溶液的浓度要准;NaOH溶液要新制,因为久置的NaOH溶液可能变质导致浓度不准;量取液体体积时读数要准;对溶液温度要读到最高点。
注意事项:
(1)这里的溶液一般要求是稀溶液,这是因为浓酸溶液和浓碱溶液相互稀释时会放出热量
(2)强酸与强碱的反应实质是H+和OH-反应(即与酸、碱的种类无关),通过多次实验测定,1molH+和1molOH-反应生成lmol H2O(l)时,放出的热量为 57.3kJ
(3)中和热是以生成1molH2O为基准的,因此表示中和热的热化学方程式中,水的化学计量数为1,酸、碱的化学计量数可以为分数
能量的相互转化:
化学反应中的能力变化表现为热量的变化。常见能量转化有:化学能和电能的相互转化、化学能和热能的相互转化、化学能和光能、风能的相互转化等。
如:燃料燃烧产生能量最终带动发电机发电,将化学能转化为电能;铜、锌形成原电池,将化学能转化为电能。
发现相似题
与“下列说法正确的是( )A.酸与碱发生中和反应所放出的热量称...”考查相似的试题有:
- 邓小平说过“中东有石油,中国有稀土”。14462Sm与15062Sm是稀土元素,下列有关说法不正确的是[ ]A.14462Sm与15062Sm互为同位...
- 真空碳热还原—氯化法可实现由铝土矿制备金属铝,其相关反应的热化学方程式如下:Al2O3(s)+AlCl3(g)+3C(s)3AlCl(g)+3CO(g) ΔH="...
- (1)医疗上常用浓度为75%的某有机物水溶液作皮肤消毒液。该有机物的结构简式是 。(2)一定条件下,0.1mol氨气与氧气反应生...
- 2010年10月1日,我国在西昌卫星发射中心成功发射“嫦娥二号”。嫦娥二号火箭推进器以联氨(N2H4)为燃料、过氧化氢为助燃剂。已知...
- 下列变化中生成物的总能量大于反应物的总能量的是A.H + H = H—HB.H—Cl =" H" + ClC.Mg + 2HCl = MgCl2+ H2↑D.H2SO4+ 2NaO...
- 下列关于放热反应的说法中错误的是 ( ) A.放热反应生成物分子成键时释放的总能量大于反应物分子断键时吸收的总能量B.放热...
- 以下说法不正确的是( )A.利用生物质能就是间接利用太阳能B.镁条燃烧时,化学能部分转化为热能C.食物腐败是吸热反应D.回...
- (6分)由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视。目前工业上有一种方...
- 对于反应:2X+Y2Z(正反应为放热反应),若升高温度则能使( )A.反应速率不变,Z的产量减少B.反应速率增大,Z的产量增大C.反...
- 已知反应A+B=C+D的能量变化如图所示,下列说法正确的是( )A.该反应为放热反应B.该反应为吸热反应C.反应物的总能量高于...