本试题 “(1)20℃时,小苏打的溶解度为9.6g,则小苏打属于______物质.(选填易溶、可溶、微溶或难溶)(2)可燃物燃烧必须同时具备两个条件:______和______.” 主要考查您对物质的溶解性与溶解度的关系
燃烧与燃烧的条件
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 物质的溶解性与溶解度的关系
- 燃烧与燃烧的条件
物质溶解性的概念:
物质的溶解性表示在某温度和压强下,一种物质在另一种物质里溶解能力的大小。
影响因素:
溶解性的大小与溶质,溶剂的性质(内因)有关,也与温度,压强(外因)有关。
如:食盐易溶于水,却不易溶于油脂,油脂易溶于汽油里,却不易溶解在水里;气体溶质的溶解性与压强, 温度有关,而固体、液体溶质的溶解性一般只与温度有关,不考虑压强。
表示方法:
溶解性即溶解能力的大小,常用易溶、可溶、微溶和难溶来表示。
物质溶解性和溶解度的关系:
①20℃时,根据各物质在水中的溶解度的大小,经物质的溶解性分类:
②数周记忆法:
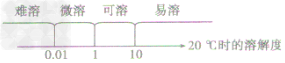
③绝对不溶于水的物质是不存在的。习惯上把难溶物质叫做“不溶”物质。
溶解性和溶解度的理解:
溶解性和溶解度都是物质的一种物理性质,不因溶质和溶剂的多少而改变,但与溶剂和溶质的性质有关,并受温度的影响。溶解性只是一般地说明某种物质在水里溶解能力的大小。通常用难溶(或不溶)、微溶、可溶、易溶等较粗略的概念表示;溶解度是衡量物质在某种溶剂里溶解性大小的尺度,是溶解性定量的表示方法。
物质的溶解性表示在某温度和压强下,一种物质在另一种物质里溶解能力的大小。
影响因素:
溶解性的大小与溶质,溶剂的性质(内因)有关,也与温度,压强(外因)有关。
如:食盐易溶于水,却不易溶于油脂,油脂易溶于汽油里,却不易溶解在水里;气体溶质的溶解性与压强, 温度有关,而固体、液体溶质的溶解性一般只与温度有关,不考虑压强。
表示方法:
溶解性即溶解能力的大小,常用易溶、可溶、微溶和难溶来表示。
物质溶解性和溶解度的关系:
①20℃时,根据各物质在水中的溶解度的大小,经物质的溶解性分类:
| 溶解度/g | <0.01 | 0.01-1 | 1-10 | >10 |
| 溶解性 | 难溶 | 微溶 | 可溶 | 易溶 |
②数周记忆法:

③绝对不溶于水的物质是不存在的。习惯上把难溶物质叫做“不溶”物质。
溶解性和溶解度的理解:
溶解性和溶解度都是物质的一种物理性质,不因溶质和溶剂的多少而改变,但与溶剂和溶质的性质有关,并受温度的影响。溶解性只是一般地说明某种物质在水里溶解能力的大小。通常用难溶(或不溶)、微溶、可溶、易溶等较粗略的概念表示;溶解度是衡量物质在某种溶剂里溶解性大小的尺度,是溶解性定量的表示方法。
概念:
燃烧是指可燃物与氧气发生的一种发光放热的剧烈的氧化反应。
燃烧的三个条件:
物质具有可燃性,可燃物与氧气接触,温度达到可燃物的着火点
促进物质燃烧的方法:
(1)增大氧气的浓度
(2)增大可燃物与氧气的接触面积
对燃烧概念的理解:
通常所说的燃烧是一种可燃物与空气中的氧气发生的一种发光、发热的剧烈的氧化反应。但实际上燃烧并不一定有氧气参加,任何发光、发热的剧烈化学反应都可称之为“燃烧”。
如2Mg+CO2
 2MgO+C;2Na+Cl2
2MgO+C;2Na+Cl2 2NaCl
2NaCl燃烧与发光,放热,火焰之间的关系:
(1)燃烧与发光,放热的关系
燃烧一定发光,放热,但发光,放热的变化不一定是化学变化,因而不一定是燃烧,如原子弹,氢弹的爆炸。
(2)燃烧与火焰的关系
火焰是气体物质燃烧所特有的现象、液体物质的燃烧主要是其蒸气的燃烧,因而产生火馅。若固体物质的沸点较高.燃烧时无蒸气逸出,则无火焰,如铁勺燃烧:若固体物质的沸点较低,燃烧时有蒸气逸出,就有火馅,如钠、硫的燃烧。
(3)发光与放热的关系
化学反应瞬间放出热量较多时.就以光的形式出现,反之则不发光,因此,发光一定收热,放热不一定发光。燃烧反应是既发光又放热的反应,单一的发光或放热反应不一定是燃烧。
影响物质着火点的因素:
着火点不是同定不变的。对同体燃料来说,着火点的高低跟表面积的大小、材料的粗细、导热系数的大小有关系。颗粒越细,表而积越大.导热系数越小,着火点越低,所以块状的木材难点燃,向木材的刨花很好点燃。对于液体燃料和气体燃料来说,火焰接触它们的情况和外界压强的大小有关系,所以测定物质的着火点对外界条件有一定标准。
(1)内在因素
可燃物的性质,不同种物质燃烧的现象不同。例如,硫在空气中燃烧发出淡监色火焰,细铁丝在空气中却不能燃烧。
(2)外部因素
①与氧气的接触面积越大,燃烧越剧烈,如煤的燃烧经历了煤块→煤球→蜂窝煤的过程,蜂窝煤能使煤更充分燃烧的原因是与空气的接触面积增大;如俗语说“人要实,火要虚”。
②氧气的浓度越大,燃烧就越剧烈。如硫在空气燃烧发出淡蓝色火焰,而在氧气中燃烧发出蓝紫色火焰。可燃物在纯氧中比在空气中燃烧会更剧烈。
燃烧的利与弊
燃烧会放出入量,人类需要的大部分能量来源于化石燃料的燃烧.人类利用燃烧放出的热量,可以做饭、取暖、发电、冶烁金属等,但燃蛲也有不利的地方,燃料燃烧不充分时,不仅产生的热量少,浪费资源,而且还会产生CO等物质,污染环境
发现相似题
与“(1)20℃时,小苏打的溶解度为9.6g,则小苏打属于______物质...”考查相似的试题有:
- 在室温下,某物质的溶解度为3克,则该物质是[ ]A、易溶物质B、可溶物质C、微溶物质D、难溶物质
- 下列气体与空气混合后遇明火,可能发生爆炸的是A.氧气B.氮气C.氢气D.二氧化碳
- 2007年10月24日是值得每位炎黄子孙永远骄傲的日子:“嫦娥一号”成功发射,中国人民开始踏上了探月之旅.下面关于发射“嫦娥一号...
- 央视新闻报道称,河南某农民因焚烧秸秆导致火势蔓延,烧毁了相邻的20亩小麦。专家称遇到这种情况可用农机具设置“防火隔离带”...
- 下述实验操作正确,并能达到实验目的是( )A.探究CO2性质B.验证空气中O2含量C.探究燃烧的三个条件D.稀释浓硫酸
- (2分)某校初三学生去野外野炊: (1)野炊活动中,东东引燃细枯枝后,迅速往灶里塞满枯枝,结果燃烧不旺,并产生很多浓烟,...
- 2008年北京成功举办了第29届奥运会,奥运圣火在“鸟巢”上空熊熊燃烧。请回答下列问题:(1)奥运圣火燃烧的三个条件是:①有可...
- 白磷的着火点为40℃,把一块白磷投入到盛80℃水的烧杯中,白磷却不燃烧,为什么?采用什么方法能使白磷在水中燃烧起来?
- 向沸水中加入一块白磷,白磷不能燃烧的原因是( )A.没有点燃B.未与氧气接触C.温度没有达到着火点D.水的温度太低
- 根据你的生活经验和所学的化学知识,判断下列做法(或说法)不正确的是A.油锅着火时,迅速盖上锅盖B.用洗洁精洗去餐具上的...