本试题 “(12分)在80℃时,将0.40 mol的N2O4气体充入1 L固定容积的密闭容器中发生反应:N2O42NO2(ΔH>0),每隔一段时间对容器内的物质进行测定,得到如下数据:时间...” 主要考查您对化学反应速率的定义、公式
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 化学反应速率的定义、公式
化学反应速率:
1.定义:化学反应速率是用来衡量化学反应进行的快慢程度的物理量。
2.表示方法:在容积不变的反应器中,通常用单位时间内反应物浓度的减少或生成物浓度的增加来表示。即: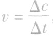
3.单位:mol·L-1·s-1或mol·L-1·min-1等。
4.注意:
(1)化学反应速率是指一段时间内的平均速率,而不是瞬时速率;通常前一段时间的平均反应速率要快于后一段时间的平均反应速率,反应速率均取正值,即v>0。
(2)在一定温度下,固体和纯液体物质单位体积的物质的量保持不变,即物质的量浓度为常数,因此在表示化学反应速率时,不代入固体或纯液体物质的浓度。浓度是指气体或溶液的浓度。
(3)同一个化学反应在相同的条件下、在同一段时间内,用不同物质表示反应速率时,数值可能相同也可能不同,但表达的意义都相同,即反应的快慢程度是一样的。
(4)在同一反应巾用不同的物质来表示反应速率时,其数值之比等于化学方程式中各物质的化学计量数之比.
如化学反应: ,
,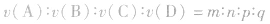 ,所以
,所以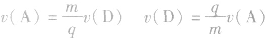
发现相似题
与“(12分)在80℃时,将0.40 mol的N2O4气体充入1 L固定容积的密...”考查相似的试题有:
- 某反应X+3Y=2Z+2P在甲、乙、丙、丁四种不同条件下测得的反应速率为: 甲: 乙: 丙: 丁: 则反应进行最快的是( ) A.甲...
- 锌和稀硫酸反应,欲想加快反应速率,应选择下列组合中的哪个反应条件①锌粒②锌片③锌粉④10%的稀硫酸⑤15%的稀硫酸⑥20%的稀硫酸⑦...
- 把0.4mol X气体和0.6mol Y气体混合于2L密闭容器中,使它们发生如下反应:4X(g)+5Y(g)=n Z(g)+6W(g).2min 末已生成0....
- 某一反应物的浓度是2.0 mol·L-1,经过4 min后,它的浓度变成1.68 mol·L-1,则在这4 min内它的平均反应速率为( )A.0.2 mol·L-1·m...
- 化合物Bilirubin在一定波长的光照射下发生分解反应,反应物浓度随反应时间变化如右图所示,计算反应4~8min间的平均反应速率 ...
- 某合作小组同学将铜片加入稀硝酸,发现开始时反应非常慢,一段时间后反应速率明显加快。该小组通过实验探究其原因。(1)该反...
- 室温下,将 4 mol A 气体和 2 mol B 气体在 2 L 的密闭容器中混合并在一定条件下发生如下反应:2A(g)+B(g)XC(g),经 2 ...
- 通过实验方法测得H2+Cl2= 2HCl的化学反应速率v和反应物浓度c的关系式为:v =" k" ·c(H2)m·c(Cl2)n。式中k为常数,m、n的数值...
- 在一定条件下,在容积为2L的密闭容器中,将2mol气体M和3mol气体N混合,发生如下反应:2M(g)+ 3N(g)x Q(g)+3R(g),经2min达平...
- 在一容积为2L的密闭容器中,充入4mol氮气和12mol氢气,使其在一定条件下发生反应:N2(g)+3H2(g) 2NH3(g),2min末测得NH3为0.8...