本试题 “下列叙述错误的是[ ]A.加热能杀死流感病毒是因为病毒的蛋白质受热变性B.人造纤维、含成纤维和光导纤维都是有机高分子化合物C.在汽车排气管上加装“催化转化...” 主要考查您对胶体
蛋白质
合成有机高分子化合物
大气污染、改善大气质量
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 胶体
- 蛋白质
- 合成有机高分子化合物
- 大气污染、改善大气质量
胶体:分散质粒子直径在10-9m~10-7m之间的分散系胶粒直径的大小是胶体的本质特征
胶体可分为固溶胶、液溶胶、气溶胶
①常见的液溶胶:Fe(OH)3、AgI、牛奶、豆浆、粥等
②常见的气溶胶:雾、云、烟等;
③常见的固溶胶:有色玻璃、烟水晶等胶体的性质:
丁达尔效应:
①当光束通过氢氧化铁胶体时,可以看到一条光亮的通路,这条光亮的通路是由于胶体粒子对光线散射(光波偏离原来方向而分散传播)形成的,即为丁达尔效应。
②布朗运动:粒子在不停地、无秩序的运动
③电泳:胶体粒子带有电荷,在电场的作用下,胶体粒子在分散剂里定向移动。一般来讲:金属氢氧化物,金属氧化物的胶粒吸附阳离子,胶体微粒带正电荷;非金属氧化物,金属硫化物的胶体胶粒吸附阴离子,胶体微粒带负电荷。
④胶体聚沉:向胶体中加入少量电解质溶液时,由于加入的阳离子(或阴离子)中和了胶体粒子所带的电荷,使胶体粒子聚集成为较大的颗粒,从而形成沉淀从分散剂里析出。该过程不可逆。
胶体的特性:
(1)丁达尔效应当一束光通过胶体时,胶体内会出现一条光亮的通路,这是由胶体粒子对光线散射而形成的,利用丁达尔效应可区分胶体和浊液。
(2)介稳性:胶体的稳定性介于溶液和浊液之间,在一定条件下能稳定存在,但改变条件就有可能发生聚沉。
(3)聚沉:给胶体加热、加入电解质或加入带相反电荷的胶体颗粒等均能使胶体粒子聚集成较大颗粒,从而形成沉淀从分散剂里析出。聚沉常用来解释生活常识,如长江三角洲的形成、明矾净水等。
(4)电泳现象:在电场作用下,胶体粒子在分散剂中作定向移动。电泳现象说明胶体粒子带电。电泳常用来分离提纯胶体,如工业上静电除尘。
分散系比较:
| 分散系 | 溶液 | 胶体 | 悬浊液 | 乳浊液 |
| 分散质粒子大小 | <1nm | 1~100nm | >100nm | >100nm |
| 分散质粒子结构 | 分子、离子 | 少量分子的结合体或大分子 | 大量分子聚集成的固体小颗粒 | 大量分子聚集成的液体小液滴 |
| 特点 | 均一、透明、稳定 | 多数均一、透明、较稳定 | 不均一、不透明、久置沉淀 | 不均一、不透明、久置分层 |
| 能否透过滤纸 | 能 | 能 | 不能 | —— |
| 实例 | 食盐水、蔗糖溶液 | Fe(OH)3(胶体)、淀粉胶体 | 泥水、石灰乳 | 牛奶、油漆 |
胶体发生聚沉的条件:
因胶粒带电,故在一定条件下可以发生聚沉:
- 向胶体中滴加电解质
- 向胶体中加入带相反电荷胶粒的胶体
- 加热
常见的胶体的带电情况:
- 胶粒带正电荷的胶体有:金属氧化物、金属氢氧化物。例如Fe(OH)3、Al(OH)3等。
- 胶粒带负电荷的胶体有:非金属氧化物、金属硫化物、硅酸胶体、土壤胶体。
- 胶粒不带电的胶体有:淀粉胶体。
- 特殊的,AgI胶粒随着AgNO3和KI相对量不同,而带正电或负电。若KI过量,则AgI胶粒吸附较多I-而带负电;若AgNO3过量,则因吸附较多Ag+而带正电。
注意:胶体不带电,而胶粒可以带电。
Fe(OH)3胶体的制备:
操作步骤:将烧杯中的蒸馏水加热至沸腾,向沸水中滴加5~6滴饱和FeCl3溶液,继续煮沸至呈红褐色为止。
离子方程式:Fe3++3H2O=(加热)=Fe(OH)3(胶体)+3H+
点拨:(1)淀粉溶液、蛋白质溶液虽叫做溶液,但属于胶体。
(2)胶体可以是液体,也可以是固体、气体,如烟、云、雾、有色玻璃等。
蛋白质:
相对分子质量在10000以上的,并具有一定空间结构的多肽,称为蛋白质。
组成:蛋白质是南C、H、O、N、S等元素组成的结构复杂的化合物。
蛋白质的性质:
(1)两性
由于形成蛋白质的多肽是由多个氨基酸分子脱水形成的,在多肽链的两端必有一NH2和一COOH,因此蛋白质既能与酸反应,又能与碱反应,表现为两性。
(2)水解
反应蛋白质在酸、碱或酶的作用下,水解生成相对分子质量较小的肽类化合物,最终逐步水解得到各种氨基酸。
(3)盐析
向蛋白质溶液巾加入某些无机盐(如硫酸铵、硫酸钠和氯化钠等)达到一定浓度时,会使蛋白质的溶解度降低而从溶液中析出,这种作用称为盐析。
注意:盐析只改变蛋白质的溶解度,没有改变它的化学性质,析出的蛋白质还能溶于水,故盐析是可逆的过程。
(4)变性
在某些物理因素(如加热、加压、搅拌、紫外线照射和超声波等)或化学因素(如强酸、强碱、重金属盐、三氯乙酸、甲醛、乙醇和丙酮等)的影响下,蛋白质的理化性质和生理功能发生改变的现象,称为蛋白质的变性。
注意:蛋白质的变性是一个不可逆过程,变性后的蛋白质在水中不能重新溶解,同时也会失去原有的生理活性。
(5)蛋白质的颜色反应
蛋白质可以与许多试剂发生颜色反应,如硝酸可以使含有苯环结构的蛋白质变黄,这是含苯环的蛋白质的特征反应,常用来鉴别部分蛋白质。在使用浓硝酸时,不慎将浓硝酸溅在皮肤上而使皮肤发黄,就是蛋白质发生颜色反应的结果。
(6)蛋白质的灼烧
蛋白质在灼烧时产生烧焦羽毛的气味,可以据此鉴别真丝和人造丝。
能够发生水解反应的物质归纳:
1.盐类水解
(1)强酸弱碱盐水解呈酸性,如CuSO4、NH4NO3、 FeCl3、Al2(SO4)3等。
(2)强碱弱酸盐水解呈碱性,如KF、Na2CO3、 K2SiO3、NaAlO2等。
2.氮化镁的水解 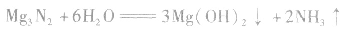
3.碳化钙的水解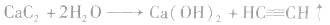
4.卤代烃的水解卤代烃水解生成醇,如 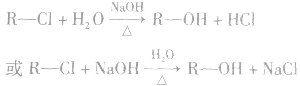
5.酯的水解 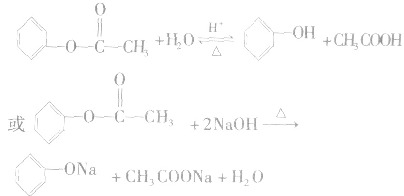
6.糖类水解糖类水解的最终产物是单糖,如 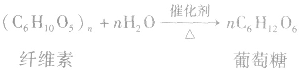
7.蛋白质的水解蛋白质水解的最终产物足多种氨基酸,肽键的断裂如下图所示: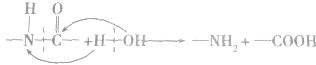
合成有机高分子化合物:
由千百个原子彼此以共价键结合形成相对分子质量特别大、具有重复结构单元的有机化合物。是由一类相对分子质量很高的分子聚集而成的化合物,也称为高分子、大分子等。一般把相对分子质量高于10000的分子称为高分子。包括天然和合成有机高分子化合物。常见合成有机高分子化合物:聚乙烯、聚氯乙烯等
有机高分子化合物的合成:
高分子化合物大部分是由小分子通过聚合反应制得的。
(1)加聚反应:不饱和单体通过加聚反应生成高分子化合物。
①聚乙烯类(塑料、纤维)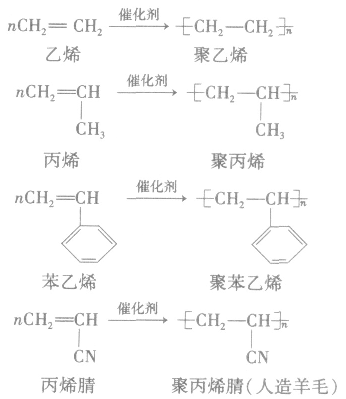
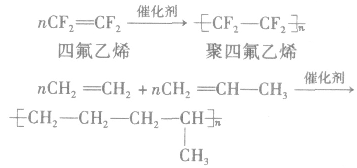
②聚二烯类(橡胶)
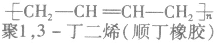
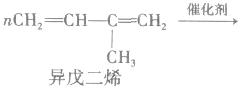
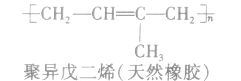
(2)缩聚反应:单体聚合成高分子的同时有小分子生成的聚合反应。
①聚酯类 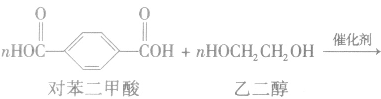
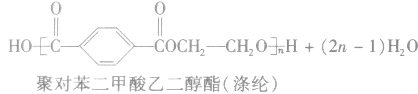
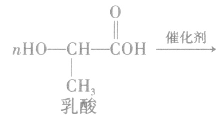
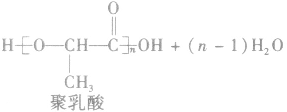
②聚氨基酯类
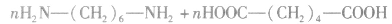
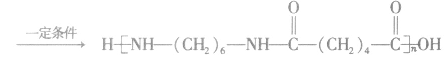
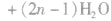

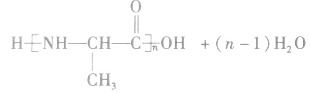
③酚醛树脂类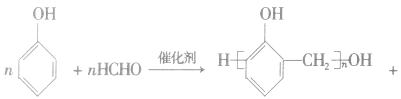
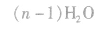
对高分子化合物的理解:
(1)通常把生成高分子化合物的低分子化合物(反应物)叫做单体(如乙烯是聚乙烯的单体),高分子化合物中化学组成相同、可重复的最小单位叫做链节(如一CH2一CH2一是聚乙烯的链节),高分子链中含有链节的数目叫做聚合度,通常用n表示。注意单体与链节是不同的,单体是反应前的低分子化合物;链节不是物质,不能独立存在,是反应后有机高分子化合物中的片段。 (2)低分子有机物的相对分子质量都有一个确定的数值,而高分子化合物的相对分子质量只是一个平均值。它是以低分子有机物作原料,经聚合反应得到各种相对分子质量不等的物质的混合物。
单体与高分子化合物的互推规律:
聚合时找准结合点,反推单体时找准分离处,“结合点必为分离处”。
1.由单体推断高聚物的方法
(1)单烯烃型单体加聚时,“断开双键,键分两端,添上括号,n写后面”。如

(2)二烯烃型单体加聚时,“单变双,双变单,破两头,移中间,添上括号.n写后面”。如
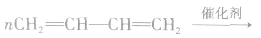
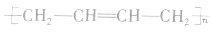
(3)分别含有一个双键的两种单体聚合时,“双键打开,中间相连,添上括号,n写后面”。如 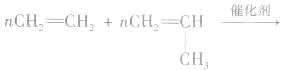
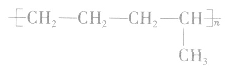
2.由高聚物推导单体的方法
(1)加聚产物单体的判断方法
①凡链节主链只有两个碳原子(无其他原子)的聚合物,其合成单体必为一种,将两个半键闭合即可。如
②凡链节主链有四个碳原子(无其他原子),且链节无双键的聚合物,其单体必为两种,在中央画线断开,然后两键闭合即可。如
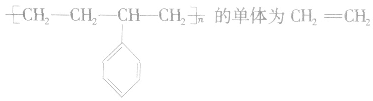
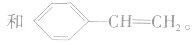
③凡链节主链上只有碳原子,斤存在碳碳双键结构的高聚物,其规律是“凡双键,四个碳;无双键,两个碳”画线断开。如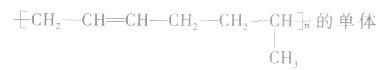
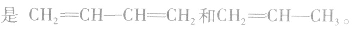
(2)缩聚产物单体的判断方法
①酯类高聚物中含有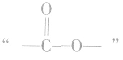 ,它的单体有两种,从
,它的单体有两种,从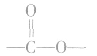 中间断开,
中间断开,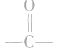 恢复为
恢复为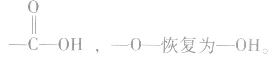
如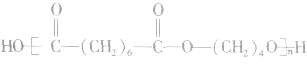 的单体为
的单体为
②酰胺类高聚物中含有"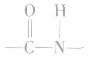 ",它的单体有两种,在亚氨基氮原子上加氢,羰基碳原子上加羟基,即得高聚物的单体。如
",它的单体有两种,在亚氨基氮原子上加氢,羰基碳原子上加羟基,即得高聚物的单体。如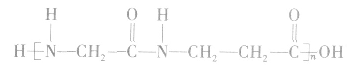 的单体为
的单体为
结构为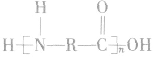 的高聚物,其合成单体必为一种,在亚氨基氮原子上加氢,在羰基碳原子上加羟基即得高聚物的单体。 如
的高聚物,其合成单体必为一种,在亚氨基氮原子上加氢,在羰基碳原子上加羟基即得高聚物的单体。 如 的单体为
的单体为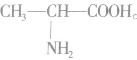
③酚醛树脂是由苯酚和甲醛缩聚而成的,链节中有酚羟基的结构。
如 和
和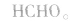
(1)大气污染源:颗粒物、硫的氧化物、氮的氧化物、CO 碳氢化合物、氟氯代烷
(2)大气污染危害:危害人体健康、影响动植物的生长、严重时会影响地球的气候
(3)全球性三大环境问题:酸雨、臭氧层受损、温室效应
①酸雨:正常雨水:PH约为5.6 酸雨:PH小于5.6 我国为硫酸型酸雨,烧煤炭造成
硫酸型:硫的氧化物转化 SO2+H2O=H2SO3 2H2SO3+O2=2H2SO4 大气中烟尘和O3作催化剂
硝酸型:氮的氧化物转化 3NO2+H2O=2HNO3+NO↑
②臭氧层:自然界的臭氧90%集中在距地面15-50km的大气平流层中 吸收自太阳的大部分紫外线
引起臭氧层受损物质 氟氯代烷(致冷剂)、哈龙(含溴的灭火剂)、CCl4、N2O、NO、核弹爆炸产物
保护臭氧层公约:《保护臭氧层维也纳公约》 《关于消耗臭氧层物质的蒙特利尔议定书公约》
③温室效应:太阳短波辐射可以透过大气射入地面,而地面增暖后放出的长短辐射却被大气中的二氧化碳等物质所吸收,从而产生大气变暖的效应
温室效应后果:荒漠将扩大,土地侵蚀加重,森林退向极地,旱涝灾害严重,雨量将增加7-11%;温带冬天更湿,夏天更旱;热带也将变得更湿,干热的副热带变得更干旱,两极冰块将熔化,使海平面上升1米多,引起厄尔尼诺现象
引起温室效应的物质:CO2、CH4、N2O、氟氯代烷
改善大气质量:
①减少煤等化石燃料燃烧产生污染:改善燃煤质量、改进燃烧装置、技术和排烟设备、发展洁净煤技术和综合利用、调整和优化能源结构
煤的综合利用: 煤的的干馏、煤的气化、煤的液化
煤的气化 C+H2O(g)=CO+H2
煤的液化 CO+2H2→CH3OH
煤的脱硫 2CaCO3+O2+2SO2=2CaSO4+2CO2
②减少汽车等机动车尾气污染
尾气污染(占大气污染排出总量的40-50%):CO、NO2、NO、碳氢化合物
使用无铅汽油:四乙基铅作抗爆震剂,铅对神经系统损害大
尾气系统加催化转化器:前半部 2CO+2NO2
 CO2+N2 后半部 2CO+O2
CO2+N2 后半部 2CO+O2 2CO2 C7H16+11O2
2CO2 C7H16+11O2 7CO2+8H2O
7CO2+8H2O与“下列叙述错误的是[ ]A.加热能杀死流感病毒是因为病毒的蛋白...”考查相似的试题有:
- 已知由AgNO3溶液和稍过量的KI溶液制得的碘化银胶体与氢氧化铁溶胶混合时,会析出AgI和Fe(OH)3的混合沉淀。由此可知( )①该Ag...
- 胶体区别于其它分散系的本质特征是A.分散质粒子的直径在1~100 nm之间B.久置不分层C.能透过滤纸D.有丁达尔效应
- 胶体区别于其他分散系的本质特征是( )A.光束穿过胶体时形成一条光亮的“通路”B.胶体微粒可以透过滤纸C.胶体微粒大小在1~...
- 下列关于胶体的叙述不正确的是[ ]A.胶体区别于其他分散系的本质特征是分散质的微粒直径在10-9~10-7m之间B.光线透过胶体时,...
- 把新制 Cu(OH)2悬浊液加入某人的尿液中,微热时如果观察到红色沉淀,说明该人患有下列哪种疾病A.高血糖症B.高血脂症C.尿路...
- 按照绿色化学的原则,最理想的“原子经济”就是反应物的原子全部转化为期望的最终产物。下列生产乙醇的反应中,原子利用率最高...
- 为了保护臭氧层,可采取的有效措施是( )A.减少二氧化硫的排放B.减少卤代烃的排放C.减少废气的含铅量D.减少二氧化碳的排放
- “人类只有一个地球!”,为了保护人类赖以生存的环境,下列做法中不正确的是( )A.回收处理垃圾,变废为宝B.废旧电池中含有...
- 下列产品的使用不会对环境造成污染的是[ ]A.含磷洗衣粉B.酒精C.氟里昂D.含汞电池
- 我国重点城市近年来已发布“空气质量日报”。下列物质中不列入首要污染物的是A.二氧化硫B.二氧化氮C.二氧化碳D.可吸入颗粒物