本试题 “在密闭容器中进行反应X2(g)+3Y2(g)⇌2Z2(g),若X2、Y2、Z2的起始浓度分别为0•1mol/L、0•3mol/L、0•2mol/L,达到平衡时下列物质的浓度可能为( )A.X2为...” 主要考查您对化学反应进行的方向
可逆反应与不可逆反应
勒夏特列原理
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 化学反应进行的方向
- 可逆反应与不可逆反应
- 勒夏特列原理
化学反应的方向与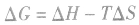 :
:
1.化学反应进行方向的判据
(1)由稳定性弱的物质向稳定性强的物质转变
如 ,稳定性
,稳定性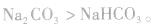
(2)离子反应总是向着使反应体系中某些离子浓度减小的方向进行
①溶解度大的物质向溶解度小的物质转变,如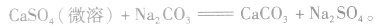
②由相对强酸(碱)向相对弱酸(碱)转变,如 ,
,  所以酸性强弱:
所以酸性强弱: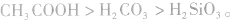
(3)由难挥发性物质向易挥发性物质转变
如 所以沸点:
所以沸点: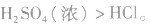
(4)由氧化性(还原性)强的物质向氧化性(还原性)弱的物质转变
如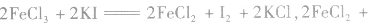
 ,则氧化性:
,则氧化性: 。
。
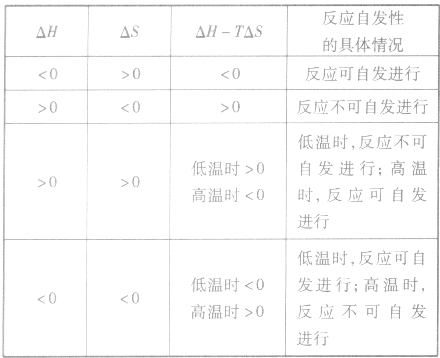
2.焓变和熵变共同判断反应的方向:
在温度、压强一定的条件下,自发反应总是向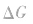
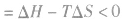 的方向进行,直至达到平衡状态;
的方向进行,直至达到平衡状态;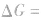
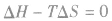 表明反应已达到平衡状态;
表明反应已达到平衡状态;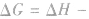
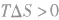 表明反应不能自发进行。
表明反应不能自发进行。
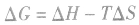 :
:1.化学反应进行方向的判据
(1)由稳定性弱的物质向稳定性强的物质转变
如
 ,稳定性
,稳定性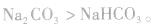
(2)离子反应总是向着使反应体系中某些离子浓度减小的方向进行
①溶解度大的物质向溶解度小的物质转变,如
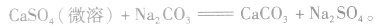
②由相对强酸(碱)向相对弱酸(碱)转变,如
 ,
,  所以酸性强弱:
所以酸性强弱: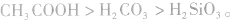
(3)由难挥发性物质向易挥发性物质转变
如
 所以沸点:
所以沸点: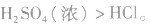
(4)由氧化性(还原性)强的物质向氧化性(还原性)弱的物质转变
如
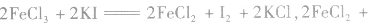
 ,则氧化性:
,则氧化性: 。
。 2.焓变和熵变共同判断反应的方向:
在温度、压强一定的条件下,自发反应总是向
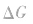
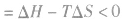 的方向进行,直至达到平衡状态;
的方向进行,直至达到平衡状态;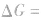
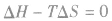 表明反应已达到平衡状态;
表明反应已达到平衡状态;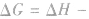
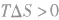 表明反应不能自发进行。
表明反应不能自发进行。
可逆反应与不可逆反应:
(1)可逆反应:在同一条件下,既能向正反应方向进行,同时又能向逆反应方向进行的反应。
注:①在可逆反应中,由反应物到生成物的反应叫正反应;由生成物到反应物的反应叫逆反应。
②可逆反应必须是“同一条件”。
(2)不可逆反应:在不同条件下能向两个方向进行的反应为不可逆反应。如:点燃情况下,氢气和氧气能生成水;在通电条件下,水电解能生成氢气和氧气。
可逆反应的特点:
①可逆反应必须是同一条件下既能向正反应方向又能向逆反应方向进行的反应,对于在不同条件下向正、逆反直方向进行的反应则不能认为是可逆反应。
②可逆反应是不能进行到底的,不能实现完全转化
(1)可逆反应:在同一条件下,既能向正反应方向进行,同时又能向逆反应方向进行的反应。
注:①在可逆反应中,由反应物到生成物的反应叫正反应;由生成物到反应物的反应叫逆反应。
②可逆反应必须是“同一条件”。
(2)不可逆反应:在不同条件下能向两个方向进行的反应为不可逆反应。如:点燃情况下,氢气和氧气能生成水;在通电条件下,水电解能生成氢气和氧气。
可逆反应的特点:
①可逆反应必须是同一条件下既能向正反应方向又能向逆反应方向进行的反应,对于在不同条件下向正、逆反直方向进行的反应则不能认为是可逆反应。
②可逆反应是不能进行到底的,不能实现完全转化
原理内容:
如果改变影响平衡的一个条件(如浓度、压强、温度),平衡将向着能够减弱这种改变的方向移动。勒夏特列原理又叫平衡移动原理。
适用范围:
平衡移动原理适用于化学平衡、溶解平衡、电离平衡、水解平衡等动态平衡。
注意事项:
(1)平衡向“减弱”外界条件变化的方向移动,但不能“抵消”外界条件的变化。
(2)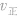 增大并不意味着平衡一定向正反应方向移动,只有
增大并不意味着平衡一定向正反应方向移动,只有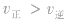 时才可以肯定平衡向正反应方向移动。
时才可以肯定平衡向正反应方向移动。
(3)当平衡向正反应方向移动时,反应物的转化率并不一定提高,生成物的体积分数也并不一定增大(因为反应物或反应混合物的总量增大了),增大一种反应物的浓度会提高另一种反应物的转化率。
(4)存在平衡且平衡发生移动时才能应用平衡移动原理。
分析思路:
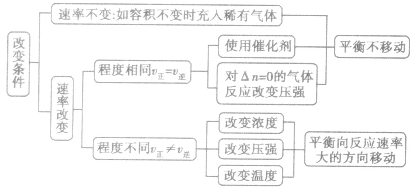
如果改变影响平衡的一个条件(如浓度、压强、温度),平衡将向着能够减弱这种改变的方向移动。勒夏特列原理又叫平衡移动原理。
适用范围:
平衡移动原理适用于化学平衡、溶解平衡、电离平衡、水解平衡等动态平衡。
注意事项:
(1)平衡向“减弱”外界条件变化的方向移动,但不能“抵消”外界条件的变化。
(2)
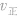 增大并不意味着平衡一定向正反应方向移动,只有
增大并不意味着平衡一定向正反应方向移动,只有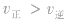 时才可以肯定平衡向正反应方向移动。
时才可以肯定平衡向正反应方向移动。 (3)当平衡向正反应方向移动时,反应物的转化率并不一定提高,生成物的体积分数也并不一定增大(因为反应物或反应混合物的总量增大了),增大一种反应物的浓度会提高另一种反应物的转化率。
(4)存在平衡且平衡发生移动时才能应用平衡移动原理。
分析思路:

发现相似题
与“在密闭容器中进行反应X2(g)+3Y2(g)⇌2Z2(g),若X2、Y2、...”考查相似的试题有:
- 下列根据化学事实进行的相关推论,正确的是 化学事实推论A某一反应需要在高温条件下才能进行该反应的△H>0B无色试液中加入氢...
- 下列关于热化学反应的描述中正确的是[ ]A.HCl和NaOH反应的中和热△H=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)...
- 下列说法不正确的是( )A.焓变是一个反应能否自发进行相关的因素,多数放热反应能自发进行B.自发进行的反应一定能迅速进行C...
- 某化学反应其△H= -122kJ·mol-1,△S=231J·mol-1·K-1,则此反应在下列哪种情况下可自发进行[ ]A.在任何温度下都能自发进行B....
- 对于化学反应能否自发进行,下列说法中错误的是[ ]A.若ΔH<0,△S>0,任何温度下都能自发进行B.若ΔH>0,△S<0,任何温度下...
- 已知热化学方程式:SO2(g)+12O2(g)⇌SO3(g)△H=-98.32kJ/mol在容器中充入2mol SO2和1mol O2充分反应,最终放出的热量为(...
- 自然界的矿物、岩石的成因和变化受到许多条件的影响.地壳内每加深1km,压强增大约25000~30000kPa.在地壳内SiO2和HF存在以...
- 一定条件下,对于可逆反应X(g)+3Y(g)═2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),到达平衡时,X、Y、Z...
- 下列事实中,不能用勒夏特列原理解释的是[ ]A.Fe(SCN)3溶液中加入固体KSCN后颜色变深B.向稀盐酸中加入少量蒸馏水,盐酸中氢...
- 下列变化不能用勒夏特列原理解释的是[ ]A.红棕色的NO2加压后颜色先变深再变浅B.H2、I2、HI混合气体加压后颜色变深C.合成氨...