本试题 “常温下,在20.0 mL 0.20 mol/L CH3COONa溶液中滴加0.20 mol/L的稀盐酸。溶液的pH的变化关系如下图所示。(1)a>7.0的理由是__________________(用离子方程式表...” 主要考查您对电离平衡常数
粒子浓度大小的比较
水解方程式
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 电离平衡常数
- 粒子浓度大小的比较
- 水解方程式
1.概念在一定条件下,弱电解质的电离达到平衡时,溶液中电离所生成的各种离子浓度的乘积与溶液中未电离的分子浓度的比是一个常数,这个常数叫做电离平衡常数,简称电离常数。用K表示(酸用
 表示,碱用
表示,碱用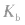 表示)。
表示)。 2.表示方法:
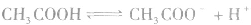
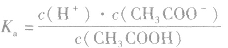
对于多元弱酸,其电离是分步进行的,每步各有电离常数,通常用
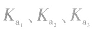 ,等分别表示,且
,等分别表示,且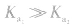
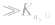
例如:
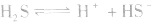
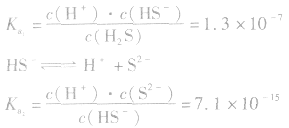
3.影响因素:温度
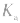 (或
(或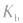 )只随温度变化而变化,不随浓度变化而变化。电离平衡常数,类似于化学平衡常数.
)只随温度变化而变化,不随浓度变化而变化。电离平衡常数,类似于化学平衡常数.4.意义:反映弱酸,弱碱酸碱性的相对强弱在一定温度下,
 越大(多元弱酸以
越大(多元弱酸以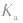 为依据),弱酸的电离程度就越大,浓度相同时c(H+)也越大,弱酸的酸性越强。
为依据),弱酸的电离程度就越大,浓度相同时c(H+)也越大,弱酸的酸性越强。离子浓度大小比较方法:
(1)考虑水解因素:如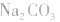 溶液
溶液 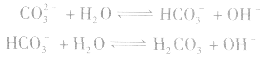
所以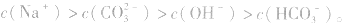
(2)不同溶液中同一离子浓度的比较要看溶液中其他离子对它的影响。如相同浓度的
 三种溶液中,
三种溶液中, 由大到小的顺序是c>a>b。
由大到小的顺序是c>a>b。
(3)混合液中各离子浓度的比较要综合分析水解因素、电离因素。如相同浓度的 的混合液中,离子浓度顺序为:
的混合液中,离子浓度顺序为: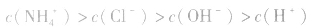
 的电离程度大于
的电离程度大于 的水解程度。
的水解程度。
盐溶液的“三大守恒”:
①电荷守恒:电解质溶液中所有阳离子所带有的正电荷数与所有的阴离子所带的负电荷数相等。如NaHCO3溶液中:
推出: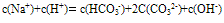
②物料守恒:电解质溶液中由于电离或水解因素,离子会发生变化变成其它离子或分子等,但离子或分子中某种特定元素的原子的总数是不会改变的。如NaHCO3溶液中nc(Na+):nc(C)=1:1,
推出: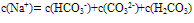
③质子守恒:电解质溶液中分子或离子得到或失去质子(H+)的物质的量应相等。例如在NH4HCO3溶液中H3O+、H2CO3为得到质子后的产物;NH3、OH-、CO32-为失去质子后的产物,故有以下关系: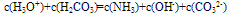
(2)粒子浓度大小比较的方法:
①单一溶液中离子浓度大小的比较
A. 一元弱酸盐溶液中离子浓度的关系是:
c(不水解离子)>c(水解离子)>c(显性离子)>c(水电离出的另一离子)
如:在CH3COONa溶液中各离子浓度大小关系: 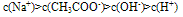
B. 二元弱酸盐溶液中离子浓度的关系是:
c(不水解离子)>c(水解离子)>c(显性离子)> c(二级水解离子)>c(水电离出的另一离子)
如:Na2CO3溶液中离子浓度的关系: 
②比较不同电解质溶液中同一种粒子浓度的大小。应注意弱酸、弱碱电离程度的大小以及影响电离度的因素,盐类水解及水解程度对该粒子浓度的影响。
③比较经过反应化学反应后离子浓度的大小:
A. 确定电解质溶液的成分
B. 确定溶液中含哪些粒子(分子、离子),此时要考虑物质的电离和水解情况
C. 确定各种粒子的浓度或物质的量的大小
D. 根据题目要求做出判断
注:要抓住“两小”。即弱电解质电离程度小,故未电离的弱电解质分子数远多于已电离出离子数目;盐的水解程度小,故未水解的粒子数目远多于水解生成的粒子数目
1、定义:表示盐水解的式子。
2、书写水解方程式的注意事项:
(1)找出盐类组成中会发生水解的离子(弱酸阴离子或弱碱阳离子),直接写出盐类水解的离子方程式。
(2)盐类的水解反应是中和反应的逆反应,中和反应的程度很大,水解反应的程度很小,故写盐类的水解反应方程式或离子方程式时,一般不写“=”而写“
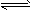 ”。
”。 (3)一般盐类水解的程度很小,水解产物也少,通常不生成沉淀或气体,也不发生分解。在书写盐类水解的离子方程式时一般不标“↑”或“↓”,也不把生成物(如NH3·H2O、H2CO3)写成其分解产物的形式。
(4)多元弱酸的盐中弱酸根离子分步水解,第一步比较容易发生,第二步比第一步难。水解时以第一步为主。多元弱酸的水解反应式应分步书写,而多元弱碱的水解反应不分步书写。
(5)某些盐溶液在混合时,由于一种盐的阳离子和另一种盐的阴离子都能发生水解,水解后溶液的性质相反,它们在一起时就能相互促进对方的水解,使两种离子的水解趋于完全。称为双水解。如:铝盐和碳酸盐混合:
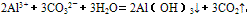 ,双水解反应中如果有复分解反应的条件(沉淀、气体、水等生成),则反应比较完全。书写时一般用“=”,标“↑”或“↓”。
,双水解反应中如果有复分解反应的条件(沉淀、气体、水等生成),则反应比较完全。书写时一般用“=”,标“↑”或“↓”。盐类水解方程式的书写:
一般来说,盐类水解的程度不大,应该用可逆号“ ”表示,盐类水解一般不会产生沉淀和气体,所以不用“↑”“↓”符号表示。
”表示,盐类水解一般不会产生沉淀和气体,所以不用“↑”“↓”符号表示。
1.一元弱酸的强碱盐和一元弱碱的强酸盐的水解。 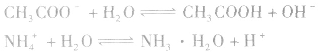
2.多元弱酸的强碱盐的水解是分步进行的,不能合并,以第一步为主。 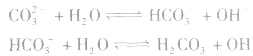
3.多元弱碱的强酸盐的水解。 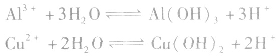
4.弱酸的铵盐的水解。 
5.完全双水解的离子间的反应用“==”表示,标明“↑”“↓”符号。如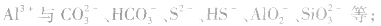


与“常温下,在20.0 mL 0.20 mol/L CH3COONa溶液中滴加0.20 mol/L...”考查相似的试题有:
- 将20 mL 0.1 mol·L-1的氨水与10 mL0.1 mol·L-1的盐酸混合,所得到的溶液中离子浓度的关系错误的是 [ ]A. c(NH4+)+c(H+)=c(OH-...
- 常温下将0.01molCH3COONa和0.004mol盐酸溶于水,配成0.5L混合溶液。(1)溶液中共有________种微粒。(2)溶液中有两种微...
- 在0.1mol/LNa2S的溶液中,下列关系不正确的是( )A.[H2S]+[HS-]+[S2-]=0.1 mol/LB.[Na+]+[H+]=2[S2-]+[HS-]+[OH-]C.[OH-]...
- 叠氮酸(HN3)与醋酸性相似,下列叙述中一定错误的是[ ]A.HN3水溶液中微粒浓度大小顺序为:c(HN3)>c(H+)>c(N3-)>c(OH-)B.HN3...
- 向体积为0.05mol·L-1CH3COOH溶液中加入体积为Vb的0.05mol·L-1KOH溶液,下列关系错误的是[ ]A.Va>Vb时:c(CH3COOH) +c(CH3COO...
- 运用化学反应原理研究以下问题:(1)合成氨反应N2(g)+3H2(g)2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,平...
- 下列说法正确的是A.NaHCO3溶液加水稀释,c(Na+)/c(HCO3-)的比值保持增大B.1 mol·L-1的NH4Cl溶液中含有NH4+的数目一定小于...
- 下列叙述正确的是( )A.0.1 mol·L-1氨水中,c(OH-)=c()B.0.1 mol·L-1NH4Cl溶液中,c(H+)=c(NH3·H2O)+c(OH-)C.0.1 mol·L...
- 25℃时,向10mL 0.01mol/L KOH溶液中滴加0.01mol/L苯酚溶液,混合溶液中粒子浓度关系正确的是( )A. pH>7时,c(C6H5O-)>c(K+...
- ⑴下列物质属于非电解质的是 ,属于弱电解质的是 (填序号)。①氨水 ②SO2 ③CI2 ④次氯酸 ⑤BaSO4 ⑥乙醇 ⑦H2O ⑧NaHCO3⑵用浓度为0....