本试题 “一些烷烃的燃烧热如下表下列表达正确的是[ ]A.正戊烷的燃烧热大于3 531.3 kJ·mol-1B.稳定性:正丁烷” 主要考查您对燃烧热
烷烃的通性
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 燃烧热
- 烷烃的通性
燃烧热:
在101kPa时,1mol纯物质完全燃烧生成稳定的氧化物时所放出的热量,叫做该物质的燃烧热。单位为kJ/mol
注意事项:
(1)规定是在101kPa 下测出的热量。书中提供的燃烧热数据都是在25℃、101kPa下测定出来的
(2)规定可燃物的物质的量为1mol(这样才有可比性)。因此,表示可燃物的燃烧热的热化学方程式中,可燃物的化学计量数为1,其他物质的化学计量数常出现分数
(3)规定生成稳定的氧化物,例如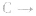
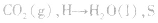
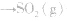 等
等
(4)叙述燃烧热时、不用“+”“-”,在热化学方程式中用△H表示时取“-”
在101kPa时,1mol纯物质完全燃烧生成稳定的氧化物时所放出的热量,叫做该物质的燃烧热。单位为kJ/mol
燃烧热和中和热的异同:
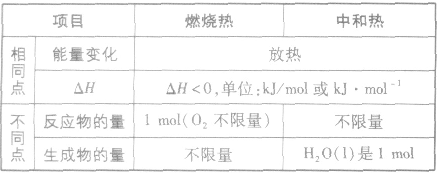
注意事项:
(1)规定是在101kPa 下测出的热量。书中提供的燃烧热数据都是在25℃、101kPa下测定出来的
(2)规定可燃物的物质的量为1mol(这样才有可比性)。因此,表示可燃物的燃烧热的热化学方程式中,可燃物的化学计量数为1,其他物质的化学计量数常出现分数
(3)规定生成稳定的氧化物,例如
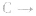
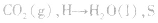
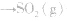 等
等 (4)叙述燃烧热时、不用“+”“-”,在热化学方程式中用△H表示时取“-”
烷烃的通性:
(1)物理性质:随着分子中碳原子数的递增,熔沸点逐渐升高,相对密度逐渐增大,常温下存在状态,由气态逐渐过渡到液态、固态。
(2)烷烃的化学性质:可发生氧化、取代、分解等反应。
烷烃的氧化反应:烷烃燃烧生成二氧化碳和水。CxHy+(x+0.25y)O2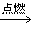 xCO2+0.5yH2O
xCO2+0.5yH2O
烷烃的取代反应:烷烃在光照下可发生取代反应。CnH2n+2+Cl2 CnH2n+1Cl+HCl
CnH2n+1Cl+HCl
烷烃的分解反应:烷烃在高温条件下能够裂解。如:C4H10 CH2=CH2+CH3CH3
CH2=CH2+CH3CH3
(1)物理性质:随着分子中碳原子数的递增,熔沸点逐渐升高,相对密度逐渐增大,常温下存在状态,由气态逐渐过渡到液态、固态。
(2)烷烃的化学性质:可发生氧化、取代、分解等反应。
烷烃的氧化反应:烷烃燃烧生成二氧化碳和水。CxHy+(x+0.25y)O2
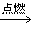 xCO2+0.5yH2O
xCO2+0.5yH2O烷烃的取代反应:烷烃在光照下可发生取代反应。CnH2n+2+Cl2
 CnH2n+1Cl+HCl
CnH2n+1Cl+HCl 烷烃的分解反应:烷烃在高温条件下能够裂解。如:C4H10
 CH2=CH2+CH3CH3
CH2=CH2+CH3CH3 发现相似题
与“一些烷烃的燃烧热如下表下列表达正确的是[ ]A.正戊烷的燃烧...”考查相似的试题有:
- 在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ,下列热化学方程式正确的是A.CH3OH(l)+3/2O2(g)CO2(g)+2H2...
- 己知:与反应的;与反应的。则在水溶液中电离的等于A.B.C.D.
- 两种气态烃的混合气体共1mol,在空气中燃烧得到1.5molCO2和2molH2O。关于该混合气体的说法正确的是( ) A.一定含甲烷,但不...
- 一般硅甲烷的泄漏会自燃引起火灾,若硅甲烷在高压下释放或在高流速下可能发生延迟性的爆炸。下列有关说法中错误的是[ ]A.硅...
- (8分)某有机物A由C、H、O三种元素组成,现取21.6g A在足量氧气中完全燃烧,将燃烧产物全部依次通过无水氯化钙和碱石灰后,...
- (8分)分子中含有10个氢原子的烷烃的分子式是 ;这种烷烃具有 种不同的结构;写出其中没有支链的烃的结构简式 ,写出该物质...
- 下列各组混合物,不论以何种比例混合,只要总物质的量一定,完全燃烧后,产生的CO2的量为一个常数的是A.乙炔和甲苯B.甲烷和...
- 将装有甲烷和氯气混合气体的三个集气瓶,用玻璃片盖好瓶口后,分别作如下处理,各有怎样的现象发生。(1)①置于黑暗中:_______...
- 下列关于有机物的说法不正确的是A.常温常压下,7.0g乙烯与丙烯的混合物中含有氢原子的数目为NAB.分子式分别为C2H6、C5H12的...
- 分子式为C3H2Cl6的同分异构体有(不考虑立体异构)A.2种B.3种C.4种D.5种