本试题 “研究性学习小组进行SO2的制备及性质探究实验。(1)根据反应Na2SO3(固)+H2SO4(浓)=Na2SO4+SO2↑+H2O,制备SO2气体。①用下列简图,画出制各并收集SO2的实验装...” 主要考查您对二氧化硫
二氧化硫的制取
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 二氧化硫
- 二氧化硫的制取
二氧化硫:
①化学式:SO2
②分子结构:SO2是由极性键形成的极性分子,因此易溶于水,其晶体为分子晶体。
二氧化硫的制备:
工业制法:

实验室制法:
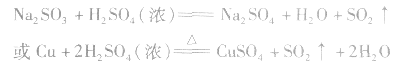
(1)收集:向上排空气法。
(2)检验:品红溶液。SO2是中学阶段学到的唯一种既能使品红褪色,加热后又能使其恢复原色的气体。
(3)尾气处理:用NaOH溶液吸收。
二氧化硫的用途:
工业上用二氧化硫漂白纸浆、毛、丝、草编制品等。此外,二氧化硫还可用于杀菌消毒,可以用作防腐剂。
二氧化硫对环境的污染及治理:

①化学式:SO2
②分子结构:SO2是由极性键形成的极性分子,因此易溶于水,其晶体为分子晶体。
二氧化硫的物理性质和化学性质:
1.物理性质:
SO2是无色、有刺激性气味的有毒气体,密度比空气大,易溶于水(常温常压下,1体积水大约溶解40体积的SO2),易液化(沸点-10℃)。
2.化学性质
(1)具有酸性氧化物的通性
①将SO2通入紫色石蕊试液中,试液变红。
②能与碱性氧化物、碱及某些盐反应。如:
(2)还原性 

(3)弱氧化性 
(4)漂白性(不能漂白酸碱指示剂) 能和某些有色物质化合生成无色物质,生成的无色物质不稳定,易分解而恢复原色,因此,SO2的漂白并不彻底。在中学化学常见试剂中,能用SO2漂白的只有品红溶液,品红溶液 无色溶液
无色溶液 恢复原色。
恢复原色。
SO2与一些物质反应的实验现象:


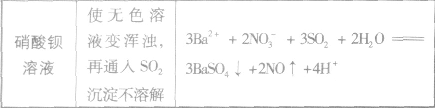
SO2与强碱反应后固体成分的确定:
SO2与强碱(如NaOH)溶液发生反应后的固体成分取决于二者的用量。遇到类似的问题,可以采用数轴分析法讨论。设SO2的物质的量为n(SO2),NaOH物质的量为n(NaOH),数轴代表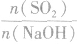 ,如下数轴所示:
,如下数轴所示: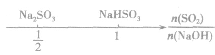
分析数轴可得:
(1)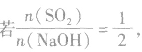 则固体物质为Na2SO3,
则固体物质为Na2SO3,
(2)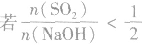 ,则固体物质为NaOH 和Na2SO3.
,则固体物质为NaOH 和Na2SO3.
(3)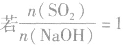 ,则同体物质为NaHSO3
,则同体物质为NaHSO3
(4)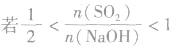 ,则固体物质为Na2SO3和NaHSO3,
,则固体物质为Na2SO3和NaHSO3,
(5)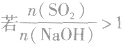 ,则固体物质为NaHSO3。
,则固体物质为NaHSO3。
二氧化硫的制备:
工业制法:

实验室制法:
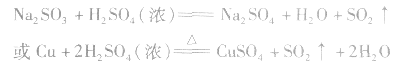
(1)收集:向上排空气法。
(2)检验:品红溶液。SO2是中学阶段学到的唯一种既能使品红褪色,加热后又能使其恢复原色的气体。
(3)尾气处理:用NaOH溶液吸收。
二氧化硫的用途:
工业上用二氧化硫漂白纸浆、毛、丝、草编制品等。此外,二氧化硫还可用于杀菌消毒,可以用作防腐剂。
二氧化硫对环境的污染及治理:

二氧化硫的制取:
1、制取原理:
稳定性强酸与不稳定性弱酸盐的复分解
2、制取方程式
Na2SO3+H2SO4(浓) Na2SO4+SO2↑+H2O
Na2SO4+SO2↑+H2O
3、制取装置
分液漏斗,圆底烧瓶
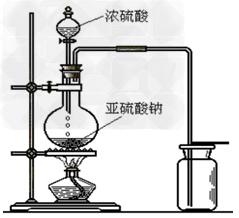
4、检验
先通入品红试液,褪色,后加热又恢复原红色
5、除杂质
通入浓H2SO4(除水蒸气)
6、收集
向上排气法
7、尾气回收
SO2+2NaOH===Na2SO3+H2O
1、制取原理:
稳定性强酸与不稳定性弱酸盐的复分解
2、制取方程式
Na2SO3+H2SO4(浓)
 Na2SO4+SO2↑+H2O
Na2SO4+SO2↑+H2O 3、制取装置
分液漏斗,圆底烧瓶

4、检验
先通入品红试液,褪色,后加热又恢复原红色
5、除杂质
通入浓H2SO4(除水蒸气)
6、收集
向上排气法
7、尾气回收
SO2+2NaOH===Na2SO3+H2O
发现相似题
与“研究性学习小组进行SO2的制备及性质探究实验。(1)根据反应Na2...”考查相似的试题有:
- 下列实验操作正确且能达到预期目的是( )实验目的操 作1比较水和乙醇中羟基氢的活泼性强弱用金属钠分别与水和乙醇反应2欲证...
- “飘尘”是物质燃烧时产生的粒状漂浮物,颗粒很小(直径小于10-7m),不宜沉降(可漂浮数小时甚至数年),它与空气中的S02接触...
- 某化学兴趣小组为探究SO2的性质,按如图所示装置进行实验.请回答下列问题:(1)装置A中盛放浓硫酸和亚硫酸钠的仪器名称分别...
- 下列实验过程中产生的现象与对应的图形正确的是( )A.盐酸中加入Na[Al(OH)4]溶液B. SO2通入溴水中C.向Na2CO3溶液中逐滴...
- 有A、B、C、D、E五种短周期元素,原子半径依次减小。E元素与其它元素不在同一周期。C、D在周期表中处于相邻位置,它们的单质...
- 下列现象或事实可用同一原理解释的是( )A.氯水和SO2使品红溶液褪色B.乙炔和乙烯使溴的四氯化碳溶液褪色C.浓硝酸和浓盐酸...
- (7分)某化工厂生产硫酸,某硫矿中硫单质的质量分数为88%。若取该矿石1.00 t,最多可制得98%的浓硫酸多少t?(假设生产过程中...
- 将过量的金属锌投入到含0.200 mol H2SO4的热、浓硫酸中,下列判断正确的是( )A.因发生“钝化”而不反应B.产生的SO2为0.100 ...
- (16分)某研究小组想研究碳与浓硝酸的反应。其实验过程如下。操作现象a.用干燥洁净的烧杯取约10 mL浓硝酸,加热。 b.把小...
- (17分)在化学课上,围绕浓硫酸的化学性质进行了如下实验探究:将适量的蔗糖放入烧杯中,加入几滴水,搅拌均匀。然后加入适...