本试题 “铁、铝、铜等金属及其化合物在日常生活中应用广泛,请根据下列实验回答问题:(1)生铁中含有一种铁碳化合物X(Fe3C)。X在足量的空气中高温煅烧,生成有磁性的固...” 主要考查您对离子反应
单质铁
氧化铁
其他物质的制备(硫酸铜晶体、铁红等)
氧化还原反应的滴定
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 离子反应
- 单质铁
- 氧化铁
- 其他物质的制备(硫酸铜晶体、铁红等)
- 氧化还原反应的滴定
定义:
凡是有离子参加或离子生成的反应都是离子反应。
离子反应包括:复分解反应、氧化还原反应、络合反应、双水解反应
常见阳离子的检验方法:
常见阴离子的检验方法:
注意: 1.若SO42-与Cl-同时检验,需注意检验顺序。应先用Ba(NO3)2溶液将SO42-检出,并滤去BaSO4,然后再用AgNO3检验Cl-。
2.检验SO32-的试剂中,只能用盐酸,不能用稀硝酸。因为稀硝酸能把SO32-氧化成SO42-。
3.若Ag+和Ba2+同时检验,也需注意检验顺序,应先用盐酸将Ag+检验出并滤去沉淀,然后再用稀硫酸检验Ba2+。
凡是有离子参加或离子生成的反应都是离子反应。
离子反应包括:复分解反应、氧化还原反应、络合反应、双水解反应
常见阳离子的检验方法:
| 离子 | 检验试剂 | 实验步骤 | 实验现象 | 离子方程式 |
| K+ | 焰色反应 | ①铂丝在火焰上灼烧至原火焰色②蘸取溶液,放在火焰上灼烧,观察火焰颜色。 | 浅紫色(通过蓝色钴玻璃片观察钾离子焰色) | —— |
| Na+ | 焰色反应 | 火焰分别呈黄色 | ||
| NH4+ | NaOH溶液(浓) | 向未知溶液中加入NaOH浓溶液并加热 | 生成有刺激性气味、使湿润红色石蕊试纸变蓝的气体 | NH4++OH-=NH3↑+H2O |
| Al3+ | 加NaOH溶液 | 向未知溶液中加入NaOH溶液 | 加入适量NaOH溶液后生成白色沉淀,该沉淀溶于过量NaOH溶液中 |
Al3++3OH-=Al(OH)3↓ |
| Cu2+ | 浓氨水 | 向未知溶液中加入浓氨水 | 加入适量浓氨水后生成蓝色沉淀,该沉淀溶于过量浓氨水中,溶液呈深蓝色 |
Cu2++2OH-=Cu(OH)2↓ Cu(OH)2+4NH3·H2O=[Cu(NH3)4]2++2OH-+4H2O |
| Ag+ | ①稀盐酸或可溶性盐酸盐②稀HNO3③氨水 | 向未知溶液中加入稀盐酸再加入稀HNO3向过滤出的沉淀中加氨水 | 生成白色沉淀,不溶于稀HNO3,但溶于氨水,生成[Ag(NH3)2]+ | Ag++Cl-=AgCl↓ |
| Ba2+ | 稀H2SO4或可溶性酸盐溶液 | 向未知溶液中加入稀H2SO4再加入稀HNO3 | 产生白色沉淀,且沉淀不溶于稀HNO3 | Ba2++SO42-=BaSO4↓ |
| Fe3+ | KSCN溶液 | 向未知溶液中加入KSCN溶液或加NaOH溶液或加苯酚 | 变为血红色溶液 | Fe3++3SCN-=Fe(SCN)3 |
| 加NaOH溶液 | 产生红褐色沉淀 | Fe3++3OH-=Fe(OH)3↓ | ||
| 加苯酚 | 溶液显紫色 | Fe3++6C6H6OH→[Fe(C6H5O)]3-+6H+ | ||
| Fe2+ | ①加NaOH溶液 | 向未知溶液中加入NaOH溶液并露置在空气中 | 开始时生成白色Fe(OH)2沉淀,迅速变成灰绿色,最后变成红褐色Fe(OH)3沉淀。 | Fe2++2OH-=Fe(OH)2↓ 4Fe(OH)2+O2+2H2O=4Fe(OH)3 |
| ②KMnO4 (H+)溶液 | 向未知溶液中加入KMnO4(H+)溶液 | KMnO4(H+)紫色褪去 | MnO4-+5Fe2++8H+=5Fe3++Mn2++4H2O | |
| ③K3[Fe(CN)6] | 向未知溶液中加入K3[Fe(CN)6]溶液 | 出现蓝色Fe3[Fe(CN)6]2沉淀 | 3Fe2++2[Fe(CN)6]-=Fe3[Fe(CN)6]2↓ | |
| ④KSCN溶液,新制的氯水 | 加入KSCN溶液,新制的氯水 | 加入KSCN溶液不显红色,加入少量新制的氯水后,立即显红色。 | 2Fe2++Cl2=2Fe3++2Cl-Fe3++3SCN-=Fe(SCN)3 |
常见阴离子的检验方法:
| 离子 | 检验试剂 | 实验步骤 | 实验现象 | 离子方程式 |
| CO32- | ①BaCl2溶液、稀盐酸 | 向未知溶液中加入BaCl2溶液再向沉淀中加入稀盐酸 | 加入BaCl2溶液后生成白色沉淀,沉淀溶于稀盐酸,并放出无色无味气体 | Ba2++CO32-=BaCO3↓ BaCO3+2H+=Ba2++CO2↑+H2O |
| ②稀盐酸、Ca(OH)2溶液 | 加入稀盐酸后放出的气体通入使澄清的Ca(OH)2溶液 | 加入稀盐酸后放出无色无味气体,通入澄清的Ca(OH)2溶液变浑浊 | CO32-+2H+=H2O+CO2↑ Ca2++2OH-+CO2=CaCO3↓+H2O | |
| SO42- | BaCl2溶液、稀硝酸或稀盐酸 | 向未知溶液中加入BaCl2溶液再向沉淀中加入稀盐酸 | 生成不溶于稀硝酸或稀盐酸的白色沉淀 | Ba2++SO42-=BaSO4↓ |
| SO32- | ①BaCl2溶液、稀盐酸 | 向未知溶液中加入BaCl2溶液再向沉淀中加入稀盐酸 | 加入BaCl2溶液后生成白色沉淀,沉淀溶于稀盐酸,并放出刺激性气味的气体 | SO32-+2H+=H2O+SO2↑ |
| ②稀盐酸、品红溶液 | 加入稀盐酸后放出的气体通入品红溶液 | 加入稀盐酸后放出的气体使品红溶液褪色 | SO32-+2H+=H2O+SO2↑ | |
| Cl- | AgNO3溶液、稀硝酸或稀盐酸 | 向未知溶液中加入AgNO3溶液,再向沉淀中加入稀盐酸 | 生成不溶于稀硝酸或稀盐酸的白色沉淀 | Ag++Cl-=AgCl↓ |
| Br- | AgNO3溶液、稀硝酸或稀盐酸 | 生成不溶于稀硝酸或稀盐酸的浅黄色沉淀 | Ag++Br-=AgBr↓ | |
| I- | AgNO3溶液、稀硝酸或稀盐酸 | 向未知溶液中加入AgNO3溶液,再向沉淀中加入稀盐酸 | 生成不溶于稀硝酸的黄色沉淀 | Ag++I-=AgI↓ |
| ②新制氯水,淀粉溶液 | 向未知溶液中加入新制氯水,再加入淀粉溶液 | 滴入新制Cl2,振荡后再滴入淀粉溶液,变蓝 | Ag++I-=AgI↓ 2I-+Cl2=I2+2Cl- I2遇淀粉变蓝 |
2.检验SO32-的试剂中,只能用盐酸,不能用稀硝酸。因为稀硝酸能把SO32-氧化成SO42-。
3.若Ag+和Ba2+同时检验,也需注意检验顺序,应先用盐酸将Ag+检验出并滤去沉淀,然后再用稀硫酸检验Ba2+。
铁元素:
在元素周期表中的位置:铁的原子序数26,位于周期表中第四周期,第Ⅷ族。
(1)物理性质:银白色、有金属光泽,密度较大,熔点较高,硬度较小,具有导电、导热、延展性,可被磁铁吸引。
(2)化学性质:较活泼的金属,+2、+3价两种价态
①与强氧化剂反应(如:Cl2 Br2 过量稀HNO3)生成+3价铁的化合物。如: 
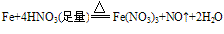
注:铁常温下在浓硫酸和浓硝酸中钝化,但加热可以反应,且被氧化成Fe3+
②与弱氧化剂反应(如S I2 H+ Cu2+)生成+2价铁的化合物,如: 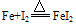
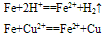
③铁与氧气、水蒸气反应生成Fe3O4(FeO·Fe2O3)

铁的性质:
- 物理性质:铁是黑色金属,具有铁磁性
- 铁的化学性质:
①与强氧化剂反应(如:Cl2、 Br2 、过量稀HNO3)生成+3价铁的化合物。如:
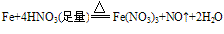
注:铁常温下在浓硫酸和浓硝酸中钝化,但加热可以反应,且被氧化成Fe3+
②与弱氧化剂反应(如S、 I2 、H+ 、Cu2+)生成+2价铁的化合物,如: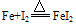
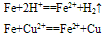
③铁与氧气、水蒸气反应生成Fe3O4(FeO·Fe2O3)

铁与稀硝酸的反应:
- 铁少量时:
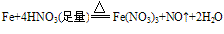
- 铁过量时:3Fe+8HNO3==3Fe(NO3)2+2NO+4H2O
两式可通过2Fe3++Fe==3Fe2+联系起来。
注意:
- 铁元素性质活泼,自然界中的铁元素几乎都是以化合态存在,只有在陨石中存在游离态的铁元素。
- 过量的铁与氯气反应,不会生成FeCl2,因为铁还原三价铁必须在水溶液中进行。
- 金属与强氧化性酸反应,不会生成H2。
化学性质:
铁元素性质活泼,有较强的还原性。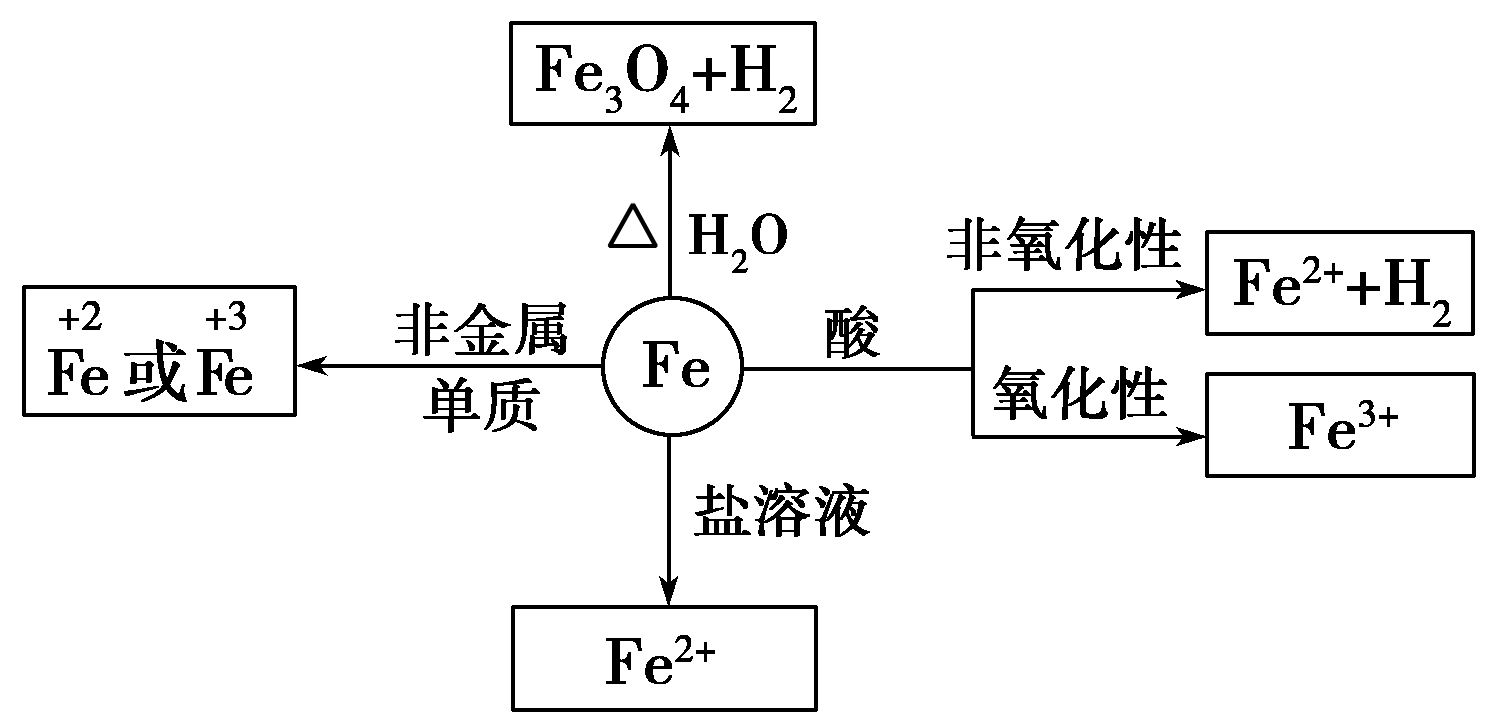
铁三角关系:

氧化铁:
化学式Fe2O3,溶于盐酸,为红棕色粉末。其红棕色粉末为一种低级颜料,工业上称氧化铁红,用于油漆、油墨、橡胶等工业中,可做催化剂,玻璃、宝石、金属的抛光剂,可用作炼铁原料。
(1)色态:红色粉末,俗称铁锈(铁红)
(2)溶解性:溶于盐酸、稀硫酸生成+3价铁盐;难溶于水,不与水反应。
(3)氧化性:高温下被CO、H2、Al、C、Si等还原
氧化铁的化学性质:
- 铝热反应:2Al+Fe2O3=(高温)=Al2O3+2Fe
- 与强酸反应:Fe2O3+6H+==2Fe3++3H2O
- 与还原性酸(HI)反应:Fe2O3+6H++2I-==2Fe2++3H2O+I2
铁的氧化物:
| 化学式 | FeO | Fe2O3 | Fe3O4 |
| 俗称 | —— | 铁红 | 磁性氧化铁 |
| 色态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
| 铁的价态 | +2 | +3 | +2、+3 |
| 水溶性 | 不溶 | 不溶 | 不溶 |
| 与酸反应 | FeO+2H+==Fe2++H2O | Fe2O3+6H+==2Fe3++3H2O | Fe3O4+8H+==Fe2++2Fe3++4H2O |
| 用途 | 玻璃色料 | 油漆、颜料 | 做颜料和抛光剂 |
| 氧化性 | 高温时都能与C、CO、H2反应,被还原生成Fe单质 | ||
实验室制取甲烷(CH4):
(1)反应原理:CH3COONa+NaOH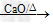 CH4+Na2CO3
CH4+Na2CO3
(2)发生装置:固+固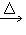 气
气
(3)净化方法:浓硫酸(除水蒸气)
(4)收集方法:排水集气法/向下排空气法
(5)尾气处理:无
(6)检验方法:①点燃,淡蓝色火焰,燃烧产物是H2O和CO2
实验室制取一氧化氮(NO):
(1)反应原理:3Cu+8HNO3(稀)==3Cu(NO3)2+2NO↑+4H2O
(2)发生装置:固+液→气
(3)净化方法:浓硫酸(除水蒸气)
(4)收集方法:排水集气法
(5)尾气处理:收集法(塑料袋)
(6)检验方法:无色气体,暴露于空气中立即变为红棕色
实验室制取二氧化氮(NO2):
(1)反应原理:Cu+4HNO3(浓)==Cu(NO3)2+2NO2↑+2H2O
(2)发生装置:固+液→气
(3)净化方法:浓硫酸(除水蒸气)
(4)收集方法:向上排空气法
(5)尾气处理:碱液吸收 (3NO2+H2O==2HNO3+NO;NO+NO2+2NaOH===2NaNO2+H2O)
实验室制取氯化氢(HCl):
(1)反应原理:2NaCl+H2SO4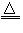 Na2SO4+2HCl?
Na2SO4+2HCl?
(2)发生装置:固+液→气
(3)净化方法:浓硫酸(除水蒸气)
(4)收集方法:向上排空气法
(5)尾气处理:水(防倒吸装置)
(6)检验方法:①能使湿润的蓝色石蕊试纸变红 ②靠近浓氨水冒白烟
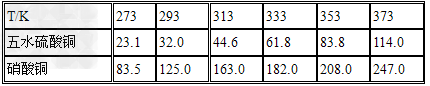
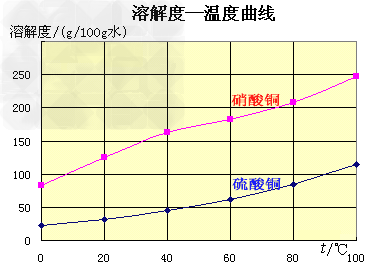
五水硫酸铜的制备:
(1)实验原理:铜是不活泼金属,不能直接和稀硫酸发生反应制备硫酸铜,必须加入氧化剂。在浓硝酸和稀硫酸的混合液中,浓硝酸将铜氧化成Cu2+,Cu2+与SO42-结合得到硫酸铜: Cu+2HNO3+H2SO4====CuSO4+2NO2+2H2O 未反应的铜屑(不溶性杂质)用倾滗法除去。利用硝酸铜的溶解度在0~100℃范围内均大于硫酸铜溶解度的性质,溶液经蒸发浓缩析出硫酸铜,经过滤与可溶性杂质硝酸铜分离,得到粗产品。硫酸铜的溶解度随温度升高而增大,可用重结晶法提纯。在粗产品硫酸铜中,加适量水,加热成饱和溶液,趁热过滤除去不溶性杂质。滤液冷却,析出硫酸铜,过滤,与可溶性杂质分离,得到纯的硫酸铜。
(2)实验步骤
①称量1.5g铜屑,灼烧至表面呈现黑色,冷却;
②加5.5mL3mol/L硫酸,2.5mL浓硝酸,反应平稳后水浴加热,补加2.5mL3mol/L硫酸,0.5mL浓硝酸;
③铜近于完全溶解后,趁热倾滗法分离;
④水浴加热,蒸发浓缩至结晶膜出现;
⑤冷却、过滤;
⑥粗产品以1.2mL水/g的比例,加热溶于水,趁热过滤;
⑦滤液冷却、过滤、晾干,得到纯净的硫酸铜晶体。
⑧称重,计算产率。
实验室制取硫化氢(H2S):
(1)反应原理:FeS+2HCl→H2S↑+FeCl2
(2)发生装置:固+液→气(启普发生器)
(3)净化方法:饱和NaHS(除HCl),固体CaCl2(除水蒸气)
(4)收集方法:向上排空气法
(5)尾气处理:CuSO4溶液或碱液吸收(H2S+2NaOH==Na2S+H2O或H2S+NaOH==NaHS+H2O)
(6)检验方法:①湿润的蓝色石蕊试纸变红 ②湿润的醋酸试纸黑
(1)反应原理:CH3COONa+NaOH
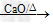 CH4+Na2CO3
CH4+Na2CO3(2)发生装置:固+固
 气
气 (3)净化方法:浓硫酸(除水蒸气)
(4)收集方法:排水集气法/向下排空气法
(5)尾气处理:无
(6)检验方法:①点燃,淡蓝色火焰,燃烧产物是H2O和CO2
实验室制取一氧化氮(NO):
(1)反应原理:3Cu+8HNO3(稀)==3Cu(NO3)2+2NO↑+4H2O
(2)发生装置:固+液→气
(3)净化方法:浓硫酸(除水蒸气)
(4)收集方法:排水集气法
(5)尾气处理:收集法(塑料袋)
(6)检验方法:无色气体,暴露于空气中立即变为红棕色
实验室制取二氧化氮(NO2):
(1)反应原理:Cu+4HNO3(浓)==Cu(NO3)2+2NO2↑+2H2O
(2)发生装置:固+液→气
(3)净化方法:浓硫酸(除水蒸气)
(4)收集方法:向上排空气法
(5)尾气处理:碱液吸收 (3NO2+H2O==2HNO3+NO;NO+NO2+2NaOH===2NaNO2+H2O)
实验室制取氯化氢(HCl):
(1)反应原理:2NaCl+H2SO4
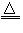 Na2SO4+2HCl?
Na2SO4+2HCl?(2)发生装置:固+液→气
(3)净化方法:浓硫酸(除水蒸气)
(4)收集方法:向上排空气法
(5)尾气处理:水(防倒吸装置)
(6)检验方法:①能使湿润的蓝色石蕊试纸变红 ②靠近浓氨水冒白烟
五水硫酸铜的制备:
(1)实验原理:铜是不活泼金属,不能直接和稀硫酸发生反应制备硫酸铜,必须加入氧化剂。在浓硝酸和稀硫酸的混合液中,浓硝酸将铜氧化成Cu2+,Cu2+与SO42-结合得到硫酸铜: Cu+2HNO3+H2SO4====CuSO4+2NO2+2H2O 未反应的铜屑(不溶性杂质)用倾滗法除去。利用硝酸铜的溶解度在0~100℃范围内均大于硫酸铜溶解度的性质,溶液经蒸发浓缩析出硫酸铜,经过滤与可溶性杂质硝酸铜分离,得到粗产品。硫酸铜的溶解度随温度升高而增大,可用重结晶法提纯。在粗产品硫酸铜中,加适量水,加热成饱和溶液,趁热过滤除去不溶性杂质。滤液冷却,析出硫酸铜,过滤,与可溶性杂质分离,得到纯的硫酸铜。


(2)实验步骤
①称量1.5g铜屑,灼烧至表面呈现黑色,冷却;
②加5.5mL3mol/L硫酸,2.5mL浓硝酸,反应平稳后水浴加热,补加2.5mL3mol/L硫酸,0.5mL浓硝酸;
③铜近于完全溶解后,趁热倾滗法分离;
④水浴加热,蒸发浓缩至结晶膜出现;
⑤冷却、过滤;
⑥粗产品以1.2mL水/g的比例,加热溶于水,趁热过滤;
⑦滤液冷却、过滤、晾干,得到纯净的硫酸铜晶体。
⑧称重,计算产率。
实验室制取硫化氢(H2S):
(1)反应原理:FeS+2HCl→H2S↑+FeCl2
(2)发生装置:固+液→气(启普发生器)
(3)净化方法:饱和NaHS(除HCl),固体CaCl2(除水蒸气)
(4)收集方法:向上排空气法
(5)尾气处理:CuSO4溶液或碱液吸收(H2S+2NaOH==Na2S+H2O或H2S+NaOH==NaHS+H2O)
(6)检验方法:①湿润的蓝色石蕊试纸变红 ②湿润的醋酸试纸黑
氧化还原滴定法:
1.特点:氧化还原滴定法在药物分析中应用广泛,用于测定具有氧化性和还原性的物质,对不具有氧化性或还原性的物质,可进行间接测定。氧化还原反应较复杂,常伴有各种副反应,反应速度较慢,因此,氧化还原滴定法要注意选择合适条件使反应能定量、迅速、完全进行。
2.反应条件:
(1)滴定反应必须按一定的化学反应式定量反应,且反应完全,无副反应。
(2)反应速度必须足够快。
(3)必须有适当的方法确定化学计量点。
3.若氧化还原反应的速度极慢,该反应就不能直接用于滴定。通常采用提高氧化还原反应速度的方法主要有以下几点。
(1)增大反应物的浓度
(2)升高温度
(3)通过催化作用
4.氧化还原滴定法终点的判断
(1)自身指示剂如KMnO4滴定H2C2O4时,KMnO4既是标准溶液又是指示剂。
(2)特殊指示剂如用于碘量法中的淀粉溶液,本身不参与氧化还原反应,但它能与氧化剂作用产生特殊的颜色,因而可指示终点。
(3)氧化还原指示剂
5.高锰酸钾法
(1)基本原理和条件高锰酸钾法是以具有强氧化能力的高锰酸钾做标准溶液,利用其氧化还原滴定原理来测定其他物质的滴定分析方法。强酸性溶液中 MnO4-+8H++5e-→Mn2++4H2O
注意:但酸度太高时,会导致高锰酸钾分解,因此酸度控制常用3mol/L的H2SO4来调节,而不用HNO3或HCl来控制酸度。因为硝酸具有氧化性会与被测物反应;而盐酸具有还原性能与KMnO4反应。
(2)测定方法:
①直接滴定法由于高锰酸钾氧化能力强,滴定时无需另加指示剂,可直接滴定具有还原性的物质。
②返滴定法可测定一些不能直接滴定的氧化性和还原性物质。
③间接滴定法有些非氧化性或还原性物质不能用直接滴定法或返滴定法测定时,可采用此法。
(3)标准溶液的配制与标定
①高锰酸钾溶液的配制市售KMnO4试剂常含有杂质,而且在光、热等条件下不稳定,会分解变质。因此高锰酸钾标准溶液不能直接配制使用,通常先配成浓溶液放置储存,需要时再取适量稀释成近似浓度的溶液,然后标定使用。
②高锰酸钾溶液的标定常用于标定KMnO4的基准物是Na2C2O4。Na2C2O4在105℃~110℃烘干2h,放入干燥器中冷却后,即可使用。已标定过的KMnO4溶液在使用一段时间后必须重新标定。标定反应为:2MnO4-+5C2O42-+16H+==2Mn2++10CO2↑+8H2O
(4)标定时注意事项:
①滴定速度:开始时因反应速度慢,滴定速度要慢;开始后反应本身所产生的Mn2+起催化作用,加快反应进行,滴定速度可加快。
②温度:近终点时加热至65℃,促使反应完全
③酸度:保持一定的酸度(3mol/LH2SO4)。
④滴定终点:滴入微过量高锰酸钾,利用自身的粉红色指示终点(30秒不褪色)。
6.碘量法
(1)基本原理碘量法是利用碘的氧化性、碘离子的还原性进行物质含量测定的方法。I2是较弱的氧化剂;I-是中等强度的还原剂。碘量法可用直接测定和间接测定两种方式进行。
(2)①直接碘量法(或碘滴定法)直接碘量法是直接用I2标准溶液滴定还原性物质,又叫做碘滴定法。直接碘量法只能在酸性、中性或弱碱性溶液中进行。直接碘量法可用淀粉指示剂指示终点。直接碘量法还可利用碘自身的颜色指示终点,化学计量点后,溶液中稍过量的碘显黄色而指示终点。
②间接碘量法(或滴定碘法)对氧化性物质,可在一定条件下,用I-还原,产生I2,然后用Na2S2O3标准溶液滴定释放出的I2。这种方法就叫做间接碘量法或滴定碘法。间接碘量法也是使用淀粉溶液作指示剂,溶液由蓝色变无色为终点。
③间接碘量法的反应条件和滴定条件
A. 酸度的影响:I2与Na2S2O3应在中性、弱酸性溶液中进行反应。
B. 防止I2挥发的方法:在滴定前,加入过量KI(比理论值大2~3倍),减少I2挥发。
C. 防止I-被氧化
(3)标准溶液的配制和标定
①碘标准溶液(0.05mol/L)的配制和标定
A. 配制由于碘具有挥发性和腐蚀性,通常情况下,碘标准溶液是采用间接法配制。配制0.05mol/L时,可取碘13g,加碘化钾36g与水50ml溶解后,加稀盐酸3滴与水适量稀释至1000ml,摇匀,贮存于棕色试剂瓶中备用。
B. 标定:用三氧化二砷(As2O3)为基准物质,甲基橙为指示剂,用待标定的碘标准溶液滴定至终点。
②硫代硫酸钠标准溶液(0.1mol/L)的配制和标定
A. 配制:Na2S2O3溶液采取间接法配制。操作步骤:称取硫代硫酸钠26g与无水碳酸钠0.2g,加新煮沸过的冷水适量稀释至1000ml,摇匀,放置8~10天,滤过,备用。
在Na2S2O3溶液的配制过程中应采取下列措施:
第一、为了除去水中的微生物,用新煮沸冷却后的蒸馏水配制。
第二、配制时加入少量的Na2CO3,使溶液呈弱碱性,可减少溶解在水中的CO2、O2和杀死微生物。
第三、将配制溶液置于棕色瓶中,放置8~10天,待其浓度稳定后再标定,但若发现溶液浑浊,需重新配制。
B. 标定:以K2Cr2O7为基准物,加入碘化钾置换出定量的碘,再用硫代硫酸钠标准溶液滴定碘
标定方法为:精密称取在120℃干燥至恒重的基准物质重铬酸钾0.15g,置碘量瓶中,加水50ml溶解,加碘化钾2.0g,轻轻振摇,加稀硫酸40ml,摇匀,密塞,水封后在暗处放置10分钟,取出加水50ml稀释,用待标定Na2S2O3溶液滴定至近终点时,加淀粉指示剂3ml,继续滴定至溶液由蓝色变亮绿色为终点。
滴定反应为:

1.特点:氧化还原滴定法在药物分析中应用广泛,用于测定具有氧化性和还原性的物质,对不具有氧化性或还原性的物质,可进行间接测定。氧化还原反应较复杂,常伴有各种副反应,反应速度较慢,因此,氧化还原滴定法要注意选择合适条件使反应能定量、迅速、完全进行。
2.反应条件:
(1)滴定反应必须按一定的化学反应式定量反应,且反应完全,无副反应。
(2)反应速度必须足够快。
(3)必须有适当的方法确定化学计量点。
3.若氧化还原反应的速度极慢,该反应就不能直接用于滴定。通常采用提高氧化还原反应速度的方法主要有以下几点。
(1)增大反应物的浓度
(2)升高温度
(3)通过催化作用
4.氧化还原滴定法终点的判断
(1)自身指示剂如KMnO4滴定H2C2O4时,KMnO4既是标准溶液又是指示剂。
(2)特殊指示剂如用于碘量法中的淀粉溶液,本身不参与氧化还原反应,但它能与氧化剂作用产生特殊的颜色,因而可指示终点。
(3)氧化还原指示剂
5.高锰酸钾法
(1)基本原理和条件高锰酸钾法是以具有强氧化能力的高锰酸钾做标准溶液,利用其氧化还原滴定原理来测定其他物质的滴定分析方法。强酸性溶液中 MnO4-+8H++5e-→Mn2++4H2O
注意:但酸度太高时,会导致高锰酸钾分解,因此酸度控制常用3mol/L的H2SO4来调节,而不用HNO3或HCl来控制酸度。因为硝酸具有氧化性会与被测物反应;而盐酸具有还原性能与KMnO4反应。
(2)测定方法:
①直接滴定法由于高锰酸钾氧化能力强,滴定时无需另加指示剂,可直接滴定具有还原性的物质。
②返滴定法可测定一些不能直接滴定的氧化性和还原性物质。
③间接滴定法有些非氧化性或还原性物质不能用直接滴定法或返滴定法测定时,可采用此法。
(3)标准溶液的配制与标定
①高锰酸钾溶液的配制市售KMnO4试剂常含有杂质,而且在光、热等条件下不稳定,会分解变质。因此高锰酸钾标准溶液不能直接配制使用,通常先配成浓溶液放置储存,需要时再取适量稀释成近似浓度的溶液,然后标定使用。
②高锰酸钾溶液的标定常用于标定KMnO4的基准物是Na2C2O4。Na2C2O4在105℃~110℃烘干2h,放入干燥器中冷却后,即可使用。已标定过的KMnO4溶液在使用一段时间后必须重新标定。标定反应为:2MnO4-+5C2O42-+16H+==2Mn2++10CO2↑+8H2O
(4)标定时注意事项:
①滴定速度:开始时因反应速度慢,滴定速度要慢;开始后反应本身所产生的Mn2+起催化作用,加快反应进行,滴定速度可加快。
②温度:近终点时加热至65℃,促使反应完全
③酸度:保持一定的酸度(3mol/LH2SO4)。
④滴定终点:滴入微过量高锰酸钾,利用自身的粉红色指示终点(30秒不褪色)。
6.碘量法
(1)基本原理碘量法是利用碘的氧化性、碘离子的还原性进行物质含量测定的方法。I2是较弱的氧化剂;I-是中等强度的还原剂。碘量法可用直接测定和间接测定两种方式进行。
(2)①直接碘量法(或碘滴定法)直接碘量法是直接用I2标准溶液滴定还原性物质,又叫做碘滴定法。直接碘量法只能在酸性、中性或弱碱性溶液中进行。直接碘量法可用淀粉指示剂指示终点。直接碘量法还可利用碘自身的颜色指示终点,化学计量点后,溶液中稍过量的碘显黄色而指示终点。
②间接碘量法(或滴定碘法)对氧化性物质,可在一定条件下,用I-还原,产生I2,然后用Na2S2O3标准溶液滴定释放出的I2。这种方法就叫做间接碘量法或滴定碘法。间接碘量法也是使用淀粉溶液作指示剂,溶液由蓝色变无色为终点。
③间接碘量法的反应条件和滴定条件
A. 酸度的影响:I2与Na2S2O3应在中性、弱酸性溶液中进行反应。
B. 防止I2挥发的方法:在滴定前,加入过量KI(比理论值大2~3倍),减少I2挥发。
C. 防止I-被氧化
(3)标准溶液的配制和标定
①碘标准溶液(0.05mol/L)的配制和标定
A. 配制由于碘具有挥发性和腐蚀性,通常情况下,碘标准溶液是采用间接法配制。配制0.05mol/L时,可取碘13g,加碘化钾36g与水50ml溶解后,加稀盐酸3滴与水适量稀释至1000ml,摇匀,贮存于棕色试剂瓶中备用。
B. 标定:用三氧化二砷(As2O3)为基准物质,甲基橙为指示剂,用待标定的碘标准溶液滴定至终点。
②硫代硫酸钠标准溶液(0.1mol/L)的配制和标定
A. 配制:Na2S2O3溶液采取间接法配制。操作步骤:称取硫代硫酸钠26g与无水碳酸钠0.2g,加新煮沸过的冷水适量稀释至1000ml,摇匀,放置8~10天,滤过,备用。
在Na2S2O3溶液的配制过程中应采取下列措施:
第一、为了除去水中的微生物,用新煮沸冷却后的蒸馏水配制。
第二、配制时加入少量的Na2CO3,使溶液呈弱碱性,可减少溶解在水中的CO2、O2和杀死微生物。
第三、将配制溶液置于棕色瓶中,放置8~10天,待其浓度稳定后再标定,但若发现溶液浑浊,需重新配制。
B. 标定:以K2Cr2O7为基准物,加入碘化钾置换出定量的碘,再用硫代硫酸钠标准溶液滴定碘
标定方法为:精密称取在120℃干燥至恒重的基准物质重铬酸钾0.15g,置碘量瓶中,加水50ml溶解,加碘化钾2.0g,轻轻振摇,加稀硫酸40ml,摇匀,密塞,水封后在暗处放置10分钟,取出加水50ml稀释,用待标定Na2S2O3溶液滴定至近终点时,加淀粉指示剂3ml,继续滴定至溶液由蓝色变亮绿色为终点。
滴定反应为:

发现相似题
与“铁、铝、铜等金属及其化合物在日常生活中应用广泛,请根据下...”考查相似的试题有:
- 向一种溶液中滴加另一种溶液后,溶液的颜色不发生变化的是[ ]A.碳酸氢钠溶液中滴加稀盐酸B.硫酸铁溶液中滴加硫氰化钾溶液C...
- 常见的五种盐A、B、C、D、E,它们的阳离子可能是Na+、、Cu2+、Ba2+、Al3+、Ag+、Fe3+,阴离子可能是Cl-、。已知:①五种盐均溶...
- 将等物质的量的镁和铝相混合,取四份等质量的该混合物分别加入到足量的下列溶液中,充分反应后,放出氢气最多的是( )A.3 m...
- 物质的性质决定了物质的用途,下面列出了金属的几种性质:①导热性、②导电性、③还原性、④延展性、⑤具有金属光泽。请在下面金属...
- 为了防止枪支生锈,常将枪支的钢铁零件放在NaNO2和NaOH的混合液中进行化学处理经处理后钢铁零件表面生成Fe3O4的致密的保护层—...
- 能与Fe3+反应,且能证明Fe3+具有氧化性的是①SCN- ②Fe ③Fe2+ ④Cu ⑤Zn ⑥OH-A.①②③B.②④⑤C.①③⑥D.①②⑤
- 利用废的生铁丝(表面有铁锈)、硫酸铜废液(含硫酸亚铁)和被有机物污染的废铜粉制备硫酸铜晶体。生产过程如下图:试回答下列...
- (4分)已知Cu+在酸性溶液中可发生自身氧化还原反应生成Cu和Cu2+。CuH是一种难溶物,它会在氯气中燃烧,也能与盐酸反应放出气...
- 工业上用某矿渣(含有Cu2O、Al2O3、Fe2O3、SiO2)提取铜的操作流程如下:已知:Cu2O+2H+═Cu+Cu2++H2O(1)实验操作I的名称为 ...
- (12分)NaClO2用于棉、麻、粘胶纤维及织物的漂白。实验室制备NaClO2的装置如下图所示:(1)装置I控制温度在35~55℃,通入SO2将...