本试题 “某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:(1)硫酸铜溶液可以加快氢气生成速率的原因是______...” 主要考查您对影响化学反应速率的因素
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 影响化学反应速率的因素
影响化学反应速率的因素:
1.内因:参加反应的物质的结构及性质。
2.外因:主要是指浓度、温度、压强和催化剂,另外还有光、超声波、激光、搅拌、固体表面积、形成原电池等。
(1)浓度:其他条件相同时,增大反应物浓度,化学反应速率增大;减小反应物浓度,化学反应速率减小。在一定温度下,同体、纯液体的浓度视为定值,如C与CO2的反应、Na与H2O的反应中,C的量和Na、H2O 的量减少并不意味着其“浓度”减小,即不冈其量的增减而影响反应速率,但会因固体表面积的变化而改变反应速率。
(2)温度:其他条件相同时,升高温度,可以加快反应速率,实验测得,温度每升高10℃,化学反应速率通常增大到原来的2~4倍。
经验公式为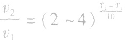
(3)压强:对于气体反应,当温度不变时,增大压强可以加快反应速率。对于气体反应体系,压强改变时有以下几种情况:

(4)催化剂:催化剂是能改变化学反应速率但在反应前后本身的质量和化学性质都不变的物质。对于某些化学反应,使用正催化剂能显著加快化学反应速率。
(5)其他因素:增大同体的表面积(如将块状改为粉末状),可增大反应速率;光照一般也可增大某些反应的速率;形成原电池可以加快反应速率;此外,超声波、放射线、电磁波等因素也能影响反应速率。
3.外因对化学反应速率影响的微观解释
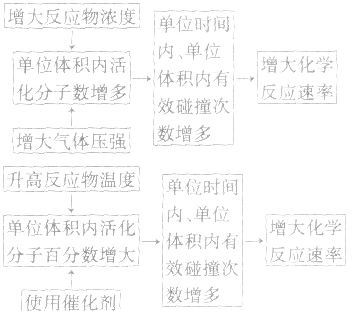
1.内因:参加反应的物质的结构及性质。
2.外因:主要是指浓度、温度、压强和催化剂,另外还有光、超声波、激光、搅拌、固体表面积、形成原电池等。
(1)浓度:其他条件相同时,增大反应物浓度,化学反应速率增大;减小反应物浓度,化学反应速率减小。在一定温度下,同体、纯液体的浓度视为定值,如C与CO2的反应、Na与H2O的反应中,C的量和Na、H2O 的量减少并不意味着其“浓度”减小,即不冈其量的增减而影响反应速率,但会因固体表面积的变化而改变反应速率。
(2)温度:其他条件相同时,升高温度,可以加快反应速率,实验测得,温度每升高10℃,化学反应速率通常增大到原来的2~4倍。
经验公式为
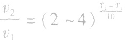
(3)压强:对于气体反应,当温度不变时,增大压强可以加快反应速率。对于气体反应体系,压强改变时有以下几种情况:

(4)催化剂:催化剂是能改变化学反应速率但在反应前后本身的质量和化学性质都不变的物质。对于某些化学反应,使用正催化剂能显著加快化学反应速率。
(5)其他因素:增大同体的表面积(如将块状改为粉末状),可增大反应速率;光照一般也可增大某些反应的速率;形成原电池可以加快反应速率;此外,超声波、放射线、电磁波等因素也能影响反应速率。
3.外因对化学反应速率影响的微观解释

发现相似题
与“某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜...”考查相似的试题有:
- 关于下列四个图象的说法中正确的是( )A.图①表示可逆反应“CO(g)+H2O(g)⇌CO2(g)+H2(g)”中的△H大于0B.图②是在电解氯...
- 下列关于化学观或化学研究方法的叙述,错误的是( )A.根据元素周期律,由HClO4可类推出氟元素也存在最高价氧化物的水化物HF...
- 用于净化汽车尾气的反应:2NO(g)+2CO(g)2CO2(g)+N2(g),已知该反应速率极慢,570 K时平衡常数为1×1059。下列说法正确的是[ ]A...
- 可逆反应:mA(g)+nB(g)pC(g)+qD(g),根据图回答:(1)压强P1比P2 __________(填大或小);(2)(a +b)比(c +d)______...
- 15.100 mL 6mol/L H2SO4跟过量锌粉反应,在一定温度下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可向反应物中加...
- 用纯净的CaCO3与稀HCl反应制CO2,实验过程记录如图所示。根据分析、判断,正确的是[ ]A.OE段表示反应速率最快B.EF段表示反...
- C+CO22CO; △H1>0,反应速率ν1 N2+3H22NH3; △H2<0,反应速率ν2。如升温,和的变化是A.同时增大 B.同时减少 C,ν1增大,ν2...
- 将除去氧化膜的镁条投入到少量稀盐酸中进行实验,实验测得氢气的产生速率变化情况如图曲线所示,对该曲线的解释中正确的是( ...
- 仅改变下列一个条件,通过提高活化分子的百分率来提高反应速率的是 ( )A.加热B.加压C.加负催化剂D.加大反应物浓度
- 恒温恒容条件下,能使正反应速率加快的是[ ]A. 减少C或D的物质的量B. 体积不变充入氦气使压强增大C. 减少B的物质的量D. 增大A...