本试题 “有A、B、C、D四种元素,其中A元素和B元素的原子都有1个末成对电子,A+比B-少一个电子层,B原子得一个电子后3p轨道全满;C原子的p轨道中有3个末成对电子,其气...” 主要考查您对原子核外电子的排布
晶体、非晶体
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 原子核外电子的排布
- 晶体、非晶体
原子核外电子的排布:
在多电子原子中,由于各电子所具有的能量不同,因而分布在离核远近不同的区域内做高速运动。能量低的电子在离核近的区域内运动,能量高的电子在离核较远的区域内运动。
电子层:
电子层在含有多个电子的原子里,电子分别存能量不同的区域内运动。我们把不同的区域简化为不连续的壳层,也称作电子层,分别用n=1,2,3,4,5.6,7或K、L、 M、N、O、P、Q来表示从内到外的电子层 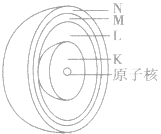

原子结构与元素的性质:
原子的核外电子排布对元素的化学性质有着非常重要的影响。元素的化学性质主要取决于原子的核外最外层电子数。
1.元素的金属性、非金属性(得失电子能力)与最外层电子数的关系
(1)稀有气体元素原子最外层电子数为8(He为 2),已达稳定结构,既不易失电子也小易得电子,所以化学性质不活泼。
(2)金属元素原子最外层电子数一般小于4,较易失去电子而达到稳定结构,其单质表现还原性。
(3)非金属元素原子最外层电子数一般大于或等于4,较易获得电子而达到稳定结构,其单质多表现氧化性。
2.元素的化合价与原子最外层电子数的关系
元素显正价还是显负价及其数值大小与原子的最外层电子数密切相关。其一般规律可归纳如下表: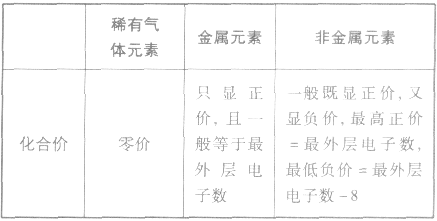
核外电子排布的一般规律:
(1)原子核外各电子层最多容纳2n2个电子.
(2)原子最外层电子数目不超过8个(K层为最外层时不超过2个)。
(3)次外层电子数目不超过18个(K层为次外层时不超过2个,L层为次外层时不超过8个)。倒数第三层电子数目不超过32个。
(4)核外电子分层排布,电子总是优先排布在能量最低的电子层里,然后由里向外,依次排布在能量逐渐升高的电子层里,即最先排K层,当K层排满后,冉排L层等。原子核外电子排布不是孤立的,而是相互联系的。层数相同而位置不同的电子层中最多容纳的电子数小一定相同,如N层为最外层时,最多只能排8个电子;N层为次外层时,最多只能排18个电子而不是32个电子(2×42=32)。
晶体与非晶体:
| 晶体 | 非晶体 | |
| 微观结构 | 原子在三维空间里呈周期性有序排列 | 原子排列相对无序 |
| 实例 | 白磷、硫黄、固态碘、高锰酸钾、干冰、金刚石、金属铜等绝大多数常见的固体 | 玻璃、石蜡、沥青等固体 |
| 自范性 | 有(能自发呈现封闭的、规则的多面体外形) | 无 |
| 各向异性 | 有(晶体在不同的方向上表现出不同的物理性质) | 无 |
| 对称性 | 有 | 无 |
| 熔点 | 固定 | 不固定 |
| 鉴别方法 | 对固体进行X一射线衍射实验。当单一波长的 X一射线通过晶体时,会在记录仪上看到分立的斑点或谱线 | |
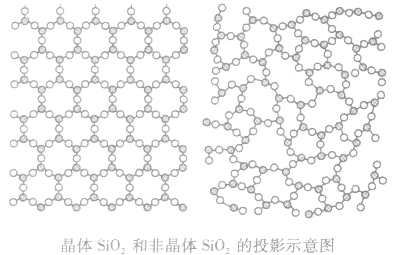
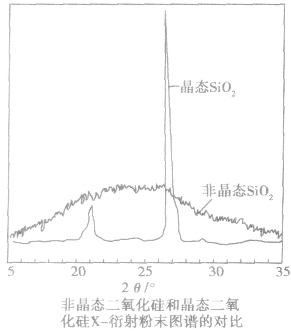
与“有A、B、C、D四种元素,其中A元素和B元素的原子都有1个末成对...”考查相似的试题有:
- 下列元素中,最高正化合价数值最大的是( )A.NaB.ClC.SD.Si
- 有X,Y两种原子,X原子的M电子层比Y原子的M电子层少3个电子,Y原子的L电子层的电子数恰为X原子的L层电子数的2倍,则X,Y元素...
- 下列叙述中不属于晶体特点的是[ ]A.一定有固定的几何外形B.一定有各向异性C.一定有固定的熔点D.一定是无色透明的固体
- 我国前科学院院长卢嘉锡与法裔加拿大科学家Gignere巧妙地利用尿素 (H2NCONH2)和H2O2形成加合物H2NCONH2·H2O2,不但使H2O2稳定...
- 下列物质中,长期放置在空气中会发生氧化还原反应而变质的是A.Na2O2B.NaOHC.Na2CO3·10 H2OD.NaCl
- 下列金属,熔点最低的是( )A.NaB.MgC.AlD.Hg
- “拟晶”(quasicrystal)是一种具有凸多面体规则外形但不同于晶体的固态物质。A165Cu23Fel2是二十世纪发现的几百种拟晶之一,具...
- 下列各组物质状态发生变化时,所克服的微粒间作用力完全相同的是A.碘的升华和干冰气化B.二氧化硅和干冰熔化C.苯和硝酸钾熔...
- 晶体与非晶体的严格判别可采用 ( )A.有否自范性B.有否各向同性C.有否固定熔点D.有否周期性结构
- (15分)铁、铝、铜等金属及其化合物在日常生活中应用广泛,请根据下列实验回答问题:(1)单质铁属于______晶体,将FeCl3溶液加...