本试题 “下列叙述正确的是( )A.乙酸与丙二酸互为同系物B.不同元素的原子构成的分子只含极性共价键C. 23592U和 23892U是中子数不同质子数相同的同种核素D.短周期...” 主要考查您对核素
元素周期表
化学键与化学反应中能量变化的关系
同系物
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 核素
- 元素周期表
- 化学键与化学反应中能量变化的关系
- 同系物
定义:
具有一定的质子数和中子数的一种原子叫做核素  的含义:
的含义: 表示一个质量数为A、质子数为Z的原子。
表示一个质量数为A、质子数为Z的原子。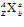 中A表示质量数,Z表示质子数,a表示粒子所带的电荷数和电性,b表示组成该粒子的原子数目。
中A表示质量数,Z表示质子数,a表示粒子所带的电荷数和电性,b表示组成该粒子的原子数目。
元素,核素与同位素的比较:
| 元素 | 同位素 | 核素 | |
| 概念 | 质子数(即核电荷数)相同的一类原子的总称 | 质子数相同而中子数不同的同一元素的不同原子互称为同位素 | 具有一定数目质子和一定数目中子的一种原子 |
| 描述对象 | 宏观物质,列同类原子而言,既有游离态,又有化合态 | 微观物质,对某种元素的原子而言,因为有同位素,所以原子种类多于元素种类 | 微观物质,指某种元素的某种原子 |
| 特征 | 以单质或化合物形式存在,性质通过形成单质或化合物来体现 | 同位素化学性质几乎相同,因为质量数不同,物理性质不同。天然存在的各种同位素所占的原子个数百分比一般不变 | 具有真实的质量,不同核素的质量不相同 |
| 实例 | H、Na、S为不同的三种元素 | 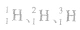 互为同位素 互为同位素 |
 是一种核素, 是一种核素, 是一种核素 是一种核素 |
元素周期表编排原则:
(1)把电子层数相同的各种元素按原子序数递增的顺序从左至右排成横行。
(2)把最外层电子数相同的元素按电子层数递增的顺序由上到下排列成纵行。
注意:①元素周期表是元素周期律的具体表现形式,它反映了元素之间相互联系的规律。
②历史上第一个元素周期表是1869年俄国化学家门捷列夫在前人探索的基础上排成的,他将元素按相对原子质量由小到大依次排列,并将化学性质相似的元素放在一个纵行。
元素周期表的结构:
(1)周期
①周期的含义在元素周期表中,把电子层数相同的元素,按原子序数递增的顺序从左到右排成横行,这样每个横行为一个周期。现在使用的元素周期表有7个横行,即7 个周期。
②周期的划分
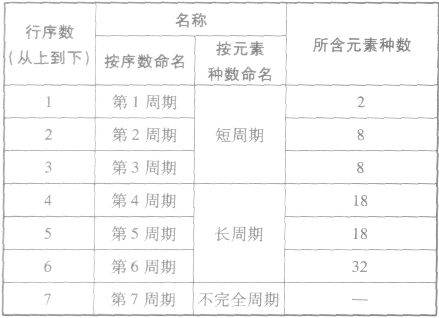
(2)族
①族的含义在周期表中,把不同横行(即周期)中最外层电子数相同的元素,按电子层数递增的顺序由上到下排成纵行,除第8、9、10三个纵行叫做第Ⅷ族外,其余15个纵行,每个纵行为一族。现在使用的元素周期表有18 个纵行,它们被划分为16个族。
②族的划分
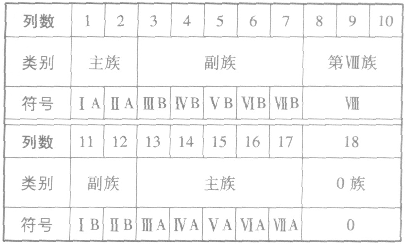
(3)元素周期表中主族元素金属性和非金属性的递变
断开化学键要吸收能量,形成化学键要释放能量,通过化学键的键能可以计算断开化学键或形成化学键所需的能量。
反应热与键能的关系:
化学反应的热效应来源于化学反应过程中断裂旧化学键并形成新化学键时的能量变化。当破坏旧化学键所吸收的能量小于形成新化学键所释放的能量时,为放热反应;
当破坏旧化学键所吸收的能量大于形成新化学键所释放的能量时,为吸热反应。

若
 反应为放热反应;若
反应为放热反应;若 或
或 ,反应为吸热反应。
,反应为吸热反应。同系物:
1.概念结构相似,在分子组成上相差一个或若干个CH2 原子团的有机物,互称为同系物。
2.判断同系物的方法
(1)同系物必符合同一通式。
(2)同系物必为同一类物质。如 和
和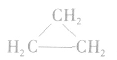 虽都符合通式
虽都符合通式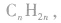 且组成上相差一个CH2原子团,但它们分别属于烯烃和环烷烃,结构不相似,不是同系物。
且组成上相差一个CH2原子团,但它们分别属于烯烃和环烷烃,结构不相似,不是同系物。
(3)同系物化学式不同。
(4)同系物结构相似但不一定完全相同,如 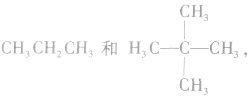 虽前者无支链,而后者有支链,结构不尽相同,但两者碳原子间均以单键结合成链状,结构仍相似,属同系物。
虽前者无支链,而后者有支链,结构不尽相同,但两者碳原子间均以单键结合成链状,结构仍相似,属同系物。
(5)同系物之间的物理性质不同,但化学性质相似。
注意:应用以上方法判断不同物质是否属于同系物时,首先要看两种有机物的结构是否相似、化学性质是否相似,然后再看组成上是否相差一个或若干个CH2原子团,才能快速、准确地作出判断。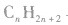 与
与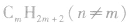 一定是同系物,
一定是同系物,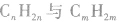 不一定是同系物;
不一定是同系物;
 与
与 与
与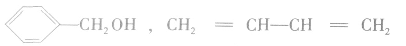 与
与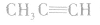 等均不是同系物。
等均不是同系物。
与“下列叙述正确的是( )A.乙酸与丙二酸互为同系物B.不同元素...”考查相似的试题有:
- 人类探测月球发现,其土壤中存在较丰富的质量数为3的氦元素,它是核聚变的重要原料之一.在地球上,氦元素主要以24He的形式存...
- 元素X的原子获得3个电子与元素Y的原子失去2个电子后,它们的电子层结构与氖原子的电子层结构相同。X、Y两种元素的单质在高温...
- 在下列化学反应中,既有离子键、极性键、非极性键断裂,又有离子键、极性键、非极性键形成的是( )A.CaC2+2H2O→Ca(OH)2+H...
- 下列各组物质中,都是由极性键构成为极性分子的一组的A.CH4和 H2OB.CO2和 HClC.NH3和 H2SD.HCN 和 BF3
- 化学反应的过程就是原来的化学键断裂,形成新的化学键的过程.下列物质中,化学键类型完全相同的是( )A.H2O和NaFB.N2和Na...
- (4分)通常人们把拆开1 mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可以估算化学反应...
- 下列过程都与热量变化有关,其中表述不正确的是( )A.CO(g)的燃烧热是283.0KJ/mol,则表示CO(g)燃烧反应的热化学方程式...
- (11分)下表中的数据是破坏1 mol物质中的化学键所消耗的能量(kJ):物质Cl2Br2I2HClHBrHIH2能量(kJ)243193151431366298436根...
- (6分)为了合理利用化学能,确保安全生产,化工设计需要充分考虑化学反应的焓变,并采取相应措施。化学反应的焓变通常用实验...
- 下列各组物质中,相互间一定互为同系物的是( ) A.1-丁烯 2-丁烯 B.C4H10和C20H42 C.C4H8和C3H6 D.一溴乙烷和1,2-二溴乙烷