本试题 “(一)5mol的CO2与8mol的SO2的分子数比是 ;原子数比是 ;质量比是 。(二)KClO3和浓HCl在一定温度下反应会生成黄绿色的易爆物二氧化氯。其反应可表述为: K...” 主要考查您对物质的量
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 物质的量
物质的量:
物质中含有一定数目粒子集体的物理量。是国际单位制中7个基本物理量之一(7个基本的物理量分别为:长度、质量、时间、电流强度、发光强度、温度、物质的量)符号:n
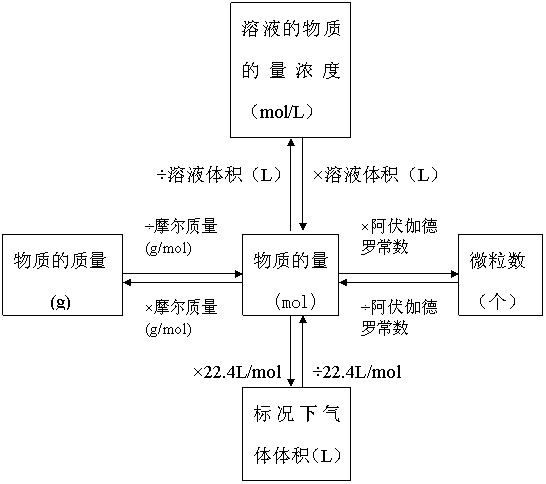
计算公式:物质的量(n)=粒子数(N)/阿伏加德罗常数(NA) 以物质的量为中心的各种化学常用量间的关系:n=N/NA=m/M=V/Vm=cV=ρV/M
物质中含有一定数目粒子集体的物理量。是国际单位制中7个基本物理量之一(7个基本的物理量分别为:长度、质量、时间、电流强度、发光强度、温度、物质的量)符号:n
计算公式:物质的量(n)=粒子数(N)/阿伏加德罗常数(NA) 以物质的量为中心的各种化学常用量间的关系:n=N/NA=m/M=V/Vm=cV=ρV/M
使用物质的量注意事项:
(1)物质的量表示物质所含指定粒子的多少,物质的量是一个整体,不得简化或增添任何字。
(2)物质的量及其单位摩尔的适用范围是微观粒子,因此在使用中应指明粒子的名称。
物质的量的相关解法:
问题探究:
(1)1mol氢这种说法正确吗?如何表示1mol氢原子、1mol氢分子、1mol氢离子?
答:使用摩尔作单位时,应用化学式(符号)指明离子的种类,1mol氢的说法不正确,因其咩有指明是氢分子还是氢离子、氢原子。1mol氢原子、1mol氢分子、1mol氢离子分别表示为1molH、1molH2、1molH+。
(2)阿佛加德罗常数和6.02×1023mol-1在实际使用上有何区别?
阿佛加德罗常数是一个非常精确的数字,而6.02×1023mol-1只是阿佛加德罗常数的一个近似值。在关于概念性描述时要求非常准确,要使用阿佛加德罗常数,而在涉及计算时,则用6.02×1023mol-1进行粗略计算。二者关系类似于数学上的圆周率∏与3.14的关系。
发现相似题
与“(一)5mol的CO2与8mol的SO2的分子数比是 ;原子数比是 ;质...”考查相似的试题有:
- 常温常压下,2.2 g CO2气体的摩尔质量是( )A.0.05 g/molB.0.05 molC.44 gD.44 g/mol
- 下列关于等温等压下,等质量气体H2、D2、T2的叙述中,正确的是①密度之比1:2:3 ②质子数之比6:3:2 ③中子数之比0:3:4 ④体...
- 有一在空气中暴露过的KOH固体,含H2O 2.8%(质量分数,下同),含K2CO37.2%。取1 g该样品投入到25 mL 2 mol·L-1盐酸中,中和多...
- 相对分子质量为M的气态化合物VL(已换算成标准状况)溶于m g水中,得到溶液的溶质质量分数为ω%,物质的量浓度为c mol/L,密度...
- 科学家发现一种化学式为H3的氢分子。1 mol H3和1 mol H2具有相同的[ ]A.分子数B.原子数C.质子数D.电子数
- 在一块大理石(主要成分是CaCO3)上,先后滴加①1mol/LHCl溶液和②0.1mol/LHCl溶液反应快的是滴加了____ _________的(填序号,...
- (8分)(1)已知20oC时的溶解度:Na2CO3:S=21.2g; NaHCO3:S=9.6g。则20oC恒温条件下向121.2g饱和碳酸钠溶液中通入足量...
- 某种氯原子的质量是a g,12C原子的质量是b g,用NA表示阿伏加德罗常数,下列说法正确的是A.氯元素的相对原子质量是B.m g该...
- 已知2.16 gX2O5中含有0.1 mol氧原子,则X的相对原子质量为 ( ) A.28B.28g/molC.14D.14g/mol
- 质量分数为a%,物质的量浓度为c mol/L 的KOH溶液,蒸发溶剂,恢复到原来温度,若质量分数变为2a%,则物质的量浓度变为A.大于...