本试题 “DME(二甲醚、CH3OCH3)是一种重要的清洁能源,可作为柴油的理想替代燃料和民用燃料,被誉为“二十一世纪的新能源”。另外,二甲醚还被广泛用作致冷剂、气雾剂...” 主要考查您对绿色化学
室内空气污染
海水资源的综合利用
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 绿色化学
- 室内空气污染
- 海水资源的综合利用
绿色化学:
1.定义绿色化学是一门研究运用现代科学技术的原理和方法来减少或消除化学产品的设计、生产和应用中有害物质的使用与产生,使所研究开发的化学产品和过程对环境更加友好的学科。
2.绿色化学的基本原则
(1)防治污染的产生优于治理产生的污染;
(2)原子经济性(设计的合成方法应将反应过程中所用的材料,尽可能全部转化到最终产品中)即原子的利用率达到100%。
(3)应考虑到能源消耗对环境和经济的影响,并应尽量少地使用能源(在常温、常压下进行)。
1.定义绿色化学是一门研究运用现代科学技术的原理和方法来减少或消除化学产品的设计、生产和应用中有害物质的使用与产生,使所研究开发的化学产品和过程对环境更加友好的学科。
2.绿色化学的基本原则
(1)防治污染的产生优于治理产生的污染;
(2)原子经济性(设计的合成方法应将反应过程中所用的材料,尽可能全部转化到最终产品中)即原子的利用率达到100%。
(3)应考虑到能源消耗对环境和经济的影响,并应尽量少地使用能源(在常温、常压下进行)。
室内空气污染物:
CO、CO2、NO2、NO、SO2、尼古丁;甲醛、苯、二甲苯、氡
CO:与血红蛋白易结合难分离而缺氧,结合能力是O2的200-300倍
甲醛HCHO:有刺激性气味气体,过敏性皮炎、免疫异常、中枢神经、致癌
氡Rn:无色无味放射性气体,存在岩石、土壤、石材中,可导致肺癌,隐性杀手
减少室内空气污染方法:
①保持室内外空气流通
②禁止吸烟
③装修用环保材料
CO、CO2、NO2、NO、SO2、尼古丁;甲醛、苯、二甲苯、氡
CO:与血红蛋白易结合难分离而缺氧,结合能力是O2的200-300倍
甲醛HCHO:有刺激性气味气体,过敏性皮炎、免疫异常、中枢神经、致癌
氡Rn:无色无味放射性气体,存在岩石、土壤、石材中,可导致肺癌,隐性杀手
减少室内空气污染方法:
①保持室内外空气流通
②禁止吸烟
③装修用环保材料
海水资源的综合利用:
浩瀚的海洋是个巨大的资源宝库,它不仅孕育着无数的生命,还孕育着丰富的矿产,而海水本身含有大量的化学物质,又是宝贵的化学资源。可从海水中提取大量的食盐、镁、溴、碘、钾等有用物质,海水素有“液体工业原料”之美誉。
浩瀚的海洋是个巨大的资源宝库,它不仅孕育着无数的生命,还孕育着丰富的矿产,而海水本身含有大量的化学物质,又是宝贵的化学资源。可从海水中提取大量的食盐、镁、溴、碘、钾等有用物质,海水素有“液体工业原料”之美誉。
海水制盐:
(1)海水制盐的方法:从海水中得到食盐的方法有蒸发法(盐田法)、电渗析法等。目前,以蒸发法(盐田法)为主。
(2)海水晒盐的基本原理:水分不断蒸发,氯化钠等盐结晶析出。
(3)海水晒盐的流程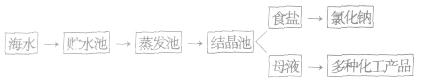
氯碱工业:
(1)食盐水的精制
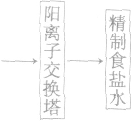
(2)电极反应
阴极: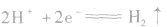
阳极:
总反应: :
:
(3)主要设备
离子交换膜电解槽一一阳极用金属钛(表面涂有钛、钉氧化物层)制成,阴极用碳钢(覆有镍镀层)制成。阳离子膜具有选择透过性,只允许Na+透过,而Cl-、 OH一和气体不能透过。 
(4)产品及用途
烧碱:可用于造纸、玻璃、肥皂等工业
氯气:可用于制农药、有机合成、氯化物的合成
氢气:可用于金属冶炼、有机合成、盐酸的制取
海水提溴:
(1)氯化
氯化氧化溴离子,在pH=3.5的酸性条件下效果最好,所以在氯化之前要将海水酸化。
(2)吹出
当海水中的Br一被氧化成Br2以后,用空气将其吹出。另外,也可以用水蒸气,使溴和水蒸气一起蒸出。
(3)吸收
目前比较多的是用二氧化硫作还原剂,使溴单质转化为HBr,再用氯气将其氧化得到溴产品。化学方程式如下: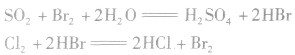
海水提镁:
(1)工艺流程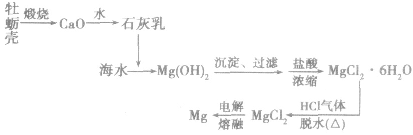
(2)主要化学反应
①制备石灰乳: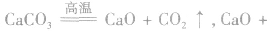
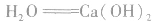
②沉淀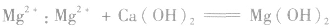
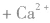
③制备
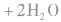
从海水中提取重水:
提取重水的方法:蒸馏法、电解法、化学交换法、吸附法等。常用方法:化学交换法(硫化氢一水双温交换法)
铀和重水目前是核能开发中的重要原料,从海水中提取铀和重水对一个国家来说具有战略意义,化学在开发海洋药物方面也将发挥越来越大的作用。潮汐能、波浪能也是越来越受到重视的新型能源。
发现相似题
与“DME(二甲醚、CH3OCH3)是一种重要的清洁能源,可作为柴油的...”考查相似的试题有:
- “绿色化学”的主要内容之一是指从技术、经济上设计可行的化学反应,使原子充分利用,不产生污染物。下列化学反应符合“绿色化学...
- 下列符合化学实验“绿色化学”的有[ ]①在萃取操作的演示实验中,将CCl4萃取溴水改为CCl4萃取碘水②在铜与浓硫酸反应的实验中,将...
- 电镀广泛地应用于工业生产中。在电镀铬的工业废水中主要含有Cr3+,同时还含有少量的Cu2+、Fe2+Fe3+和Al3+等,且酸性较强。为回...
- 我省要建成资源节约和生态保护型省份。下列措施或说法不符合这一理念的是A.做好空气质量预报工作,以便空气污染时及时采取防...
- ( 16分)活性ZnO俗称锌1-3,能改逬玻璃的化学稳定性,可用于生产特种玻璃,在橡胶的虫产屮能缩短硫化吋间,在涂料、油漆等工业...
- 2008年我国成功举办了奥运会、残奥会,让全世界人们重新认识了中国。北京奥运会期间各种污染物浓度日平均值比去年同期下降50%...
- (4分)2008年春节后汽车销售形势喜人,但是汽车尾气(含有烃类、CO、SO2与NO等物质)是城市的污染源。治理的方法之一是在汽...
- 下列对某些合成材料,如塑料制品废弃物的处理方法正确的是( )A.将废弃物混在垃圾中填埋在土壤里B.将废弃物焚烧C.将废弃物用...
- (1)防治环境污染,改善生态环境已成为全球的共识。①空气质量报告的各项指标可以反映出各地空气的质量。下列物质未纳入我国...
- 危险化学品的包装标签上要印有警示性标志。下列物质选用“腐蚀品”标志的是( )A.汽油B.食盐C.浓硫酸D.炸药