本试题 “无水硫酸铜(CuSO4)是白色粉末,具有很强的吸水性.吸水后白色粉末转化为蓝色晶体﹣胆矾(CuSO4·5H2O).(1)露置在空气中的无水硫酸铜吸收水蒸汽得到胆矾...” 主要考查您对饱和溶液,不饱和溶液
物理变化和化学变化的特征和判别
氢气的检验和验满
一氧化碳的检验
二氧化碳的检验和验满
物质的相互转化和制备
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 饱和溶液,不饱和溶液
- 物理变化和化学变化的特征和判别
- 氢气的检验和验满
- 一氧化碳的检验
- 二氧化碳的检验和验满
- 物质的相互转化和制备
饱和溶液和不饱和溶液的概念:
①饱和溶液:在一定温度下,在一定量的溶剂里,不能再溶解某种溶质的溶液,
叫做这种溶质的饱和溶液
②不饱和溶液:在一定温度下,在一定量的溶剂里,还能再继续溶解某种溶质的溶液,
叫做这种溶质的不饱和溶液
饱和溶液与不饱和溶液的相互转化方法:
(1)对于大多数固体:在一定量的水中溶解的最大量随温度升高而增大
饱和溶液 不饱和溶液
不饱和溶液
(2)对于Ca(OH)2:在一定量的水中溶解的最大量随温度升高而减少
饱和石灰水 不饱和石灰水
不饱和石灰水
概念的理解:
(1)溶液的饱和与不饱和跟温度和溶质的量的多少有关系。因此在谈饱和溶液与不饱和溶液时,一定要强调“在一定温度下”和“一定量的溶剂里”,否则就无意义。
(2)一种溶质的饱和溶液仍然可以溶解其他溶质。如氯化钠的饱和溶液中仍可溶解蔗糖。
(3)有些物质能与水以任意比例互溶,不能形成饱和溶液,如:酒精没有饱和溶液。
饱和溶液和不饱和溶液的相互转化:
一般,对饱和溶液与不饱和溶液相互转化过程中溶液组成的分析:
①饱和溶液 不饱和溶液(或不饱和溶液
不饱和溶液(或不饱和溶液 饱和溶液。不发生结晶的前提下)
饱和溶液。不发生结晶的前提下)
溶液中溶质、溶剂、溶液的质量不变,溶质质量分数不变。
②不饱和溶液 饱和溶液
饱和溶液
溶液的溶剂质量不变,溶质、溶液、溶质质量分数均增大。
③不饱和溶液 饱和溶液(不发生结晶的前提下)
饱和溶液(不发生结晶的前提下)
溶质质量不变,溶剂、溶液质量变小,溶质质量分数变大。
④饱和溶液 不饱和溶液
不饱和溶液
溶剂、溶液质量增大,溶质质量不变,溶质质量分数变小
判断溶液是否饱和的方法:
①观察法:当溶液底部有剩余溶质存在,且溶质的量不再减少时,表明溶液已饱和。
②实验法:当溶液底部无剩余溶质存在时,可向该溶液中加入少量该溶质,搅拌后,若能溶解或溶解一部分,表明该溶液不饱和;若不能溶解,则表明该溶液已饱和。
浓溶液,稀溶液与饱和溶液,不饱和溶液的关系:
为粗略地表示溶液中溶质含量的多少,常把溶液分为浓溶液和稀溶液。在一定量的溶液里含溶质的量相对较多的是浓溶液,含溶质的量相对较少的是稀溶液。它们与饱和溶液、不饱和溶液的关系如下图所示:
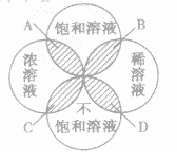 A. 饱和浓溶液B.饱和稀溶液C.不饱和浓溶液D.不饱和稀溶液
A. 饱和浓溶液B.饱和稀溶液C.不饱和浓溶液D.不饱和稀溶液
(1)溶液的饱和与不饱和与溶液的浓和稀没有必然关系。
(2)饱和溶液不一定是浓溶液,不饱和溶液不一定是稀溶液;浓溶液不一定是饱和溶液,稀溶液不一定是不饱和溶液。
(3)在一定温度下,同种溶剂、同种溶质的饱和溶液要比其不饱和溶液浓度大。
①饱和溶液:在一定温度下,在一定量的溶剂里,不能再溶解某种溶质的溶液,
叫做这种溶质的饱和溶液
②不饱和溶液:在一定温度下,在一定量的溶剂里,还能再继续溶解某种溶质的溶液,
叫做这种溶质的不饱和溶液
饱和溶液与不饱和溶液的相互转化方法:
(1)对于大多数固体:在一定量的水中溶解的最大量随温度升高而增大
饱和溶液
 不饱和溶液
不饱和溶液(2)对于Ca(OH)2:在一定量的水中溶解的最大量随温度升高而减少
饱和石灰水
 不饱和石灰水
不饱和石灰水概念的理解:
(1)溶液的饱和与不饱和跟温度和溶质的量的多少有关系。因此在谈饱和溶液与不饱和溶液时,一定要强调“在一定温度下”和“一定量的溶剂里”,否则就无意义。
(2)一种溶质的饱和溶液仍然可以溶解其他溶质。如氯化钠的饱和溶液中仍可溶解蔗糖。
(3)有些物质能与水以任意比例互溶,不能形成饱和溶液,如:酒精没有饱和溶液。
饱和溶液和不饱和溶液的相互转化:
一般,对饱和溶液与不饱和溶液相互转化过程中溶液组成的分析:
①饱和溶液
 不饱和溶液(或不饱和溶液
不饱和溶液(或不饱和溶液 饱和溶液。不发生结晶的前提下)
饱和溶液。不发生结晶的前提下)溶液中溶质、溶剂、溶液的质量不变,溶质质量分数不变。
②不饱和溶液
 饱和溶液
饱和溶液溶液的溶剂质量不变,溶质、溶液、溶质质量分数均增大。
③不饱和溶液
 饱和溶液(不发生结晶的前提下)
饱和溶液(不发生结晶的前提下)溶质质量不变,溶剂、溶液质量变小,溶质质量分数变大。
④饱和溶液
 不饱和溶液
不饱和溶液溶剂、溶液质量增大,溶质质量不变,溶质质量分数变小
判断溶液是否饱和的方法:
①观察法:当溶液底部有剩余溶质存在,且溶质的量不再减少时,表明溶液已饱和。
②实验法:当溶液底部无剩余溶质存在时,可向该溶液中加入少量该溶质,搅拌后,若能溶解或溶解一部分,表明该溶液不饱和;若不能溶解,则表明该溶液已饱和。
浓溶液,稀溶液与饱和溶液,不饱和溶液的关系:
为粗略地表示溶液中溶质含量的多少,常把溶液分为浓溶液和稀溶液。在一定量的溶液里含溶质的量相对较多的是浓溶液,含溶质的量相对较少的是稀溶液。它们与饱和溶液、不饱和溶液的关系如下图所示:
 A. 饱和浓溶液B.饱和稀溶液C.不饱和浓溶液D.不饱和稀溶液
A. 饱和浓溶液B.饱和稀溶液C.不饱和浓溶液D.不饱和稀溶液(1)溶液的饱和与不饱和与溶液的浓和稀没有必然关系。
(2)饱和溶液不一定是浓溶液,不饱和溶液不一定是稀溶液;浓溶液不一定是饱和溶液,稀溶液不一定是不饱和溶液。
(3)在一定温度下,同种溶剂、同种溶质的饱和溶液要比其不饱和溶液浓度大。
物理变化:
1. 定义:没有生成其他物质的变化
2. 实例:灯泡发光,冰融化成水;水蒸发变成水蒸气;碘,干冰的升华,汽油挥发,蜡烛熔化等都是物理变化。
化学变化:
1. 定义:物质发生变化时生成其他物质的变化。
2. 实例:木条燃烧,铁生锈,食物腐烂
3. 现象:化学变化在生成新物质的同时,时常伴随着一些反应现象,表现为颜色改变,放出气体,生成沉淀等,化学变化不但生成其他物质,而且哈伴随着能量的变化,这种能量变化常表现为吸热,放热,发光等。
物理变化概念的理解:
(1)扩散,聚集,膨胀,压缩,挥发,摩擦生热,升温,活性炭吸附氯气等都是物理变化
(2)石墨在一定条件下变成金刚石不是物理变化而是化学变化,因为变成了另一种物质
(3)物理变化前后,物质的种类不变,组成不变,化学性质不变
(4)物理变化的实质是分子的聚集状态发生了改变,导致物质的外形或状态随之改变。
成语、俗语、古诗词蕴含的化学知识
(1)成语、俗语中的变化
①物理变化:只要功夫深,铁柞磨成针;
冰冻三尺非一日之寒;
木已成舟;滴水成冰;花香四溢等。
②化学变化:百炼成钢、点石成金、蜡炬成灰等。
(2)古诗词中的变化于谦的《石灰吟》:
千锤万凿出深山—物理变化
烈火焚烧若等闲—化学变化
粉身碎骨浑不怕—化学变化
要留清白在人间—化学变化
物质的三态变化
(1)物态变化是指同一种物质可在固态,气态,液态三种状态发生转化的过程,如下图,物态变化过程没有新物质生成,属于物理变化。

(2)物态变化过程中的名称和热量变化
1. 定义:没有生成其他物质的变化
2. 实例:灯泡发光,冰融化成水;水蒸发变成水蒸气;碘,干冰的升华,汽油挥发,蜡烛熔化等都是物理变化。
化学变化:
1. 定义:物质发生变化时生成其他物质的变化。
2. 实例:木条燃烧,铁生锈,食物腐烂
3. 现象:化学变化在生成新物质的同时,时常伴随着一些反应现象,表现为颜色改变,放出气体,生成沉淀等,化学变化不但生成其他物质,而且哈伴随着能量的变化,这种能量变化常表现为吸热,放热,发光等。
物理变化:
1. 特征:没有新物质生成。
2. 微观实质:分子本身没有变(对于由分子构成的物质),主要指形状改变或三态变化。
化学变化:
1. 特征:有新物质生成
2. 微观实质:物质发生化学变化时,反应物的分子在化学反应中分成了原子,原子重新组成构成新分子。
物理变化概念的理解:
(1)扩散,聚集,膨胀,压缩,挥发,摩擦生热,升温,活性炭吸附氯气等都是物理变化
(2)石墨在一定条件下变成金刚石不是物理变化而是化学变化,因为变成了另一种物质
(3)物理变化前后,物质的种类不变,组成不变,化学性质不变
(4)物理变化的实质是分子的聚集状态发生了改变,导致物质的外形或状态随之改变。
成语、俗语、古诗词蕴含的化学知识
(1)成语、俗语中的变化
①物理变化:只要功夫深,铁柞磨成针;
冰冻三尺非一日之寒;
木已成舟;滴水成冰;花香四溢等。
②化学变化:百炼成钢、点石成金、蜡炬成灰等。
(2)古诗词中的变化于谦的《石灰吟》:
千锤万凿出深山—物理变化
烈火焚烧若等闲—化学变化
粉身碎骨浑不怕—化学变化
要留清白在人间—化学变化
物质的三态变化
(1)物态变化是指同一种物质可在固态,气态,液态三种状态发生转化的过程,如下图,物态变化过程没有新物质生成,属于物理变化。

(2)物态变化过程中的名称和热量变化
| 变化过程 | 名称 | 热量变化 |
| 固态→气态 | 升华 | 吸热 |
| 气态→固态 | 凝华 | 放热 |
| 固态→液态 | 熔化 | 吸热 |
| 液态→固态 | 凝固 | 放热 |
| 液态→气态 | 汽化 | 吸热 |
| 气态→液态 | 液化 | 放热 |
氢气检验和验满方法:
1.检验:点燃待检测的气体,在火焰上方罩一个干燥的烧杯有水珠出现,滴入澄清石灰水
不变浑浊,则证明有氢气的存在
2.验满:一般使用排水法收集比较纯净的氢气,可以根据液面的高度判断。
向下排空气法:把带火星的木条放到瓶口,若有轻微的爆鸣声,说明氢气已满。
1.检验:点燃待检测的气体,在火焰上方罩一个干燥的烧杯有水珠出现,滴入澄清石灰水
不变浑浊,则证明有氢气的存在
2.验满:一般使用排水法收集比较纯净的氢气,可以根据液面的高度判断。
向下排空气法:把带火星的木条放到瓶口,若有轻微的爆鸣声,说明氢气已满。
一氧化碳的检验方法:
①点燃待检气体,先用干燥的小烧杯罩在火焰上方,无水珠.再用内壁涂有澄清石灰水的小烧杯罩在火焰上方,若出现白色浑浊物,则为CO气体。
②将待检气体通过灼热的CuO,若出现红色物质,且产生的气体能使澄清石灰水变浑浊,则该气体为CO。
二氧化碳的检验和验满:
1.检验:用燃着的木条检验,如果木条熄灭,则证明有二氧化碳存在;
或用澄清石灰水检验,如果澄清石灰水变浑浊,则证明有二氧化碳存在

2.验满:将燃着的木条放在瓶口,若熄灭则证明二氧化碳已满
常见气体的检验:
1.检验:用燃着的木条检验,如果木条熄灭,则证明有二氧化碳存在;
或用澄清石灰水检验,如果澄清石灰水变浑浊,则证明有二氧化碳存在

2.验满:将燃着的木条放在瓶口,若熄灭则证明二氧化碳已满
常见气体的检验:
| 物质 | 检验试剂或方法或装置或步骤 | 反应现象 | 结论和化学式 |
| O2 | 带火星的木条 | 木条复燃 | 氧气能支持燃烧 |
| CO2 | 澄清石灰水 | 澄清石灰水变浑浊 | CO2+Ca(OH )2==CaCO3↓+H2O |
| CO | 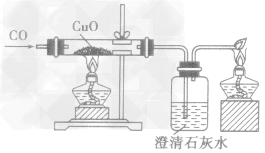 |
氧化铜由黑色变成红色,澄清石灰水变浑浊 | CO+CuO Cu+CO2 Cu+CO2Ca(OH)2+CO2==CaCO3↓+H2O |
| H2 |  |
氧化铜由黑色变成红色,无水CuSO4变成蓝色 | H2+CuO H2O+Cu H2O+CuCuSO4+5H2O==CuSO4·5H2O |
| H2O(g) |  |
无水CuSO4变蓝 | CuSO4+5H2O==CuSO4·5H2O |
| CH4 | (1)点燃 (2)火焰上方罩一个干燥的烧杯 (3)罩一个内壁用澄清石灰水润洗过的烧杯 |
(1)产生蓝色火焰 (2)烧杯内壁有水珠生成 (3)澄清石灰水变浑浊 |
CH4+O2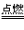 CO2+H2O CO2+H2OCa(OH)2+CO2==CaCO3↓+H2O |
| NH3 | (1)闻气味 (2)利用湿润的红色石蕊试纸检验 |
(1)有氨臭味 (2)湿润的红色石蕊试纸变蓝 |
—— |
物质的相互转化和制备:
主要是指以氧气、氢气、碳、硫、磷等为代表的非金属单质,以铝、镁、锌、铁、铜为代表的金属单质,以一氧化碳、二氧化碳等为代表的非金属氧化物,以氧化铜、氧化铁等为代表的金属氧化物,以盐酸、硫酸、碳酸等为代表的酸,以氢氧化钠、氢氧化钙等为代表的碱,以氯化钠、碳酸钠、碳酸氢钠、碳酸钙等为代表的盐,等等物质之间的相互和制备.
物质的相互转化:
氢氧化钠与氢氧化钙的制备:
(1)NaOH的制备
方法一:Na2O+H2O==2NaOH
方法二:Na2CO3+Ca(OH)2==CaCO3↓ +2NaOH
(2)Ca(OH)2的制备方法:CaO+H2O==Ca(OH)2
常见物质的相互转化:
Na→Na2O→NaOH→Na2CO3
C→CO→CO2→H2CO3
Fe→Fe2O3→Fe2(SO4)3→Fe(OH)3→FeCl3
S→SO2→SO3→H2SO4(单质硫不能直接转化为SO3)
各类物质间的转化关系:
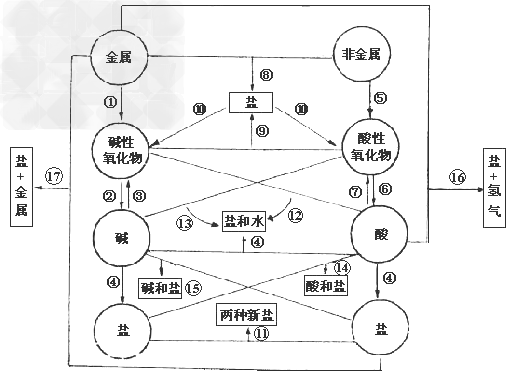
(1)金属+
 金属氧化物(碱性氧化物)
金属氧化物(碱性氧化物) 
(2)碱性氧化物(可溶)+水
 碱(可溶)
碱(可溶)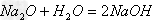
(3)碱(难溶)
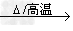 碱氧(难溶)+水
碱氧(难溶)+水 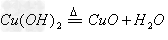
(4)酸+碱
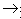 盐+水
盐+水 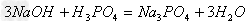 ;
;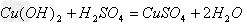
(5)非金属+
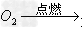 非金属氧化物(酸性氧化物)
非金属氧化物(酸性氧化物)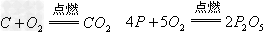
(6)酸性氧化物(易溶)+水
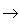 酸(易溶)
酸(易溶)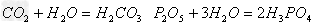
(7)酸(易挥发/难溶)
 酸氧+水(易挥发/难溶)
酸氧+水(易挥发/难溶) 
从纵向来看,金属
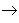 碱性氧化物
碱性氧化物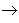 碱
碱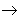 盐,其中金属元素相同。
盐,其中金属元素相同。非金属
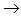 酸性氧化物
酸性氧化物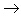 酸(含氧酸)
酸(含氧酸) 盐,其中非金属元素相同。
盐,其中非金属元素相同。横向:
(8)金属+非金属(无氧酸)
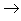 盐
盐 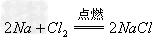
(9)碱氧+酸氧(含氧酸)
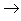 盐
盐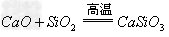
(10)含氧酸盐
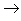 碱氧+酸氧
碱氧+酸氧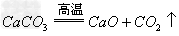
(11)盐+盐
 两种新盐
两种新盐 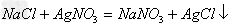
交叉:
(12)酸+碱氧
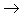 盐+水
盐+水
(13)碱+酸氧
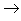 盐+水
盐+水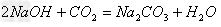
(14)酸+盐
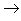 新酸+新盐
新酸+新盐 ;
;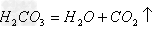
(15)碱+盐
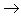 新碱+新盐
新碱+新盐
(16)金属+酸
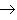 盐+
盐+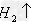
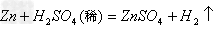
(17)金属+盐
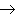 新盐+新金属
新盐+新金属(18)金属+盐
 新盐+新金属
新盐+新金属 (置换反应)
(置换反应) 发现相似题
与“无水硫酸铜(CuSO4)是白色粉末,具有很强的吸水性.吸水后白...”考查相似的试题有:
- 下列变化属于化学变化的是( )A.路面的水结成冰B.地震中房屋的倒塌C.电解水得到氢气和氧气D.将铁丝弯成奥运五环
- 抗甲型H1N1流感的有效药物达菲(化学式:C16H28N2O4) 可用莽草酸(化学式:C7H10O5)制取.下列说法错误的是( )A.莽草酸...
- 现在大量的城市改造美化了人们生活环境,在修路中用到大量的生石灰来使松软的地基变结实,这其中发生的变化有①将石灰石敲碎成...
- 生活中的下列现象属于化学变化的是( )A.冰棒融化B.湿衣晾干C.瓷碗破碎D.水果腐烂
- 下列过程中没有发生化学变化的是[ ]A. 水果榨果汁B. 鲜奶制酸奶C. 糯米酿甜酒D. 铁矿石冶炼成铁
- 物质的下列性质中,属于化学性质的是A.导电性B.氧化性C.吸水性D.挥发性
- 下列装置或操作肯定不能达到实验目的的是[ ]A.测定空气中氧气的含量B.探究质量守恒定律C.探究燃烧的条件D.检验二氧化碳是否集满
- 实验桌上放着三瓶没有标签的CO、O2、CO2气体,鉴别它们最简便的方法是A.测定它们是否有毒B.闻气味C.用澄清的石灰水D.用一...
- 下表列出了除去物质中所含少量杂质的方法,其中正确的是 物质所含杂质除去杂质的方法ACO气体CO2通过足量氢氧化钠溶液,并干燥...
- 物质间存在着一定的反应关系和转化关系.下列各组物质可以按所给图示进行直接转化的是( )A.Fe→Fe2O3→FeSO4→FeB.CO→CO2→H2...