本试题 “4P(红磷s)P4(白磷s);△H = +17kJ·mol-1根据以上方程式,下列推论正确的是[ ]A.当lmol白磷完全转变成红磷时放出17kJ热量B.正反应是一个放热反应C.当4g红磷...” 主要考查您对吸热反应、放热反应
焓变、反应热
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 吸热反应、放热反应
- 焓变、反应热
吸热反应:
吸收热量的反应,即生成物的总能量大于反应物的总能量,反应需要吸收能量
放热反应:
放出热量的反应,即生成物的总能量小于反应物的总能量,反应释放出能量
放热反应和吸热反应的比较:
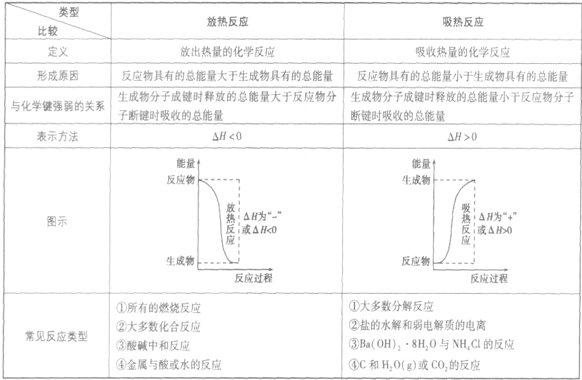
吸收热量的反应,即生成物的总能量大于反应物的总能量,反应需要吸收能量
放热反应:
放出热量的反应,即生成物的总能量小于反应物的总能量,反应释放出能量
放热反应和吸热反应的比较:

反应热,焓变:
化学能可以转化为热能、电能和光能等,化学反应中的能量变化,通常主要表现为热量的变化。
1.定义:在化学反应过程中,当生成物和反应物具有相同温度时所放出或吸收的热量,通常叫做化学反应的反应热。在恒温、恒压条件下,化学反应过程中吸收或放出的热量称为反应的焓变。
2.符号:△Ⅳ
3.单位:kJ·mol-1
4.产生原因:化学反应过程中旧键断裂吸收的总能量与新键形成释放的总能量不相等,故化学反应均伴随着能量变化——吸热或放热。
5.表示方法:放热反应的△H<0,吸热反应的△H>0.
化学能可以转化为热能、电能和光能等,化学反应中的能量变化,通常主要表现为热量的变化。
1.定义:在化学反应过程中,当生成物和反应物具有相同温度时所放出或吸收的热量,通常叫做化学反应的反应热。在恒温、恒压条件下,化学反应过程中吸收或放出的热量称为反应的焓变。
2.符号:△Ⅳ
3.单位:kJ·mol-1
4.产生原因:化学反应过程中旧键断裂吸收的总能量与新键形成释放的总能量不相等,故化学反应均伴随着能量变化——吸热或放热。
5.表示方法:放热反应的△H<0,吸热反应的△H>0.
发现相似题
与“4P(红磷s)P4(白磷s);△H = +17kJ·mol-1根据以上方程式,下列...”考查相似的试题有:
- 关于化学反应,下列叙述中不正确的是( )①放热的反应发生时不必加热②化学反应一定有能量变化③吸热反应需要加热后才能发生④化...
- 已知2SO2+O22SO3为放热反应,对该反应的下列说法中正确的是[ ]A.O2的能量一定高于SO2的能量B.SO2和O2的总能量一定高于SO3的...
- 下列说法正确的是[ ]A.Na2O2和水的反应是放热反应B.放热反应都不需加热即可进行C.若反应物总能量低于生成物总能量,该反应...
- 已知:(1)Zn(s)+O2(g)=== ZnO(s),ΔH=" -348.3" kJ·mol-1,(2)2Ag(s)+O2(g)=== Ag2O(s),ΔH=" -31.0" kJ·mol-1,则...
- 为了合理利用化学能,确保安全生产,化工设计需要充分考虑化学反应的焓变,并采取相应的措施。化学反应的焓变一般通过实验进...
- 已知:① 2CO(g)+O2(g)===2CO2(g) ΔH=-568kJ/mol② H2(g)+1/2O2(g)=H2O(g) ΔH=―248kJ·mol-1已知CO和H2的混合物1mol在...
- 以下反应中,Q1>Q2的是A.S(s)+O2(g)→ SO2(g)+ Q1kJ; S(g)+O2(g)→ SO2(g)+ Q2kJB.2H2(g)+O2(g)→ 2H2O(l)+Q1kJ ;2H2...
- 研究CO2与CH4,反应使之转化为CO和H2,对减缓燃料危机、减小温室效应具有重要的意义。(1)已知:2CO(g)+O2(g)=2CO2(g...
- (1)5.7g汽油(主要成分为C8H18,相对分子质量为114)完全燃烧生成液态水和CO2,放出275.9KJ的热量,则汽油的燃烧热为_______...
- 已知:H—H、Cl—Cl、H—Cl的键能分别为436 kJ/mol、243 kJ/mol和431 kJ/mol,估计1molCl2和1molH2完全反应生成2 molHCl的反应热...