本试题 “有A、B、C、D、E五种化合物,其中A、B、C、D是含铝元素的化合物,F是一种气体,标准状况下相对于空气的密度为1.103。它们之间有下列的转化关系:①A+NaOH→D+H2...” 主要考查您对无机推断
过氧化钠
氧化铝
氢氧化铝
偏铝酸盐
铝盐(铝离子)
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 无机推断
- 过氧化钠
- 氧化铝
- 氢氧化铝
- 偏铝酸盐
- 铝盐(铝离子)
无机推断的解题题眼:
1.题眼一:
常见气体单质气体:H2、O2、N2、Cl2(黄绿色)、F2(淡黄绿色)
气态氢化物:NH3(无色有刺激性气味,易液化,极易溶于水,能使湿润的红色石蕊试纸变蓝,遇到HCl形成白烟)
HCl(无色有刺激性气味,极易溶于水,能使湿润的蓝色石蕊试纸变红,在空气中形成白雾,遇到NH3形成白烟)
H2S(无色有臭鸡蛋气味,蛋白质腐败的产物,能溶于水,能使湿润的醋酸铅试纸变黑)
非金属气态氧化物:CO、CO2(直线型非极性分子)、NO(遇到空气变红棕色)、NO2(红棕色,加压、降温会转变成无色N2O4)、SO2(无色、有刺激性气味、能使品红溶液褪色) [固态氧化物]:SO3(无色晶体、易挥发)、P2O5(白色固体、易吸湿,常用作干燥剂)、SiO2(不溶于水、不溶于普通酸的高熔点固体,但溶于氢氟酸和强碱溶液)
气态卤代烃:一氯甲烷(CH3Cl)、氯乙烯(CH2=CHCl)气态醛:甲醛(HCHO)
2.题眼二:
气体溶解性归纳难溶于水的:H2、N2、CO、NO、CH4、C2H4;
微溶于水的:O2、C2H2;
能溶于水的:Cl2(1:1)、H2S(1:2.6)、SO2(1:40);
极易溶于水的:NH3(1:700)、HCl(1:500)、HF、HBr、HI。
3.题眼三:
常见液态物质无机物:液溴Br2、水(H2O)、过氧化氢(H2O2)、二硫化碳(CS2)、三氯化磷(PCl3)
有机物:一般5个碳原子以上的低级烃;除一氯甲烷、氯乙烯之外的低级卤代烃;低级醇;除甲醛之外的低级醛;低级羧酸;低级酯。
4.题眼四:
常见物质的颜色
①红色:Fe(SCN)3(红色溶液); Cu2O(红色固体);Fe2O3(红棕色固体); 液溴(深红棕色);Fe(OH)3(红褐色固体);Cu(紫红色固体);溴蒸气、NO2(红棕色)
②紫色:Fe3+与苯酚反应产物(紫色);I2(有金属光泽紫黑色固体)KMnO4固体(紫黑色);MnO4-(紫红色溶液) 钾的焰色反应(紫色) I2蒸气、I2在非极性溶剂中(紫色)
③橙色:溴水(橙色) K2Cr2O7溶液(橙色)
④黄色:AgI(黄色固体);AgBr(淡黄色固体); FeS2(黄色固体);Na2O2(淡黄色固体);S(黄色固体);I2的水溶液(黄色);Na的焰色反应(黄色);工业浓盐酸(黄色)(含有Fe3+);Fe3+的水溶液(黄色);久置的浓硝酸(黄色)(溶有分解生成的NO2);浓硝酸粘到皮肤上(天然蛋白质)(显黄色);
⑤绿色:Cu2(OH)2CO3(绿色固体);Fe2+的水溶液(浅绿色);FeSO4?7H2O(绿矾);Cl2、氯水(黄绿色);F2(淡黄绿色); CuCl2的浓溶液(蓝绿色);
⑥棕色:FeCl3固体(棕黄色);CuCl2固体(棕色)
⑦蓝色:Cu(OH)2、CuSO4?5H2O、Cu2+在水溶液中(蓝色);淀粉遇I2变蓝色; Cu(OH)2溶于多羟基化合物(如甘油、葡萄糖等)的水溶液中(绛蓝色);
⑧黑色:FeO;Fe3O4;FeS;CuO;CuS;Cu2S;MnO2;C粉;Ag2S;Ag2O;PbS; AgCl、AgBr、AgI、AgNO3光照分解均变黑;绝大多数金属在粉末状态时呈黑色或灰黑色。
⑨白色:常见白色固体物质如下(呈白色或无色的固体、晶体很多):AgCl;Ag2CO3;Ag2SO4;Ag2SO3;BaSO4;BaSO3;BaCO3;CaCO3;MgO;Mg(OH)2;MgCO3;Fe(OH)2;AgOH;PCl5;SO3;三溴苯酚;铵盐(白色固体或无色晶体); Fe(OH)2沉淀在空气中的现象:白色→(迅速)灰绿色→(最终)红褐色
5.题眼五:
根据框图中同一元素化合价的变化为主线,即A→B→C→……型归纳
C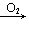 CO
CO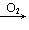 CO2;H2S
CO2;H2S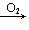 S
S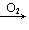 SO2
SO2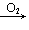 SO3(H2SO4); NH3(N2)
SO3(H2SO4); NH3(N2) NO
NO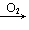 NO2→HNO3; Na
NO2→HNO3; Na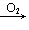 Na2O
Na2O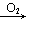 Na2O2; Fe→Fe2+→Fe(OH)2
Na2O2; Fe→Fe2+→Fe(OH)2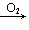 Fe(OH)3;Fe→Fe2+→Fe3+;
Fe(OH)3;Fe→Fe2+→Fe3+;
CH2=CH2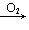 CH3CHO
CH3CHO CH3COOH;CH3CH2OH
CH3COOH;CH3CH2OH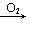 CH3CHO
CH3CHO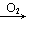 CH3COOH
CH3COOH
6.题眼六:
根据化学反应形式
(1)根据置换反应“单质+化合物=新的单质+新的化合物” 进行推理
㈠金属置换金属
铝热反应:需高温条件才能引发反应的发生,通常用来冶炼一些高熔点金属。如:2Al+Fe2O3 Al2O3+2Fe; 8Al+3Fe3O4
Al2O3+2Fe; 8Al+3Fe3O4 4Al2O3+9Fe
4Al2O3+9Fe
㈡.金属置换非金属
①金属与水反应置换出H2 2Na+2H2O==2Na++2OH-+H2↑ (非常活泼的金属在常温下与H2O反应) 3Fe+4H2O Fe3O4+4H2↑
Fe3O4+4H2↑
②金属与非氧化性酸(或氧化物)反应 2Al+6H+==2Al3++3H2↑;2Mg+CO2 2MgO+C
2MgO+C
㈢.非金属置换非金属
①非金属单质作氧化剂的如:2F2+2H2O==4HF+O2;2FeBr2+3Cl2==2FeCl3+2Br2;X2+H2S==2H++2X-+S↓(X2=Cl2、Br2、I2);2H2S+O2(不足)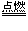 2S+2H2O (H2S在空气中不完全燃烧) 2H2S+O2==2S↓+2H2O(氢硫酸久置于空气中变质)
2S+2H2O (H2S在空气中不完全燃烧) 2H2S+O2==2S↓+2H2O(氢硫酸久置于空气中变质)
②非金属单质作还原剂的如:C+H2O CO+H2 (工业上生产水煤气的反应) Si+4HF==SiF4(易挥发)+2H2↑
CO+H2 (工业上生产水煤气的反应) Si+4HF==SiF4(易挥发)+2H2↑
㈣.非金属置换金属
如:2CuO+C 2Cu+CO2↑
2Cu+CO2↑
①根据反应“化合物+化合物=单质+化合物”进行推理,常见的该类型反应有:
2Na2O2+2H2O==4NaOH+O2↑
2Na2O2+2CO2==2Na2CO3+O2
2H2S+SO2==3S↓+2H2O
KClO3+6HCl(浓)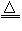 KCl+3Cl2↑+3H2O
KCl+3Cl2↑+3H2O
MnO2+4HCl(浓)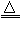 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
②根据反应“一种物质三种物质”进行推理,常见该类型的反应有:
Cu2(OH)2CO3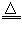 2CuO+CO2↑+H2O
2CuO+CO2↑+H2O
2KMnO4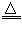 K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
NH4HCO3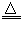 NH3↑+CO2↑+H2O
NH3↑+CO2↑+H2O
(NH4)2CO3 2NH3↑+CO2↑+H2O
2NH3↑+CO2↑+H2O
NH4HSO3 NH3↑+SO2↑+H2O
NH3↑+SO2↑+H2O
③根据反应“化合物+单质==化合物+化合物+……”,常见该类型的反应有:
Na2SO3+Cl2+H2O==Na2SO4+2HCl
Na2SO3+Br2+H2O==Na2SO4+2HBr
C+4HNO3(浓)==CO2↑+4NO2↑+2H2O
Cu+4HNO3(浓)==Cu(NO3)2+2NO2↑+2H2O
3Cu+8HNO3(稀)==3Cu(NO3)2+2NO↑+4H2O
7.题眼七:
根据常见反应的特征现象。
(1)两种物质反应既有沉淀又有气体生成的
①双水解:主要指Al3+、Fe3+与CO32-、HCO3-等之间的双水解
②Ba(OH)2和(NH4)2SO4生成氨气和硫酸钡沉淀
(2)遇水能放出气体的
①Li、Na、K、Ca、Ba、Mg(△)、Fe(高温)[氢后面的金属不跟水反应]
②Na2O2、NaH、CaC2、Al2S3、Mg3N2
③加碱能产生气体的:Al、Si、NH4+
④加酸有沉淀生成的:如SiO32-、AlO2-、S2O32-、C6H5O-(常温下)
⑤有“电解”条件的,通常联想到下列代表物:
a.电解电解质型:不活泼金属的无氧酸盐如CuCl2(aq)
b.放氧生酸型:不活泼金属的含氧酸盐如CuSO4(aq)
c.放氢生碱型:活泼金属的无氧酸盐如NaCl(aq)
d.电解熔融离子化合物:如Al2O3(l)、NaCl(l)
无机推断题的突破方法:
解决无机框图推断题的一般流程是:
整体浏览、寻找突破;
由点到面、广泛联系;
大胆假设、验证确认;
明确要求、规范解答 。
解题的关键是仔细审题,依据物质的特征来寻找突破口,顺藤摸瓜,进而完成全部未知物的推断。常用的突破方法主要有以下几种。
1.依据元素或物质的特征数据突破
常用的有:
(1)在地壳中含量最多的元素是氧;
(2)在地壳中含量最多的金属元素是铝;
(3)组成化合物种类最多的元素是碳;
(4)相对分子质量最小的单质是氢气;
(5)日常生活中应用最广泛的金属是铁。
2.依据物质的特性突破
常用的有:
(1)使淀粉变蓝的是I2;
(2)能使铁、铝钝化的是冷的浓硫酸或浓硝酸;
(3)能与SiO2反应而能雕刻玻璃的是氢氟酸;
(4)能使品红溶液褪色,褪色后的溶液受热后恢复红色的是二氧化硫;
(5)遇SCN-溶液变红色的是Fe3+;
(6)在放电的条件下与氧气化合生成NO的是氮气;
(7)能与水剧烈反应生成氧气的气体是F2;
(8)具有磁性的黑色固体是Fe3O4;
(9)红棕色粉末是Fe2O3;
(10)黄绿色气体是Cl2,红褐色沉淀是Fe(OH)3,能与水反应放出气体的淡黄色粉末是Na2O2。
3.依据物质的特殊用途突破
常用的有:
(1)可作呼吸面具和潜水艇中的供氧剂的是Na2O2;
(2)可用于杀菌、消毒、漂白的物质主要有Cl2、ClO2、NaClO和漂白粉等;
(3)可用作半导体材料、太阳能电池的是晶体硅;
(4)用于制造光导纤维的是SiO2;
(5)可用于治疗胃酸过多的物质是NaHCO3、Al(OH)3等;
(6)可用于制造发酵粉的是NaHCO3;
(7)可用作钡餐的是BaSO4;
(8)可用于焊接钢轨、冶炼难熔金属的是铝热剂;
(9)可用作感光材料的是AgBr;
(10)可用作腐蚀印刷电路板的是FeCl3溶液。
4.依据特殊现象突破
常用的有:
(1)燃烧时产生苍白色火焰的是氢气在氯气中燃烧;
(2)灼烧时火焰呈黄色的是含钠元素的物质;
(3)灼烧时火焰呈紫色(透过蓝色钴玻璃)的是含钾元素的物质;
(4)在空气中迅速由无色变红棕色的气体是NO;
(5)白色沉淀迅速变为灰绿色,最后变为红褐色的是Fe(OH)2转化为Fe(OH)3;
(6)能使湿润的红色石蕊试纸变蓝色的气体是NH3;
(7)使澄清石灰水先变浑浊后变澄清的是CO2、SO2;
(8)加入NaOH溶液先产生白色沉淀后沉淀溶解的溶液中含有Al3+。
5.根据限定条件和解题经验突破
常用的有:
(1)“常见金属”往往是铁或铝;
(2)“常见气体单质”往往是H2、N2、O2、Cl2;
(3)“常用的溶剂”往往是H2O;
(4)“常温常压下为液态”的往往是H2O;
(5)“能与过量HNO3反应”则意味着某元素有变价;
(6)“与浓酸反应”的物质往往是铜、碳、MnO2等;
(7)“电解”生成三种物质的往往为NaCl溶液或CuSO4溶液或AgNO3溶液;“电解”生成两种物质的往往是电解水型的溶液,生成的两种物质为氢气和氧气。熔融电解往往是电解Al2O3、NaCl或MgCl2。
无机物间的特殊转化关系:


二、三角型转化
1.铁三角: 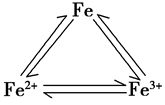
2.铝三角: 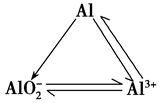
3.氯三角: 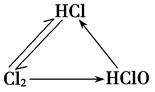
4.硅三角: 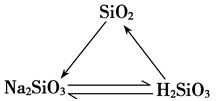
三、交叉型转化关系
1.硫及其重要化合物间的转化 :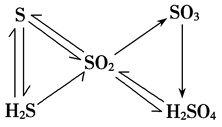
2.氮及其重要化合物间的转化 :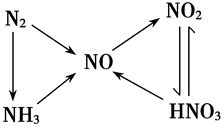
3.钠及其重要化合物间的转化 :



过氧化钠(Na2O2)的基本性质:
淡黄色固体,较稳定,可用作供氧剂、漂白剂
(1)与水反应:2Na2O2+2H2O==4NaOH+O2↑
(2)与CO2反应:2Na2O2+2CO2==2Na2CO3+ O2
(3)与HCl反应:2Na2O2+4HCl==4NaCl+2H2O+ O2↑
过氧化钠的特性及计算:
1.过氧化钠的强氧化性
2.Na2O2与CO2、H2O(g)反应的重要关系
(1)气体体积差的关系
2Na2O2+2CO2===2Na2CO3+O2 气体体积差 ①
2 1 ΔV=1
2Na2O2+2H2O(g)===4NaOH+O2 气体体积差 ②
2 1 ΔV=1
由此可见,若CO2和水蒸气的混合气体(或单一气体)通过足量Na2O2,气体体积的减少量是原气体体积的1/2,即为生成氧气的量。
(2)先后顺序关系
一定量的Na2O2与一定量的CO2和H2O(g)的混合物反应,可视为Na2O2首先与CO2反应,剩余的Na2O2再与H2O(g)反应。
(3)电子转移关系
当Na2O2与CO2或H2O反应时,每产生1molO2就转移2mol电子。
(4)固体质量变化关系
①足量过氧化钠与水、CO2反应的计算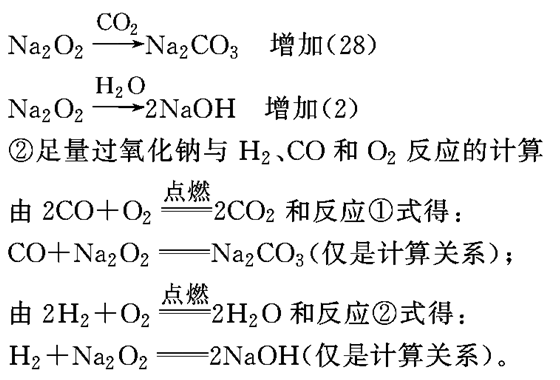
所以,有ag通式符合(CO)m(H2)n(m=0,1,2,3…,n=0,1,2,3…)的物质(包括纯净物和混合物)在氧气中燃烧,将其通过足量过氧化钠,反应完毕后,固体增重ag。
氧化钠与过氧化钠的比较:
| 物质 | 氧化钠 | 过氧化钠 |
| 色态 | 白色固体 | 淡黄色固体 |
| 类别 | 碱性氧化物 |
过氧化物(不属于碱性氧化物) |
| 化学键类型 | 仅含离子键 | 离子键和非极性键 |
| 电子式 | 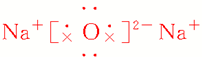 |
 |
| 生成条件 | 常温 | 点燃或加热 |
| 氧的化合价 | -2 | -1 |
| 阴阳离子个数比 | 1:2 | 1:2 |
| 稳定性 | 不稳定 | 稳定 |
| 转化关系 | 2Na2O+O2=2Na2O2 | |
| 用途 | 用于制取少量过氧化钠 | 供氧剂、漂白剂、氧化剂 |
| 与水反应方程式 | 2Na2O+2H2O=2NaOH | 2Na2O2+2H2O=4NaOH+O2↑ |
| 与CO2反应 | Na2O+CO2=NaCO3 | 2Na2O2+2CO2=2Na2CO3+O2↑ |
| 与HCl反应 | Na2O+2HCl=2NaCl+H2O | 2Na2O2+4HCl=4NaCl+2H2O+O2↑ |
| 保存 | 隔绝空气、密封保存 | 隔绝空气、远离易燃物、密封保存 |
特别提醒:
(1)用脱脂棉包裹住过氧化钠,滴加少量水时脱脂棉可以燃烧,不仅可以说明Na2O2与H2O反应生成O2,还可以说明该反应放热。
(2)Na2O2与H2O反应时H2O既不是氧化剂也不是还原剂。
方法技巧:Na2O与Na2O2的结构与性质
(1)Na2O中只含离子键,Na2O2中既含离子键,又含非极性键。
(2)等物质的量的Na2O与Na2O2分别于等量且足量的H2O反应,所得溶液的成分浓度相同
氧化铝的性质:
- 物理性质:白色固体,熔点高,是较好的耐火材料,天然的Al2O3叫刚玉,硬度仅次于金刚石;
- 化学性质:不溶于水的两性化合物,既能与酸反应,又能与强碱反应。
(1)与酸反应: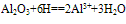
(2)与碱反应:
氧化铝的两性:
氧化铝属于两性氧化物,既能与酸反应,也能与强碱反应:
Al2O3+6H+===2Al3++3H2O
Al2O3+2OH-===2AlO2-+H2O
氧化铝与氧化镁的比较:
| 氧化物 | MgO | Al2O3 | |
| 工业制备 | MgCO3=(煅烧)=MgO+CO2↑ | 铝土矿——Al2O3 | |
| 中央物理性质 | 白色固体,熔点高,密度小 | 白色固体,熔点高,密度较小 | |
| 主要化学性质 | H2O | MgO+H2O==Mg(OH)2,很慢 | 不溶解,也不反应 |
| H+ | MgO+2H+==Mg2++H2O | Al2O3+6H+==2Al3++3H2O | |
| OH- | 不反应 | Al2O3+2OH-==2AlO2-+H2O | |
| 重要用途 | 制造耐火、耐高温器材 | 制造耐火、耐高温器材;工业冶炼铝 | |
氢氧化铝的性质:
不溶于水的白色胶状物质;能凝聚水中的悬浮物,可用作净水剂、可治疗胃酸过多、作糖的脱色剂等;既能与酸反应,又能与碱反应。
(1)与酸反应:Al(OH)3+3H+==Al3++3H2O
(2)与碱反应:Al(OH)3+OH-==AlO2-+2H2O
氢氧化铝的性质:
- 氢氧化铝是一种白色不溶于水的胶状沉淀,它能凝聚水中的悬浮物,并能吸附色素。
- 氢氧化铝既能与强酸反应也能与强碱反应,是两性氢氧化物。
- 氢氧化铝是医用的胃酸中和剂的一种,它的碱性不强,不至于对胃壁产生强烈的刺激或腐蚀作用,但却可以与酸反应,是胃液酸度降低,起到中和过多胃酸的作用。
- 氢氧化铝受热是分解成氧化铝和水。2Al(OH)3=(加热)=Al2O3+3H2O
氢氧化铝的制备:
实验室制法:Al2(SO4)3+6NH3·H2O==(NH4)2SO4+Al(OH)3↓
其他制法:①AlO2-+HCO3-+H2O=Al(OH)3↓+CO32-
②2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-
③AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-
④3AlO2-+Al3++6H2O==4Al(OH)3↓
例题:用稀H2SO4、NaOH溶液和金属铝为原料制取Al(OH)3。
甲、乙、丙三个学生的制备途径分别是
甲:
乙: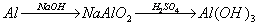
丙: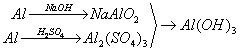
若要得到等量的Al(OH)3,则( B )
A.三者消耗的原料相同 B.甲消耗的原料的总物质的量最多 C.乙消耗的原料的总物质的量最少 D.丙消耗的原料的总物质的量最多
有关Al(OH)3的计算及图象分析:
解答有关Al(OH)3的图象和计算问题要注意以下三点:
(1)“铝三角”关系图中各物质转化方程式中的化学计量数关系。
(2)铝元素的存在形式。
(3)图象分析时:首先要看清横、纵坐标的含义,其次要对图象进行全面的分析,尤其需要关注的是特殊点(起点、折点、顶点、终点)的含义。
1、铝盐与强碱溶液作用生成Al(OH)3沉淀的计算
反应关系如下:
(1)Al3++3OH-==Al(OH)3(生成沉淀)
(2)Al(OH)3+OH-==AlO2-+2H2O(沉淀溶解)
(3)Al3++4OH-==AlO2-+2H2O(生成沉淀,又恰好溶解)
分析以上三个化学反应方程式,所得Al(OH)3沉淀的物质的量与n(Al3+)、n(OH-)的关系为:
当 ≤3时,所得沉淀的物质的量:n[Al(OH)3]=
≤3时,所得沉淀的物质的量:n[Al(OH)3]=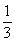 n(OH-)
n(OH-)
当 ≥4时,所得沉淀的物质的量:n[Al(OH)3]=0
≥4时,所得沉淀的物质的量:n[Al(OH)3]=0
当3< <4时,所得沉淀的物质的量:n[Al(OH)3]=4n(Al3+)-n(OH-)
<4时,所得沉淀的物质的量:n[Al(OH)3]=4n(Al3+)-n(OH-)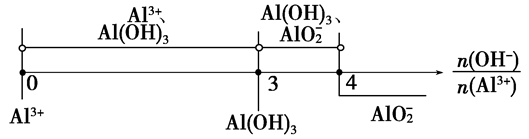
2、有关Al(OH)3的图像分析
①向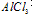 溶液中滴加
溶液中滴加 溶液
溶液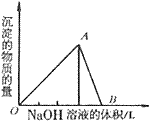
O~A段: 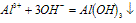
A~B段: 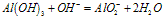
②向强碱溶液中滴入铝盐溶液 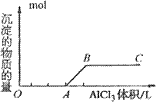
O~A段: 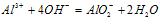
A~B段: 
③向铝盐溶液中滴入氨水或向氨水中滴加铝盐溶液
A. 向铝盐中滴加氨水时,当氨水增加到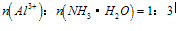 时,产生最大沉淀量
时,产生最大沉淀量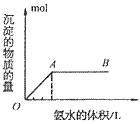
B. 向氨水中滴加铝盐溶液时,开始时氨水过量,如图所示 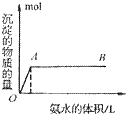
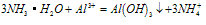
分析得:氢氧化铝不溶于弱碱氨水中。
④向偏铝酸盐溶液中滴入强酸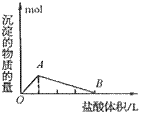
O~A段:
O~B段: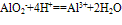
⑤向盐酸中滴加偏铝酸盐溶液 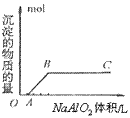
O~A段: 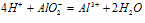
A~B段: 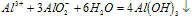
方法与技巧:
- 利用互滴顺序不同,现象不同可检验的溶液
(1)AlCl3溶液和盐酸
(2)NaAlO2溶液和盐酸
(3)Na2CO3溶液和盐酸
(4)AgNO3溶液和氨水 - 当溶液中有多种离子时,要考虑离子之间的反应顺序,如向含有H+、NH4+、Mg2+、Al3+的混合溶液中逐滴加入NaOH溶液,NaOH先与H+反应,再与Mg2+、Al3+反应生成沉淀,再与NH4+反应,最后才溶解Al(OH)3沉淀。一般是按生成水、沉淀、气体的顺序反应。可用图像表示为:
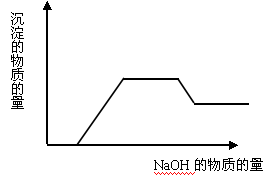
- AlO2-与HCO3-的反应不属于水解相互促进的反应,而是HCO3-电离出的H+与AlO2-发生的反应:AlO2-+HCO3-+H2O=Al(OH)3↓+CO32-
偏铝酸盐:
偏铝酸盐是指含有“AlO2-”集团的盐,是铝及其氧化物与强碱反应的产物。
例如Al(OH)3+OH-═AlO2-+2H2O。
偏铝酸盐的性质用离子方程式表示如下: ①偏铝酸盐溶液发生水解反应,溶液呈碱性。 ALO2-+2H2O==AL(OH)3+OH- ②偏铝酸盐与酸反应与强酸发生反应:适量强酸:ALO2-+H+H2O==AL(OH)3 过量强酸:ALO2-+4H+==AL3++2H2O 与弱酸(H2CO3)发生反应:即通入CO2气适量CO2:2ALO2-+CO2+3H2O==2AL(OH)3+CO32- 过量CO2:ALO2-+CO2+2H2O==AL(OH)3+HCO3- ③铝盐与偏铝酸盐溶液反应: AL3++3ALO2-+6H2O==4AL(OH)3 偏铝酸盐也可以理解为两性物质Al盐偏碱性的盐。AlO2-+H+(少量)+H2O==Al(OH)3↓
AlO2-+4H+(过量)==Al3++2H2O
偏铝酸盐的性质:
偏铝酸盐的性质用离子方程式表示如下:
①偏铝酸盐溶液发生水解反应,溶液呈碱性。AlO2-+2H2O==Al(OH)3+OH-
②偏铝酸盐与酸反应与强酸发生反应:
适量强酸:AlO2-+H++H2O==Al(OH)3
过量强酸:AlO2-+4H+==Al3++2H2O
与弱酸(H2CO3)发生反应:即通入适量CO2:2AlO2-+CO2+3H2O==2Al(OH)3+CO32-
过量CO2:AlO2-+CO2+2H2O==Al(OH)3+HCO3-
③铝盐与偏铝酸盐溶液反应:Al3++3AlO2-+6H2O==4Al(OH)3偏铝酸盐也可以理解为两性物质Al盐偏碱性的盐。
方法与技巧:
偏铝酸盐是在强碱性条件下生成的,所以它的存在环境也是强碱性环境,在离子共存题目中,经常遇到含有AlO2-的情况,遇到这样的题目,我们可以认为该溶液中含有OH-,与很多显酸性的离子不共存。例如:AlO2-与Al3+、Fe3+、NH4+、HCO3-等常见离子不共存。
“铝三角”关系:
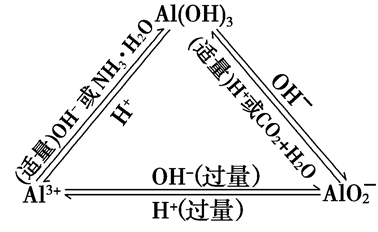
Al3++3OH-===Al(OH)3↓
Al(OH)3+OH-===AlO2-+2H2O
Al3++4OH-===AlO2-+2H2O
AlO2-+2H2O+CO2===Al(OH)3↓+HCO3-
AlO2-+H++H2O===Al(OH)3↓
AlO2-+4H+===Al3++2H2O
铝盐:
铝盐是指正三价铝离子和酸根阴离子组成的盐,一般来说呈白色或无色晶体,溶于水,个别不溶于水。
常用的铝盐主要有三氯化铝、硫酸铝和明矾。
(1)与碱反应:Al3++3OH-(少量)==Al(OH)3↓
Al3++4OH-(过量)== AlO2-+2H2O
(2)Al3++3AlO2-+6H2O==4Al(OH)3↓
铝盐的性质:
Al3+易水解,显酸性Al3++3H2O==Al(OH)3+3H+
(1)与碱反应:Al3++3OH-(少量)==Al(OH)3↓
Al3++4OH-(过量)==AlO2-+2H2O
(2)易发生双水解:Al3++3AlO2-+6H2O==4Al(OH)3↓
铝盐与强碱溶液作用生成Al(OH)3沉淀的计算
反应关系如下:
(1)Al3++3OH-==Al(OH)3(生成沉淀)
(2)Al(OH)3+OH-==AlO2-+2H2O(沉淀溶解)
(3)Al3++4OH-==AlO2-+2H2O(生成沉淀,又恰好溶解)
分析以上三个化学反应方程式,所得Al(OH)3沉淀的物质的量与n(Al3+)、n(OH-)的关系为:
当 ≤3时,所得沉淀的物质的量:n[Al(OH)3]=
≤3时,所得沉淀的物质的量:n[Al(OH)3]=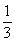 n(OH-)
n(OH-)
当 ≥4时,所得沉淀的物质的量:n[Al(OH)3]=0
≥4时,所得沉淀的物质的量:n[Al(OH)3]=0
当3< <4时,所得沉淀的物质的量:n[Al(OH)3]=4n(Al3+)-n(OH-)
<4时,所得沉淀的物质的量:n[Al(OH)3]=4n(Al3+)-n(OH-)
2、有关Al(OH)3的图像分析
①向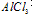 溶液中滴加
溶液中滴加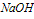 溶液
溶液
O~A段: 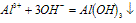
A~B段: 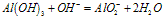
②向强碱溶液中滴入铝盐溶液 
O~A段: 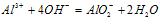
A~B段: 
③向铝盐溶液中滴入氨水或向氨水中滴加铝盐溶液
A. 向铝盐中滴加氨水时,当氨水增加到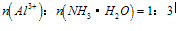 时,产生最大沉淀量
时,产生最大沉淀量
B. 向氨水中滴加铝盐溶液时,开始时氨水过量,如图所示 
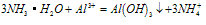
分析得:氢氧化铝不溶于弱碱氨水中。
④向偏铝酸盐溶液中滴入强酸
O~A段:
O~B段: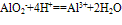
⑤向盐酸中滴加偏铝酸盐溶液 
O~A段: 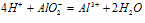
A~B段: 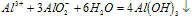
“铝三角”关系:

Al3++3OH-===Al(OH)3↓
Al(OH)3+OH-===AlO2-+2H2O
Al3++4OH-===AlO2-+2H2O
AlO2-+2H2O+CO2===Al(OH)3↓+HCO3-
AlO2-+H++H2O===Al(OH)3↓
AlO2-+4H+===Al3++2H2O
典型例题解析:
在50mLbmol·L-1的AlCl3溶液中加入50mLamol·L-1NaOH溶液。
(1)当a≤3b时,生成Al(OH)3沉淀的物质的量为________。
(2)当a、b满足________条件时,无沉淀产生。
(3)当a、b满足________条件时,先有沉淀生成,后又有部分沉淀溶解,此时Al(OH)3的质量为________g。
解析:依题意知,在AlCl3溶液中加入NaOH溶液有如下两个反应发生: AlCl3+3NaOH===Al(OH)3↓+3NaCl ①
AlCl3+4NaOH===NaAlO2+3NaCl+2H2O ②
根据以上两反应可以看出:
(1)当a≤3b时,只发生第一个反应,此时NaOH不足量,产生沉淀的量取决于NaOH。3n[Al(OH)3]=n(NaOH)?。所以答案为0.05a/3mol。
(2)如果无沉淀生成,Al元素全部以AlO2-形式存在。 n(AlCl3)∶n(NaOH)≤1∶4,即a∶b≥4∶1,所以答案为a≥4b。
(3)此种情况应当是两个反应均发生,铝元素以Al(OH)3和AlO2-两种形式存在。符合关系: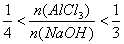 即
即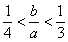 ,整理得:3b<a<4b或
,整理得:3b<a<4b或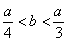 。
。
求沉淀的量的方法很多。
解法一:联立方程法。
设反应①中,AlCl3物质的量为x,则Al(OH)3为x,NaOH为3x。
反应②中AlCl3物质的量为y,NaOH为4y。 
解得x=(0.2b-0.05a)mol=0.05(4b-a)mol。 m[Al(OH)3]=78g·mol-1×0.05(4b-a)mol=3.9(4b-a)g。
解法二:守恒法。此种条件下,溶液中的离子有Na+、Cl-、AlO2-。
n(AlO2-)=n(Na+)-n(Cl-)=0.05amol-0.05×3bmol。
n[Al(OH)3]=n(Al3+)总-n(AlO2-)=0.05bmol-(0.05amol-0.15bmol)=(0.2b-0.05a)mol=0.05(4b-a)mol。
m[Al(OH)3]=78g·mol-1×0.05(4b-a)mol =3.9(4b-a)g。
【答案】 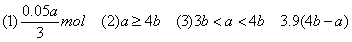
与“有A、B、C、D、E五种化合物,其中A、B、C、D是含铝元素的化合...”考查相似的试题有:
- (12分)已知物质M由同一短周期的X、Y两种元素组成,X原子的最外层电子数是最内层电子数的一半,Y元素最高正价与它的负价代数...
- A、B、C、D是按原子序数由小到大排列的前20号元素的单质。B、E均为组成空气的成分。F的焰色反应呈黄色。在G中,非金属元素与...
- 下图是中学化学中常见物质的转化关系,部分物质和反应条件略去。(1)G加热可分解生成A,A的化学式为________,写出物质A的一...
- (8分)已知A—K均为短周期元素形成的常见物质,H、I为气体单质,c为一种无色液体,I和K是工业上重要的还原剂,反应②是重要的...
- 下列关于钠及其化合物的叙述不正确的是A.钠是一种灰黑色、具有金属光泽、质地软的金属B.氧化钠与过氧化钠的颜色不同C.因为...
- 取ag某物质在氧气中完全燃烧,将其产物跟足量的过氧化钠固体完全反应,反应后固体的质量恰好也增加了ag.下列物质中不能满足...
- 下列叙述正确的是( )A.金属钠、镁等活泼金属着火时,可以使用泡沫灭火器来灭火B.称取等质量的两份铝粉,分别加入过量的稀盐...
- 下列物质中既能与稀硫酸反应,又能与氢氧化钠溶液反应是[ ](1)NaHCO3(2) (NH4)2S (3) Al2O3(4) Al (5) Al (OH)3A.(3) (4)B.(3...
- A、B、C是中学化学常见物质,含有同一种元素。其转化关系如下(1)若X为无色无味的气体,是一种常用氧化剂。A为气体化合物,...
- 下列各组物质混合之后,可生成A mol沉淀的是( )A.含A mol NaAlO2的溶液与A mol CO2B.含A mol NaAlO2的溶液与含A mol AlCl...