本试题 “草酸与高锰酸钾在酸性条件下能够发生如下反应:MnO4-+H2C2O4+H+--Mn2++CO2↑+H2O(未配平) 用4mL 0.001mol/L KMnO4溶液与2mL 0.01mol/L H2C2O4溶液,研究不同...” 主要考查您对影响化学反应速率的因素
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 影响化学反应速率的因素
影响化学反应速率的因素:
1.内因:参加反应的物质的结构及性质。
2.外因:主要是指浓度、温度、压强和催化剂,另外还有光、超声波、激光、搅拌、固体表面积、形成原电池等。
(1)浓度:其他条件相同时,增大反应物浓度,化学反应速率增大;减小反应物浓度,化学反应速率减小。在一定温度下,同体、纯液体的浓度视为定值,如C与CO2的反应、Na与H2O的反应中,C的量和Na、H2O 的量减少并不意味着其“浓度”减小,即不冈其量的增减而影响反应速率,但会因固体表面积的变化而改变反应速率。
(2)温度:其他条件相同时,升高温度,可以加快反应速率,实验测得,温度每升高10℃,化学反应速率通常增大到原来的2~4倍。
经验公式为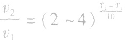
(3)压强:对于气体反应,当温度不变时,增大压强可以加快反应速率。对于气体反应体系,压强改变时有以下几种情况:

(4)催化剂:催化剂是能改变化学反应速率但在反应前后本身的质量和化学性质都不变的物质。对于某些化学反应,使用正催化剂能显著加快化学反应速率。
(5)其他因素:增大同体的表面积(如将块状改为粉末状),可增大反应速率;光照一般也可增大某些反应的速率;形成原电池可以加快反应速率;此外,超声波、放射线、电磁波等因素也能影响反应速率。
3.外因对化学反应速率影响的微观解释
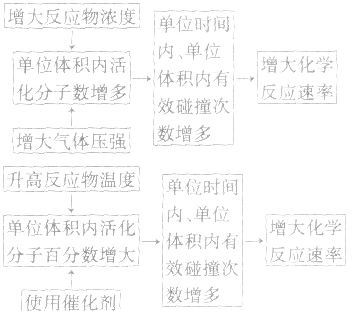
1.内因:参加反应的物质的结构及性质。
2.外因:主要是指浓度、温度、压强和催化剂,另外还有光、超声波、激光、搅拌、固体表面积、形成原电池等。
(1)浓度:其他条件相同时,增大反应物浓度,化学反应速率增大;减小反应物浓度,化学反应速率减小。在一定温度下,同体、纯液体的浓度视为定值,如C与CO2的反应、Na与H2O的反应中,C的量和Na、H2O 的量减少并不意味着其“浓度”减小,即不冈其量的增减而影响反应速率,但会因固体表面积的变化而改变反应速率。
(2)温度:其他条件相同时,升高温度,可以加快反应速率,实验测得,温度每升高10℃,化学反应速率通常增大到原来的2~4倍。
经验公式为
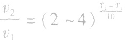
(3)压强:对于气体反应,当温度不变时,增大压强可以加快反应速率。对于气体反应体系,压强改变时有以下几种情况:

(4)催化剂:催化剂是能改变化学反应速率但在反应前后本身的质量和化学性质都不变的物质。对于某些化学反应,使用正催化剂能显著加快化学反应速率。
(5)其他因素:增大同体的表面积(如将块状改为粉末状),可增大反应速率;光照一般也可增大某些反应的速率;形成原电池可以加快反应速率;此外,超声波、放射线、电磁波等因素也能影响反应速率。
3.外因对化学反应速率影响的微观解释

发现相似题
与“草酸与高锰酸钾在酸性条件下能够发生如下反应:MnO4-+H2C2O4+...”考查相似的试题有:
- 工业上利用可逆反应N2(g)+3H2(g)2NH3(g)合成氨,下列叙述正确的是A.合成氨的适宜条件是高温、高压、催化剂,其中催化剂不改...
- 一定量的Fe与过量的稀硫酸反应制取氢气,一定温度下为加快反应速率而又不影响氢气的量,可向其中加入少量[ ]A.K2SO4固体B.Z...
- 用氮化硅陶瓷代替金属制造发动机的耐热部件,能大幅度提高发动机的热效率。工业上用化学气相沉积法制备氮化硅,其反应如下:3...
- 可逆反应mA(g)⇌nB(g)+pC(s);△H=Q,温度和压强的变化对正、逆反应速率的影响分别符合如图中的两个图象,以下叙述正确的...
- 下列关于各装置图的叙述不正确的是( )A.装置①中,c为阳极,d为阴极B.装置②可定量测定H2O2的分解速率C.关闭活塞a,从b处...
- 在100mL2mol/L的盐酸中加入足量的纯锌片,为了加快反应速率,又不影响生成氢气的总量,可采取的方法是A.加入适量6mol/L的HCl...
- 对于可逆反应:2SO2(g)+O2(g)2SO3(g) ΔH<0,降低温度产生的影响为A.v正增大,v逆减小B.v正减小,v逆增大C.v正和v逆同程...
- 升高温度,下列数据不一定同时增大的是[ ]A.化学反应速率vB.弱电解质的电离平衡常数KaC.化学平衡常数KD.水的离子积常数KW
- 等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定在不同时间t产生氢气体积V的数据,根据数据绘制得图,则曲线a、b、c...
- 在一固定体积的密闭容器中,充入2molA和1molB,发生如下反应:2A(g) + B(g)xC(g),平衡后,C的体积分数为W%,若维持容...