本试题 “已知氯气的漂白作用实际上是氯气与水反应生成的次氯酸的漂白作用.为了探究二氧化硫的漂白作用到底是二氧化硫本身还是二氧化硫与水作用的产物,某学习小组设...” 主要考查您对二氧化硫
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 二氧化硫
二氧化硫:
①化学式:SO2
②分子结构:SO2是由极性键形成的极性分子,因此易溶于水,其晶体为分子晶体。
二氧化硫的制备:
工业制法:

实验室制法:
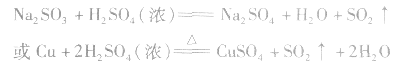
(1)收集:向上排空气法。
(2)检验:品红溶液。SO2是中学阶段学到的唯一种既能使品红褪色,加热后又能使其恢复原色的气体。
(3)尾气处理:用NaOH溶液吸收。
二氧化硫的用途:
工业上用二氧化硫漂白纸浆、毛、丝、草编制品等。此外,二氧化硫还可用于杀菌消毒,可以用作防腐剂。
二氧化硫对环境的污染及治理:

①化学式:SO2
②分子结构:SO2是由极性键形成的极性分子,因此易溶于水,其晶体为分子晶体。
二氧化硫的物理性质和化学性质:
1.物理性质:
SO2是无色、有刺激性气味的有毒气体,密度比空气大,易溶于水(常温常压下,1体积水大约溶解40体积的SO2),易液化(沸点-10℃)。
2.化学性质
(1)具有酸性氧化物的通性
①将SO2通入紫色石蕊试液中,试液变红。
②能与碱性氧化物、碱及某些盐反应。如:
(2)还原性 

(3)弱氧化性 
(4)漂白性(不能漂白酸碱指示剂) 能和某些有色物质化合生成无色物质,生成的无色物质不稳定,易分解而恢复原色,因此,SO2的漂白并不彻底。在中学化学常见试剂中,能用SO2漂白的只有品红溶液,品红溶液 无色溶液
无色溶液 恢复原色。
恢复原色。
SO2与一些物质反应的实验现象:


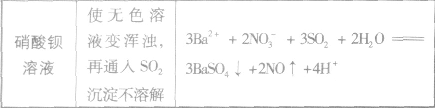
SO2与强碱反应后固体成分的确定:
SO2与强碱(如NaOH)溶液发生反应后的固体成分取决于二者的用量。遇到类似的问题,可以采用数轴分析法讨论。设SO2的物质的量为n(SO2),NaOH物质的量为n(NaOH),数轴代表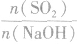 ,如下数轴所示:
,如下数轴所示: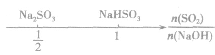
分析数轴可得:
(1)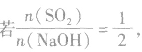 则固体物质为Na2SO3,
则固体物质为Na2SO3,
(2)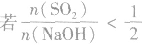 ,则固体物质为NaOH 和Na2SO3.
,则固体物质为NaOH 和Na2SO3.
(3)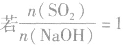 ,则同体物质为NaHSO3
,则同体物质为NaHSO3
(4)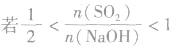 ,则固体物质为Na2SO3和NaHSO3,
,则固体物质为Na2SO3和NaHSO3,
(5)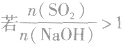 ,则固体物质为NaHSO3。
,则固体物质为NaHSO3。
二氧化硫的制备:
工业制法:

实验室制法:
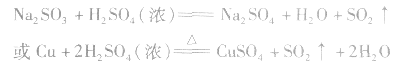
(1)收集:向上排空气法。
(2)检验:品红溶液。SO2是中学阶段学到的唯一种既能使品红褪色,加热后又能使其恢复原色的气体。
(3)尾气处理:用NaOH溶液吸收。
二氧化硫的用途:
工业上用二氧化硫漂白纸浆、毛、丝、草编制品等。此外,二氧化硫还可用于杀菌消毒,可以用作防腐剂。
二氧化硫对环境的污染及治理:

发现相似题
与“已知氯气的漂白作用实际上是氯气与水反应生成的次氯酸的漂白...”考查相似的试题有:
- 下列溶液中通入SO2一定不会产生沉淀的是( )A.Ba(OH)2B.Ba(NO3)2C.Na2SD.BaCl2
- 有一纯净的亚硫酸钠晶体因部分被氧化而变质,为了测定样品中杂质的质量分数进行以下实验过程,按要求填写空格:(1)向混合溶...
- 下列叙述正确的是A.浓硫酸具有吸水性,因而能使蔗糖炭化B.浓硫酸在常温下不容易与铜片反应放出二氧化硫气体C.浓硫酸是一种...
- 下列实验能证明SO2存在的是( )①能使澄清的石灰水变浑浊 ②能使湿润的蓝色石蕊试纸变红 ③能使湿润的品红试纸褪色 ④通入足量的...
- 己知25mL 0.1mol/L Na2S2O3溶液恰好把224mL Cl2(标准状况)完全反应为Cl-,则S2O32-将转化为( ) A.S2-B.SC.SO32-D.SO42-
- 下列叙述正确的是( )A.向NaAlO2溶液中滴加NH4Cl溶液,产生白色沉淀,加入NaHCO3溶液,则不产生沉淀B.在稀硫酸中加入铜粉...
- 工业上制硫酸的主要反应如下:4FeS2+11O2高温2Fe2O3+8SO2 2SO2+O22SO3SO3+H2O=H2SO4。用黄铁矿可以制取H2SO4,再用H2SO4可以...
- 在二氧化碳中混有少量的二氧化硫、三氧化硫、氯化氢杂质。设计一种一步只除去一种杂质,最后得到干燥纯净二氧化碳的实验方案...
- 下列说法中不正确的有[ ]①氯气与烧碱溶液或石灰乳反应都能得到含氯消毒剂; ②光照氯水有气泡逸出,该气体是Cl2; ③燃煤时加入...
- 在试管中注入某红色溶液,给试管加热,溶液颜色逐渐变浅,则原溶液可能是( )①滴有石蕊的H2SO4溶液 ②滴有酚酞的氨水溶液③滴...