本试题 “从下列物质①O2②CO2③CH4④NaOH ⑤H2SO4⑥H2中,将符合题意要求的序号填写在下面的横线上.(1)能使带火星的木条复燃的气体是______,(2)最简单的有机物是_____...” 主要考查您对浓硫酸的稀释
氧气的性质
乙醇
碱的性质
碱的用途
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 浓硫酸的稀释
- 氧气的性质
- 乙醇
- 碱的性质
- 碱的用途
浓硫酸:
俗称坏水。坏水指浓度大于或等于70%的硫酸溶液。浓硫酸在浓度高时具有强氧化性,这是它与普通硫酸或普通浓硫酸最大的区别之一。同时它还具有脱水性,强氧化性,难挥发性,酸性,稳定性,吸水性等。
浓硫酸的稀释:
稀释浓硫酸时,一定要将浓硫酸沿着器壁慢慢地注入水里,并不断搅拌,使产生的热量迅速地扩散,切不可把水倒入浓硫酸中,因为水的密度较小,浮在浓硫酸上面,溶解时放出的热会使水立刻沸腾。使硫酸液滴向四周飞溅,这是非常危险的(如下图)。若不慎将浓硫酸沾到皮肤上,应立即用大量水冲洗,然后涂上3%一5%的 NaHCO3溶液。
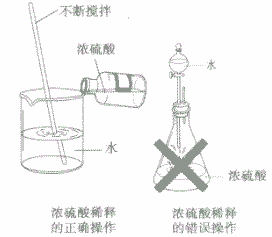
切记“酸入水,沿器壁,慢慢倒,不断搅”。注酸入水不断搅拌
俗称坏水。坏水指浓度大于或等于70%的硫酸溶液。浓硫酸在浓度高时具有强氧化性,这是它与普通硫酸或普通浓硫酸最大的区别之一。同时它还具有脱水性,强氧化性,难挥发性,酸性,稳定性,吸水性等。
浓硫酸的稀释:
稀释浓硫酸时,一定要将浓硫酸沿着器壁慢慢地注入水里,并不断搅拌,使产生的热量迅速地扩散,切不可把水倒入浓硫酸中,因为水的密度较小,浮在浓硫酸上面,溶解时放出的热会使水立刻沸腾。使硫酸液滴向四周飞溅,这是非常危险的(如下图)。若不慎将浓硫酸沾到皮肤上,应立即用大量水冲洗,然后涂上3%一5%的 NaHCO3溶液。

切记“酸入水,沿器壁,慢慢倒,不断搅”。注酸入水不断搅拌
定义:
氧气,空气主要组分之一,比空气重,标准状况(0℃和大气压强101325帕)下密度为1.429克/升。无色、无臭、无味。在水中溶解度很小。压强为101kPa时,氧气在约-183摄氏度时变为淡蓝色液体,在约-218摄氏度时变成雪花状的淡蓝色固体。
氧气的性质:
1.氧气的物理性质:
(1)无色无味,标况下,氧气的密度为1.429g/L,密度比空气大,难溶于水,1L水中只能溶解约30ml的氧气。
(2)三态变化:氧气(无色气体) 液氮(淡蓝色液体)
液氮(淡蓝色液体)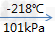 固态氮(淡蓝色雪花状)
固态氮(淡蓝色雪花状)
(3)工业产生的氧气,一般加压贮存在蓝色的钢瓶中。
2.氧气的化学性质:
(1)化学性质较活泼,在一定条件下,可以和多种物质发生化学反应,同时放出热量;具有助燃性和氧化性,在化学反应中提供氧,是一种常用的氧化剂。
(2)助燃性,氧化性
①与金属的反应:
2Mg+O2 2MgO
2MgO
3Fe+2O2 Fe3O4
Fe3O4
②与非金属的反应:
C+O2 CO2(O2充分)
CO2(O2充分)
2C+O2 2CO(O2不充分)
2CO(O2不充分)
③与化合物的反应:
2CO+O2 2CO2
2CO2
CH4+2O2 CO2+2H2O
CO2+2H2O
C2H5OH+3O2 2CO2+3H2O
2CO2+3H2O
易错点:
(1)误认为氧气具有可燃性,可以做燃料
氧气可以帮助可燃物燃烧,具有助燃性,它本身不能燃烧,不能做可燃物。
(2)误认为氧气的化学性质非常活泼,能与所有物质发生反应
氧气是一种化学性质非常活泼的气体,在一定条件下能与许多物质发生化学反应,但不是与所有物质都能发生化学反应。
(3)误认为燃烧都需要氧气
燃烧有广义和狭义之分,通常所说的燃烧是指可燃物与氧气发生的一种发光,放热的剧烈的氧化反应。燃烧的条件之一是需要氧气。但有一些燃烧不需要氧气,如镁在二氧化碳中也能燃烧。
(4)误认为物质与氧气的反应叫氧化反应
氧化反应是物质与氧发生的反应,其中包括物质与氧气中的氧元素发生的反应,也包括物质与其他含氧物质中的氧元素发生的反应。如氢气与氧气反应生成水是氧化反应,氢气与氧化铜反应生成铜和水也是氧化反应。
(5)误认为氧气与液氧性质不行
物质的性质包括物理性质和化学性质,氧气与液氧物理性质不同,但化学性质是相同的,因为它们二者的分子构成相同,都是由氧分子构成的。
(6)误认为含氧的物质都能制取氧气。
制取氧气需要含氧的物质,但不是所有的含氧物质都能用来制取氧气。
氧气,空气主要组分之一,比空气重,标准状况(0℃和大气压强101325帕)下密度为1.429克/升。无色、无臭、无味。在水中溶解度很小。压强为101kPa时,氧气在约-183摄氏度时变为淡蓝色液体,在约-218摄氏度时变成雪花状的淡蓝色固体。
氧气的性质:
1.氧气的物理性质:
(1)无色无味,标况下,氧气的密度为1.429g/L,密度比空气大,难溶于水,1L水中只能溶解约30ml的氧气。
(2)三态变化:氧气(无色气体)
 液氮(淡蓝色液体)
液氮(淡蓝色液体) 固态氮(淡蓝色雪花状)
固态氮(淡蓝色雪花状)(3)工业产生的氧气,一般加压贮存在蓝色的钢瓶中。
2.氧气的化学性质:
(1)化学性质较活泼,在一定条件下,可以和多种物质发生化学反应,同时放出热量;具有助燃性和氧化性,在化学反应中提供氧,是一种常用的氧化剂。
(2)助燃性,氧化性
①与金属的反应:
2Mg+O2
 2MgO
2MgO3Fe+2O2
 Fe3O4
Fe3O4②与非金属的反应:
C+O2
 CO2(O2充分)
CO2(O2充分)2C+O2
 2CO(O2不充分)
2CO(O2不充分)③与化合物的反应:
2CO+O2
 2CO2
2CO2CH4+2O2
 CO2+2H2O
CO2+2H2OC2H5OH+3O2
 2CO2+3H2O
2CO2+3H2O易错点:
(1)误认为氧气具有可燃性,可以做燃料
氧气可以帮助可燃物燃烧,具有助燃性,它本身不能燃烧,不能做可燃物。
(2)误认为氧气的化学性质非常活泼,能与所有物质发生反应
氧气是一种化学性质非常活泼的气体,在一定条件下能与许多物质发生化学反应,但不是与所有物质都能发生化学反应。
(3)误认为燃烧都需要氧气
燃烧有广义和狭义之分,通常所说的燃烧是指可燃物与氧气发生的一种发光,放热的剧烈的氧化反应。燃烧的条件之一是需要氧气。但有一些燃烧不需要氧气,如镁在二氧化碳中也能燃烧。
(4)误认为物质与氧气的反应叫氧化反应
氧化反应是物质与氧发生的反应,其中包括物质与氧气中的氧元素发生的反应,也包括物质与其他含氧物质中的氧元素发生的反应。如氢气与氧气反应生成水是氧化反应,氢气与氧化铜反应生成铜和水也是氧化反应。
(5)误认为氧气与液氧性质不行
物质的性质包括物理性质和化学性质,氧气与液氧物理性质不同,但化学性质是相同的,因为它们二者的分子构成相同,都是由氧分子构成的。
(6)误认为含氧的物质都能制取氧气。
制取氧气需要含氧的物质,但不是所有的含氧物质都能用来制取氧气。
定义:
乙醇的结构简式为C2H5OH,俗称酒精,它在常温、常压下是一种易燃、易挥发的无色透明液体,它的水溶液具有特殊的、令人愉快的香味,并略带刺激性。乙醇的用途很广,可用乙醇来制造醋酸、饮料、香精、染料、燃料等。医疗上也常用体积分数为70%——75%的乙醇作消毒剂等。
性状:无色透明液体(纯酒精),有特殊香味的气味,易挥发。能与水、氯仿、乙醚、甲醇、丙酮和其他多数有机溶剂混溶,相对密度(d15.56)0.816,易燃,蒸气能与空气形成爆炸性混合物。
危险特征:本品易燃,其蒸气与空气可形成爆炸性混合物。遇明火、高热能引起燃烧爆炸。与氧化剂接触发生化学反应或引起燃烧。在火场中,受热的容器有爆炸的危险。其蒸气比空气重,能在较低处扩散到相当远的地方,遇明火会引着回燃。
乙醇的性质:
1. 物理性质:性状无色透明、易燃易挥发液体。有酒的气味和刺激性辛辣味。
熔点-117.3℃
沸点78.32℃
相对密度0.7893
闪点14℃
溶解性溶于水、甲醇、乙醚和氯仿。能溶解许多有机化合物和若干无机化合物。
2. 化学性质:
氧化反应
(1)燃烧:发出淡蓝色火焰,生成二氧化碳和水(蒸气),并放出大量的热,不完全燃烧时还生成一氧化碳,有黄色火焰,放出热量
完全燃烧:C2H5OH+3O2 2CO2+3H2O
2CO2+3H2O
不完全燃烧:2C2H5OH+5O2 2CO2+2CO+6H2O
2CO2+2CO+6H2O
安全措施:
泄漏:迅速撤离泄漏污染区人员至安全区,并进行隔离,严格限制出入。切断火源。建议应急处理人员戴自给正压式呼吸器,穿消防防护服。尽可能切断泄漏源,防止进入下水道、排洪沟等限制性空间。
小量泄露:用砂土或其它不燃材料吸附或吸收。也可用大量水冲洗,洗水稀释后放入废水系统。
大量泄露:构筑围堤或挖坑收容;用泡沫覆盖,降低蒸气灾害。用防爆泵转移至槽车或专用收集器内,回收或运至废物处理场所处置。
灭火方法:
燃烧性:极易燃
灭火剂:抗溶性泡沫、干粉、二氧化碳、砂土。
灭火注意事项:尽可能将容器从火场移至空旷处。喷水保持容器冷却,直至灭火结束。
紧急处理:
吸入:迅速脱离现场至新鲜空气,若现象严重要尽快就医。
误食:饮足量温水,催吐。若现象严重要尽快就医。
皮肤接触:脱去被污染衣着,用流动清水冲洗。
眼睛接触:提起眼睑,用流动清水或生理盐水冲洗。若现象严重要尽快就医。
实验室使用及灭火
(1)应使用火柴点燃,否则容易使酒精灯内的酒精燃烧。
(2)使用完毕后,应用灯帽将火盖灭。
(3)如不慎将酒精洒出并引燃,则应用湿抹布将其盖灭。
乙醇的用途:
溶剂;有机合成;各种化合物的结晶;洗涤剂;萃取剂;食用酒精可以勾兑白酒;用作粘合剂;硝基喷漆;清漆、化妆品、油墨、脱漆剂等的溶剂以及农药、医药、橡胶、塑料、人造纤维、洗涤剂等的制造原料、还可以做防冻剂、燃料、消毒剂等。 75%(体积分数)的乙醇溶液常用于医疗消毒。
乙醇和甲醇的区别:
①甲醇是甲烷的一个氢原子被羟基(一个氢和一个氧组成的原子团,不是氢氧根)替换后的产物。
乙醇是乙烷一个氢原子被羟基替换后的产物,俗称酒精。
②分子式不一样。
甲醇:CH3OH
乙醇:CH3CH2OH
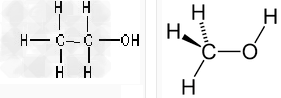
乙醇结构 甲醇结构
他们的分子式不一样,化学性质和物理性质也有区别。
③工业酒精里常含有甲醇,甲醇有毒,不能用工业酒精配制酒
乙醇汽油:
乙醇汽油也被称为(E型汽油),我国使用乙醇汽油是用90%的普通汽油与10%的燃料乙醇调和而成。它可以改善油品的性能和质量,降低一氧化碳、碳氢化合物等主要污染物排放。
乙醇的结构简式为C2H5OH,俗称酒精,它在常温、常压下是一种易燃、易挥发的无色透明液体,它的水溶液具有特殊的、令人愉快的香味,并略带刺激性。乙醇的用途很广,可用乙醇来制造醋酸、饮料、香精、染料、燃料等。医疗上也常用体积分数为70%——75%的乙醇作消毒剂等。
性状:无色透明液体(纯酒精),有特殊香味的气味,易挥发。能与水、氯仿、乙醚、甲醇、丙酮和其他多数有机溶剂混溶,相对密度(d15.56)0.816,易燃,蒸气能与空气形成爆炸性混合物。
危险特征:本品易燃,其蒸气与空气可形成爆炸性混合物。遇明火、高热能引起燃烧爆炸。与氧化剂接触发生化学反应或引起燃烧。在火场中,受热的容器有爆炸的危险。其蒸气比空气重,能在较低处扩散到相当远的地方,遇明火会引着回燃。
乙醇的性质:
1. 物理性质:性状无色透明、易燃易挥发液体。有酒的气味和刺激性辛辣味。
熔点-117.3℃
沸点78.32℃
相对密度0.7893
闪点14℃
溶解性溶于水、甲醇、乙醚和氯仿。能溶解许多有机化合物和若干无机化合物。
2. 化学性质:
氧化反应
(1)燃烧:发出淡蓝色火焰,生成二氧化碳和水(蒸气),并放出大量的热,不完全燃烧时还生成一氧化碳,有黄色火焰,放出热量
完全燃烧:C2H5OH+3O2
 2CO2+3H2O
2CO2+3H2O 不完全燃烧:2C2H5OH+5O2
 2CO2+2CO+6H2O
2CO2+2CO+6H2O安全措施:
泄漏:迅速撤离泄漏污染区人员至安全区,并进行隔离,严格限制出入。切断火源。建议应急处理人员戴自给正压式呼吸器,穿消防防护服。尽可能切断泄漏源,防止进入下水道、排洪沟等限制性空间。
小量泄露:用砂土或其它不燃材料吸附或吸收。也可用大量水冲洗,洗水稀释后放入废水系统。
大量泄露:构筑围堤或挖坑收容;用泡沫覆盖,降低蒸气灾害。用防爆泵转移至槽车或专用收集器内,回收或运至废物处理场所处置。
灭火方法:
燃烧性:极易燃
灭火剂:抗溶性泡沫、干粉、二氧化碳、砂土。
灭火注意事项:尽可能将容器从火场移至空旷处。喷水保持容器冷却,直至灭火结束。
紧急处理:
吸入:迅速脱离现场至新鲜空气,若现象严重要尽快就医。
误食:饮足量温水,催吐。若现象严重要尽快就医。
皮肤接触:脱去被污染衣着,用流动清水冲洗。
眼睛接触:提起眼睑,用流动清水或生理盐水冲洗。若现象严重要尽快就医。
实验室使用及灭火
(1)应使用火柴点燃,否则容易使酒精灯内的酒精燃烧。
(2)使用完毕后,应用灯帽将火盖灭。
(3)如不慎将酒精洒出并引燃,则应用湿抹布将其盖灭。
乙醇的用途:
溶剂;有机合成;各种化合物的结晶;洗涤剂;萃取剂;食用酒精可以勾兑白酒;用作粘合剂;硝基喷漆;清漆、化妆品、油墨、脱漆剂等的溶剂以及农药、医药、橡胶、塑料、人造纤维、洗涤剂等的制造原料、还可以做防冻剂、燃料、消毒剂等。 75%(体积分数)的乙醇溶液常用于医疗消毒。
乙醇和甲醇的区别:
①甲醇是甲烷的一个氢原子被羟基(一个氢和一个氧组成的原子团,不是氢氧根)替换后的产物。
乙醇是乙烷一个氢原子被羟基替换后的产物,俗称酒精。
②分子式不一样。
甲醇:CH3OH
乙醇:CH3CH2OH

乙醇结构 甲醇结构
他们的分子式不一样,化学性质和物理性质也有区别。
③工业酒精里常含有甲醇,甲醇有毒,不能用工业酒精配制酒
乙醇汽油:
乙醇汽油也被称为(E型汽油),我国使用乙醇汽油是用90%的普通汽油与10%的燃料乙醇调和而成。它可以改善油品的性能和质量,降低一氧化碳、碳氢化合物等主要污染物排放。
碱的定义:
碱是指在溶液中电离成的阴离子全部是OH-的化合物。碱由金属离子(或铵根离子)和氢氧根离子构成,可用通式R(OH)n表示。从元素组成来看,碱一定含有氢元素和氧元素。
常见的碱:
(1)氢氧化钠、氢氧化钙都属于碱。除这两种碱外,常见的碱还有氢氧化钾(KOH)、氨水(NH3·H2O)、治疗胃酸过多的药物中的氢氧化铝[Al(OH)3)。
(2)晶体(固体)吸收空气里的水分.表而潮湿而逐步溶解的现象叫做潮解。氢氧化钠、粗盐、氯化镁等物质都易潮解,应保存在密闭干燥的地方。同时称量 NaOH固体时要放在玻璃器皿中,不能放在纸上,防止 NaOH固体潮解后腐蚀天平的托盘。
(3)熟石灰可由生石灰(CaO)与水反应制得,反应的化学方程式为:CaO+H2O==Ca(OH)2,反应时放出大量的热。
碱的通性
常见的碱有NaOH、KOH、Ca(OH)2、氨水的特性:
①氢氧化钠(NaOH)俗名苛性钠、火碱、烧碱,这是因为它有强腐蚀性。NaOH是一种可溶性强碱。白色固体,极易溶于水,暴露在空气中易潮解,可用作碱性气体(如NH3)或中性气体(如H2、O2、CO等)的干燥剂。NaOH易与空气中的CO2反应生成Na2CO3固体。NaOH溶液可以腐蚀玻璃,盛NaOH溶液的试剂瓶不能用磨口的玻璃塞,只能用橡胶塞。
②氢氧化钙[Ca(OH)2]是白色粉末,微溶于水,俗称熟石灰或消石灰,其水溶液称为石灰水。Ca(OH)2也有腐蚀作用。Ca(OH)2与CO2反应生成白色沉淀CaCO3,常用于检验CO2。 Ca(OH)2+CO2=CaCO3↓+H2O Ca(OH)2能跟Na2CO3反应生成NaOH,用于制取NaOH。反应方程式为: Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
③氨水(NH3·H2O)是一种可溶性弱碱,NH3溶于水可得氨水。有刺激性气味,有挥发性。将氨气通过盛放氧化铜的玻璃管,生成氮气、水和铜,其反应方程式为: 2NH3+3CuO=(加热)=3Cu+N2↑+3H2O,说明氨气具有还原性。
此外,KOH、Ba(OH)2也是常见的可溶性强碱。不溶的碱大多是弱碱,如:Fe(OH)3、Cu(OH)2等。他们的共同性质是热稳定性差,受热易分解生成对应的金属氧化物和水。
氢氧化钠、氢氧化钙的物理性质和用途比较
氢氧化钠、氢氧化钙化学性质的比较
几种碱的颜色和溶解度
概念性质的理解
①氢氧化钠有强烈的腐蚀性,使用时必须十分小心,要防止沽到皮肤.上或洒在衣服上。如果不慎将碱液沽到皮肤上,应立即用较多的水冲洗,再涂上硼酸溶液。
②浓硫酸、氢氧化钠固体溶于水放热,属于物理变化;而氧化钙溶于水放热是氧化钙与水反应放出大量的热,属于化学变化;生石灰具有强烈的吸水性,可以作某些气体的干燥剂。
③由于NaOH易潮解,同时吸收空气中的CO2发生变质,所以NaOH必须密封保存。
④保存碱溶液的试剂瓶应用橡胶塞、不能用玻璃塞,以防止长期不用碱溶液,碱溶液腐蚀玻璃造成打不开的情况。
⑤只有可溶性碱溶液才能使指示剂变色,如NaOH溶液能使无色酚酞变红;但不溶性碱不能使指示剂变色,如Mg(OH)2中滴加无色酚酞,酚酞不变色。
⑥盐和碱的反应,反应物中的盐和碱必须溶于水,生成物中至少有一种难溶物、气体或H2O。铵盐与碱反应生成的碱不稳定,分解为NH3和H2O。
⑦碱与酸的反应中碱可以是不溶性碱,如 Cu(OH)2+H2SO4==CuSO4+2H2O。
氢氧化钠和氢氧化钙的鉴别:
NaOH与Ca(OH)2的水溶液都能使酚酞变红,故鉴别NaOH和Ca(OH)2不能用指示剂,通常情况下,可采用以下两种方法来鉴别NaOH和Ca(OH)2
方法一:通入CO2气体,NaOH溶液与CO2气体反应后无明显现象,但Ca(OH)2溶液即澄清石灰水与 CO2反应生成白色沉淀。
方法二:滴加Na2CO3溶液或K2CO3溶液,NaOH溶液与K2CO3,Na2CO3溶液不反应,但Ca(OH)2溶液与 Na2CO3、K2CO3溶液反应均生成白色沉淀。Ca(OH)2+ Na2CO3==CaCO3↓+2NaOH,Ca(OH)2+K2CO3 ==Na2CO3+2KOH。
检验二氧化碳气体是否与氢氧化钠溶液反应的方法
通常情况下,将二氧化碳气体直接通人装有氢氧化钠溶液的试管中,很难直接判断二氧化碳气体是否与氢氧化钠溶液反应。因此,要判断二氧化碳气体确实能与氢氧化钠反应,可以采取如下两种方法:
(1)检验产物的方法:验证通入二氧化碳气体后的溶液中是否含有碳酸钠,检验碳酸根离子是否存在。通常检验碳酸根离子的方法是:
方法1:取样,加入稀盐酸,并将产生的气体通入澄清石灰水中,若澄清石灰水变浑浊,则证明溶液中存在碳酸根离子。
方法2:取样,加入氢氧化钙溶液,若产生白色沉淀,则证明溶液中存在碳酸根离子。上述两种方法其实也可以检验氢氧化钠溶液是否变质.而且方法I还可以用于除去变质后的氢氧化钠溶液中的碳酸钠。
(2)改进实验装置,通过一些明显的实验现象间接证明二氧化碳气体能与氢氧化钠反应。如:
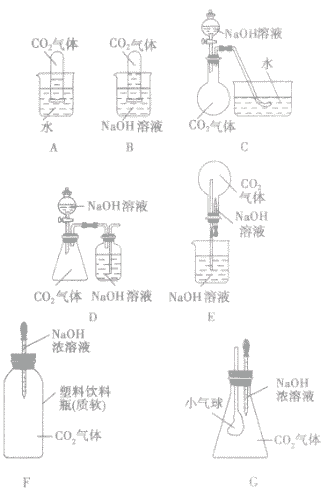
碱的命名:
一般读作氢氧化某,如:NaOH读作氢氧化钠。变价金属元素形成的碱,高价金属碱读作氢氧化某,如Fe(OH)3读作氢氧化铁,低价金属碱读作氢氧化亚某,如Fe(OH)2读作氢氧化亚铁。
氨水:
氨气的水溶液俗称氨水,主要成分是NH3·H2O,通常状况下是无色液体,具有挥发性。浓氨水能挥发出具有刺激性气味的氨气NH3。
氨水显碱性,能使指示剂变色。
氨水的组成中含有N元素,因此可通过与酸反应生成铵盐来制氮肥,其本身也是一种氮肥。在化学实验中一般可用浓氨水做分子运动的探究实验。
碱是指在溶液中电离成的阴离子全部是OH-的化合物。碱由金属离子(或铵根离子)和氢氧根离子构成,可用通式R(OH)n表示。从元素组成来看,碱一定含有氢元素和氧元素。
常见的碱:
(1)氢氧化钠、氢氧化钙都属于碱。除这两种碱外,常见的碱还有氢氧化钾(KOH)、氨水(NH3·H2O)、治疗胃酸过多的药物中的氢氧化铝[Al(OH)3)。
(2)晶体(固体)吸收空气里的水分.表而潮湿而逐步溶解的现象叫做潮解。氢氧化钠、粗盐、氯化镁等物质都易潮解,应保存在密闭干燥的地方。同时称量 NaOH固体时要放在玻璃器皿中,不能放在纸上,防止 NaOH固体潮解后腐蚀天平的托盘。
(3)熟石灰可由生石灰(CaO)与水反应制得,反应的化学方程式为:CaO+H2O==Ca(OH)2,反应时放出大量的热。
碱的通性
| 碱的通性 | 反应规律 | 化学方程式 | 反应类型 |
| 碱溶液与指示剂的反应 | 碱溶液能使紫色石蕊试液变蓝,无色酚酞试液变红 | —— | —— |
| 碱与非金属氧化物反应 | 碱+非金属氧化物→盐+水 | 2NaOH+CO2==Na2CO3+H2O Ca(OH)2+CO2==CaCO3↓+H2O |
—— |
| 碱与酸反应 | 碱+酸→盐+水 | NaOH+HCl==NaCl+H2O 2NaOH+H2SO4==Na2SO4+2H2O |
复分解反应 |
| 碱与某些盐反应 | 碱1+盐1→碱2+盐2 | 2NaOH+CuSO4==Cu(OH)2↓+Na2SO4 Ca(OH)2+Na2CO3==CaCO3↓+2NaOH |
复分解反应 |
| 碱+铵盐→氨气+水+盐 | NH4Cl+NaOH NaCl+NH3↑+H2O NaCl+NH3↑+H2O |
复分解反应 |
常见的碱有NaOH、KOH、Ca(OH)2、氨水的特性:
①氢氧化钠(NaOH)俗名苛性钠、火碱、烧碱,这是因为它有强腐蚀性。NaOH是一种可溶性强碱。白色固体,极易溶于水,暴露在空气中易潮解,可用作碱性气体(如NH3)或中性气体(如H2、O2、CO等)的干燥剂。NaOH易与空气中的CO2反应生成Na2CO3固体。NaOH溶液可以腐蚀玻璃,盛NaOH溶液的试剂瓶不能用磨口的玻璃塞,只能用橡胶塞。
②氢氧化钙[Ca(OH)2]是白色粉末,微溶于水,俗称熟石灰或消石灰,其水溶液称为石灰水。Ca(OH)2也有腐蚀作用。Ca(OH)2与CO2反应生成白色沉淀CaCO3,常用于检验CO2。 Ca(OH)2+CO2=CaCO3↓+H2O Ca(OH)2能跟Na2CO3反应生成NaOH,用于制取NaOH。反应方程式为: Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
③氨水(NH3·H2O)是一种可溶性弱碱,NH3溶于水可得氨水。有刺激性气味,有挥发性。将氨气通过盛放氧化铜的玻璃管,生成氮气、水和铜,其反应方程式为: 2NH3+3CuO=(加热)=3Cu+N2↑+3H2O,说明氨气具有还原性。
此外,KOH、Ba(OH)2也是常见的可溶性强碱。不溶的碱大多是弱碱,如:Fe(OH)3、Cu(OH)2等。他们的共同性质是热稳定性差,受热易分解生成对应的金属氧化物和水。
氢氧化钠、氢氧化钙的物理性质和用途比较
| 俗名 | 苛性钠,火碱,烧碱 | 熟石灰,消石灰 |
| 颜色、状态 | 白色,片状固体 | 白色,粉末状固体 |
| 腐蚀性 | 强烈腐蚀性 | 较强腐蚀性 |
| 溶解性 | 易溶于水,易潮解,溶解时放热 | 微溶于水,其水溶液俗称石灰水 |
| 用途 | 化工原料,用于肥皂、石油、纺织、印染工业等;生活中用于除油污 | 用于建筑工业,制漂自粉,改良土壤,配制农药等 |
氢氧化钠、氢氧化钙化学性质的比较
| 氢氧化钠 | 氢氧化钙 |
| 跟指示剂作用.使紫色石蕊试液变成蓝色,使无色酚酞试液变成红色 | 跟指示剂作用,使紫色石蕊试液变成蓝色,使无色酚酞试液变成红色 |
| 跟某些非金属氧化物反应 2NaOH+CO2==Na2CO3+H2O 2NaOH+SO2==Na2SO3+H2O 2NaOH+SO3==Na2SO4+H2O |
跟某些非金属氧化物反应 Ca(OH)2+CO2==CaCO3↓+H2O Ca(OH)2+SO2==CaSO3↓+H2O Ca(OH)2+SO3==CaSO4+H2O |
| 跟酸发生中和反应 2NaOH+H2SO4==Na2SO4+2H2O |
跟酸发生中和反应 Ca(OH)2+H2SO4==CaSO4+2H2O |
| 跟某些盐反应 2NaOH+CuSO4==Cu(OH)2↓+Na2SO4 |
跟某些盐反应 Ca(OH)2+Na2CO3==CaCO3↓+2NaOH |
几种碱的颜色和溶解度
| 碱 | 颜色 | 溶解性 |
| NaOH、KOH、Ba(OH)2 | 白色 | 易溶 |
| Ca(OH)2 | 白色 | 微溶 |
| Mg(OH)2、Al(OH )3、Fe(OH )2 | 白色 | 难溶 |
| Fe(OH )3 | 红褐色 | 难溶 |
| Cu(OH)2 | 蓝色 | 难溶 |
概念性质的理解
①氢氧化钠有强烈的腐蚀性,使用时必须十分小心,要防止沽到皮肤.上或洒在衣服上。如果不慎将碱液沽到皮肤上,应立即用较多的水冲洗,再涂上硼酸溶液。
②浓硫酸、氢氧化钠固体溶于水放热,属于物理变化;而氧化钙溶于水放热是氧化钙与水反应放出大量的热,属于化学变化;生石灰具有强烈的吸水性,可以作某些气体的干燥剂。
③由于NaOH易潮解,同时吸收空气中的CO2发生变质,所以NaOH必须密封保存。
④保存碱溶液的试剂瓶应用橡胶塞、不能用玻璃塞,以防止长期不用碱溶液,碱溶液腐蚀玻璃造成打不开的情况。
⑤只有可溶性碱溶液才能使指示剂变色,如NaOH溶液能使无色酚酞变红;但不溶性碱不能使指示剂变色,如Mg(OH)2中滴加无色酚酞,酚酞不变色。
⑥盐和碱的反应,反应物中的盐和碱必须溶于水,生成物中至少有一种难溶物、气体或H2O。铵盐与碱反应生成的碱不稳定,分解为NH3和H2O。
⑦碱与酸的反应中碱可以是不溶性碱,如 Cu(OH)2+H2SO4==CuSO4+2H2O。
氢氧化钠和氢氧化钙的鉴别:
NaOH与Ca(OH)2的水溶液都能使酚酞变红,故鉴别NaOH和Ca(OH)2不能用指示剂,通常情况下,可采用以下两种方法来鉴别NaOH和Ca(OH)2
方法一:通入CO2气体,NaOH溶液与CO2气体反应后无明显现象,但Ca(OH)2溶液即澄清石灰水与 CO2反应生成白色沉淀。
方法二:滴加Na2CO3溶液或K2CO3溶液,NaOH溶液与K2CO3,Na2CO3溶液不反应,但Ca(OH)2溶液与 Na2CO3、K2CO3溶液反应均生成白色沉淀。Ca(OH)2+ Na2CO3==CaCO3↓+2NaOH,Ca(OH)2+K2CO3 ==Na2CO3+2KOH。
检验二氧化碳气体是否与氢氧化钠溶液反应的方法
通常情况下,将二氧化碳气体直接通人装有氢氧化钠溶液的试管中,很难直接判断二氧化碳气体是否与氢氧化钠溶液反应。因此,要判断二氧化碳气体确实能与氢氧化钠反应,可以采取如下两种方法:
(1)检验产物的方法:验证通入二氧化碳气体后的溶液中是否含有碳酸钠,检验碳酸根离子是否存在。通常检验碳酸根离子的方法是:
方法1:取样,加入稀盐酸,并将产生的气体通入澄清石灰水中,若澄清石灰水变浑浊,则证明溶液中存在碳酸根离子。
方法2:取样,加入氢氧化钙溶液,若产生白色沉淀,则证明溶液中存在碳酸根离子。上述两种方法其实也可以检验氢氧化钠溶液是否变质.而且方法I还可以用于除去变质后的氢氧化钠溶液中的碳酸钠。
(2)改进实验装置,通过一些明显的实验现象间接证明二氧化碳气体能与氢氧化钠反应。如:

| 所选装置 | 操作方法 | 实验现象 |
| A | 将充满二氧化碳的试管倒扣在水中 | 试管内的液面略有上升 |
| B | 将充满二氧化碳的试管倒扣在氢氧化钠溶液中 | 试管内的液面明显上升 |
| C | 将氢氧化钠溶液滴入烧瓶 | 水槽中的水倒吸入烧瓶内 |
| D | 将氢氧化钠溶液滴入锥形瓶 | 集气瓶中,NaOH溶液中的长导管下端产生气泡 |
| E | 将胶头滴管中氢氧化钠溶液挤入烧瓶 | 烧瓶内产生“喷泉” 现象 |
| F | 将胶头滴管中的氢氧化钠溶液挤入软塑料瓶 | 塑料瓶变瘪 |
| G | 将胶头滴管中的氢氧化钠溶液挤入锥形瓶中 | 小气球胀大 |
碱的命名:
一般读作氢氧化某,如:NaOH读作氢氧化钠。变价金属元素形成的碱,高价金属碱读作氢氧化某,如Fe(OH)3读作氢氧化铁,低价金属碱读作氢氧化亚某,如Fe(OH)2读作氢氧化亚铁。
氨水:
氨气的水溶液俗称氨水,主要成分是NH3·H2O,通常状况下是无色液体,具有挥发性。浓氨水能挥发出具有刺激性气味的氨气NH3。
氨水显碱性,能使指示剂变色。
氨水的组成中含有N元素,因此可通过与酸反应生成铵盐来制氮肥,其本身也是一种氮肥。在化学实验中一般可用浓氨水做分子运动的探究实验。
常见的碱的用途:
1. 氢氧化钠:是重要的化工原料,广泛用于肥皂、石油、造纸、纺织和印染等工业。实验室中可作干燥剂。
2. 氢氧化钙:用于建筑业,制漂白粉,改良土壤。常用于实验室二氧化碳的检验。
1. 氢氧化钠:是重要的化工原料,广泛用于肥皂、石油、造纸、纺织和印染等工业。实验室中可作干燥剂。
2. 氢氧化钙:用于建筑业,制漂白粉,改良土壤。常用于实验室二氧化碳的检验。
发现相似题
与“从下列物质①O2②CO2③CH4④NaOH ⑤H2SO4⑥H2中,将符合题意要求的...”考查相似的试题有:
- 下列实验操作中,正确的是( )A.加入粉末状固体B.氧气验满C.稀释浓硫酸D.称量固体物质
- 富含淀粉的谷 物、甘薯等都可以酿酒。在酿酒的过程中,淀粉先转化成_________,再发酵成____________ 。
- 烧杯中盛有x溶液,逐滴加入(或通入)y物质,烧杯内液体的pH变化如下图所示。则符合该变化的一组物质是[ ]xy A NaOH 溶液稀HC...
- 下列物质中,难溶于水的是( )A.H2SO4B.NaClC.HClD.BaSO4
- 长途运输鱼苗时,人们常在水中加入少量过氧化钙(CaO2)固体.甲、乙两位同学发现往水中投入过氧化钙时产生气泡.请你、小明...
- 某同学把自制的一种黄色花汁,分别滴加到下列不同的试剂中,并记录观察到的现象如下表所示。试剂稀盐酸食醋蔗糖水蒸馏水肥皂...
- 下图是某品牌“洁厕灵” 标签上的部分文字(1)该“洁厕灵”呈 (填酸或碱)性(2)要在家中验证此结论,可采用的方法是 。
- 下列变化过程中,对应关系正确的是A.向一定量氢氧化钠溶液中加入水B.往等质量的Na2CO3和NaHCO3固体中加入足量HCl溶液C.将等...
- 当打开瓶盖时,瓶口能出现白雾的溶液是A.氢氧化钠B.氢氧化钙C.浓盐酸D.浓硫酸
- 下列物质放入水中,不会放出大量热的是( )A.浓硫酸B.氯化钠C.生石灰D.氢氧化钠