本试题 “小力同学对所学部分化学知识归纳如下,其中有错误的一组是( )A元素与人体健康B 相对大小比较人体缺氟--易生龋牙人体缺锌--影响人体发育人体缺碘--甲状腺肿...” 主要考查您对化学元素和人体健康
化学发展史
物质组成元素的质量分数
化合价的求法
地壳中各种元素的含量
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 化学元素和人体健康
- 化学发展史
- 物质组成元素的质量分数
- 化合价的求法
- 地壳中各种元素的含量
在人体中元素的存在形式:
①碳、氢、氧、氮主要以水、糖类、蛋白质、维生素和脂肪的形式存在。
②其他的元素主要以无机盐的形式存在于水溶液中。
③钙元素主要以羟基磷酸钙[Ca10(PO4)6(OH)2] 晶体的形式存在。
常量元素:
常量元素人体中含量较多的元素有11种,它们约占人体质量的99.95%。在人体中含量超过0.01%的元素,称为常量元素。
①人体中的常量元素
| 元素名称 | 元素符号 | 质量分数% |
| 氧 | O | 65.0 |
| 碳 | C | 18.0 |
| 氢 | H | 10.0 |
| 氮 | N | 3.0 |
| 钙 | Ca | 2.0 |
| 磷 | P | 1.0 |
| 钾 | K | 0.35 |
| 硫 | S | 0.25 |
| 钠 | Na | 0.15 |
| 氯 | Cl | 0.15 |
| 镁 | Mg | 0.05 |
②一些常量元素在人体中的作用及每天适宜摄入量
| 钙 | 使骨骼和牙街具有坚硬的结构支架 | 800—1200mg | 缺钙主要影响骨骼的发育和结构,临床症状表现为青少年的佝偻病和成年人的骨质软化症及老年人的骨质疏松症。钙是无毒的元素,但摄入过量会导致高血钙,从而引起消化系统、泌尿系统等的疾病 | 海产品、豆类、奶类、各种绿叶蔬菜等 | 其中99%存在于骨骼和牙齿中,主要以羟基磷酸钙 [Ca10(PO4)6(OH)2晶体的形式存在 |
| 钠 | 细胞外液和细胞内液中的Na+和K+各自保持一定的浓度,维持人体内的水分和体液恒定的pH | 2000—2500mg | 缺钠会引起肌肉痉挛、头痛等;过量会引起水肿、高血压、贫血等 | 食盐 | 其中一半以Na+的形式存在于细胞外液中 |
| 钾 | 1850—5600mg | 缺钾会引起肌肉不发达、心律小齐等;过量会导致恶心、腹泻等 | 香蕉、柑橘、橙子、山楂、蘑菇、豆炎及其制品等 | 主要以K+的形式萍在干细胞内液中 | |
| 镁 | 促进骨骼发育、细胞遗传物质合成等 | 300—400mg | 缺镁会引起肌肉不发达、抽搐、痉挛、心律不齐等;过量会引起神经系统紊乱、肾病等 | 坚果、大豆、牛奶等 | 70%的镁以磷酸盐和碳酸盐形式参与骨骼和牙齿的组成,25%的镁存在于软组织中 |
微量元素:
在人体中含量在0.01%以下的元素。
①一些人体必需的微量元素
| 元素名称 | 元素符号 |
| 铁 | Fe |
| 钴 | Co |
| 铜 | Cu |
| 锌 | Zn |
| 铬 | Cr |
| 锰 | Mn |
| 钼 | Mo |
| 氟 | F |
| 碘 | I |
| 硒 | Se |
②一些必需微量元素对人体的作用及14—18岁人群每天的适宜摄入量
| 元素 | 人体内的含量 | 对人体的作用 | 适宜摄入量(每天) | 摄入量过高,过低对人体健康的影响 |
| 铁 | 4—5g | 是血红蛋白的成分,能帮助氧气的运输 | 20—50mg | 缺铁会引起贫血 |
| 锌 | 2.5g | 影响人体发育 | 15.5—19mg | 缺锌会引起食欲不振,生长迟缓,发育不良 |
| 硒 | 14—21mg | 有防癌、抗癌作用 | 50μg | 缺硒可能引起表皮角质化和癌症。如摄入量过高,会使人中毒 |
| 碘 | 25—50mg | 是甲状腺激素的重要成分 | 150μg | 缺碘会引起甲状腺肿大,幼儿缺碘会影响生长发育,造成思维迟钝。过量也会引起甲状腺肿大 |
| 氟 | 2.6g | 能防治龋齿 | 1.5mg | 缺氟易产生龋齿,过量会引起氟斑牙和氟骨病 |
知识拓展:
如果人体所需的元素仅从食物中摄取还不足时,可通过食品添加剂和保健药剂来予以补充。
如在食品巾添加含钙、锌、硒、锗的化合物,或制成补钙、补锌等的保健药剂或制成加碘食盐,来增加对这些元素的摄人量。但要注意即使是人体必需的元素,也要注意适宜的摄入量,摄人量过高和过低对人体健康都有不良的影响。
化学的发展:
1.我国商代有了青铜器,春秋晚期能炼铁,战国时期能炼钢,唐代有了火药。
2.1774年法国化学家拉瓦锡提出了空气主要是由氧气和氮气组成的。
3.瑞典化学家舍勒和英国化学家普利斯特里先后用不同的方法制得了氧气。
4.1776年俄国化学家罗蒙诺索夫建立了质量守恒定律。
5.十九世纪初英国科学家道尔顿提出了近代原子学说。
6.1811年意大利科学家阿佛加德罗提出了分子的概念。
7.1869年俄国化学家门捷列夫发现了元素周期律。
化学发展六个时期:
(一)史前期:从远古到公元前1500年,化学作为一种技术,实际上已经开始出现了。尽管在这个期间,并没有文字记载,但是在中国、埃及、印度、巴比伦和后来的希腊、罗马,都可以找到人类利用化学的遗迹。猿人就知道用火,知道用火煮东西和烧制陶器。这可以说是最早期化学的开始。
(二)炼丹时期:大体说来是从公元前1500年到公元1650年。这个时期中国在化学方面的著作最多,例如《参同契》、《道藏》以及重要的本草书,都对我国古代化学成就作了详细的记载。至於在欧洲,这方面的书籍也很不少,例如阿拉伯、埃及和希腊,在1572年就有一部书,书名是《炼金的化学方法》。在欧洲,已经开始有“化学”这个名词了,并在1572年出版了《化学原理》(ArtisChemiaePrincipes)一书。许多希腊、阿拉伯、罗马的有名学者,例如帕拉图、阿里士多德、阿维森纳、给伯尔,都写了有关化学方面的书,在这方面最有力的证据乃是这些学者开始认识到实验是科学工作的重要工具。
(三)医药化学时期:在1500—1700年这两百年间,欧洲发生了很大的变化,科学史上称之为复兴时期。在这个时期欧洲出版了很多最早的化学著作,例如德国化学家格劳贝尔于1684年写的《新哲学的炉》;德国化学家孔柯尔写的《化学实验》;德国冶金学家阿格里柯拉写过一本名为“DeReMetallica”的书,中国明崇祯十六年李天经和汤若望将此书翻译出版,中文书名《坤舆格致》,可以说是中国最早翻译的化学书籍。
(四)燃素时期:这个时期从1650年到1775年,在这个时期出现了很多化学家,例如德国化学家施塔尔,他写过《化学基础》一书,是1723年出版的。还有德国化学家贝歇尔,他写过《冶金术》一书和很多其他著作。尽管他们的理论是不正确的,可是他们做了很多实验,积累了许多感性知识。一直到1661年,英国化学家波义耳写了《怀疑派化学家》一书,才开始对于元素理论有了基本的认识。
(五)定量时期:这个时期从1775年至1900年,这一时期化学研究的目的是开始利用化学知识解决工农业上的许多问题,并利用定量的化学实验建立了不少化学基本定律。这个时期又称为近代化学发展时期,很多科学家写了许多著名的书籍和论文,特别是英国化学家道尔顿在1808年所写的《化学哲学新体系》一书,提出了原子学说;法国化学家拉瓦锡於1777年发表《燃烧概论》论文,建立了燃烧作用的氧学说,并确立了物质不灭定律,使化学开始进入近代化学时期。接下来,瑞典化学家贝采里乌斯开始使用化学符号;俄国化学家门捷列夫发表周期律;德国化学家李比希和维勒在发展有机化学上作出了重要贡献,都为现代化学的发展奠定了基础。
(六)科学相互渗透时期:这个时期基本上从二十世纪初开始。一方面,物理学提出的量子论使化学和物理学有了共同的语言。另一方面化学又向生物学和地质学等学科渗透,使过去很难解决的蛋白质、酶等的结构问题,正在逐步得到解决。过去认为原子是看不见的,现在不但可以用超显微镜看到原子,而且原子本身的能量也已经开始被人们利用了。
物质中某元素的质量分数,就是该元素的质量与组成物质的各元素总质量之比。
公式:
某元素的质量分数=

如AmBn中A元素的质量分数=

若题目给出物质的化学式,又同时知道物质的实际质量,则可根据物质的质量×某元素的质量分数=该元素的质量,将其中所含元素的质量求出。同理,物质的质量=某元素质量÷该元素的质量分数。
公式的理解:
计算时应先列式计算,然后代入数据算出结果。如水中氢元素的质量分数=
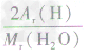 ×100%=
×100%= ×100%=
×100%= ×100%=11.1%而不能写成
×100%=11.1%而不能写成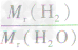 ×100%=
×100%= ×100%=
×100%= ×100%=11.1%
×100%=11.1%化学式中质量分数的应用:
①已知物质的质量求所含的某元素的质量
利用公式:元素的质量=物质的质量×该元素的质量分数
②已知元素的质量求物质的质量
利用公式:物质的质量=元素的质量÷该元素的质量分数
③根据元素的质量分数确定物质的化学式
利用化学式的变形比较元素质量分数的大小:
例:
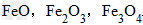 三种铁的氧化物按铁元素的质量分数由大到小排列的顺序为?
三种铁的氧化物按铁元素的质量分数由大到小排列的顺序为?解析:三种含铁的氧化物的化学式可变形为
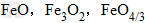 ,则三种含铁的氧化物中铁元素的质量分数分别为:
,则三种含铁的氧化物中铁元素的质量分数分别为: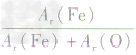 、
、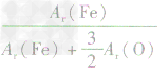 、
、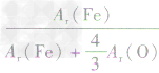 ,通过比较分母可知:
,通过比较分母可知: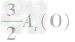 >
>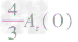 >Ar(O),故铁元素的质量分数由大到小排列的顺序为
>Ar(O),故铁元素的质量分数由大到小排列的顺序为 。
。化合价是元素的一种性质,它只有在元素彼此化合时才表现出来。在化合物中正、负化合价代数和等于零,这是求化合价的准则。
几种求法:
一、由化学式或根式
1.求AmBn化合物中A元素化合价的公式: (B元素的化合价×B的原子个数)/A的原子个数
2.求多元化合物中未知化合价的元素的化合价公式: (已知化合价诸元素价数的代数和)/未知化合价的元素的原子个数
3.根据正、负电荷数判断元素(或原子团)的化合价。 在根式中,正、负化合价总价数的代数和等于根式所带的正、负电荷数。
二、由元素质量比
1.(A元素的相对原子质量×B元素的化合价)/(B元素的相对原子质量×元素的化合价)=A元素的质量比值/B元素的质量比值
2.A元素的质量比值(或百分组成)×A的化合价/A的相对原子质量=B元素的质量比值(或百分比组成)×B的化合价/B相对原子质量
三、由质量比
(B的化合价×A的相对原子质量比值)/(A的化合价×B的相对原子质量比值)=A元素的质量比值/B元素的质量比值
正负代化合价数和为零:
【例1】试确定化合物K2MnO4中Mn元素的化合价。 解析:设化合物中Mn元素化合价为+x价,依化合物中各元素化合价正负代数和为零的原则有2×(+1)+1×(+x)+4×(-2)=0解之得x=6 故K2MnO4中Mn元素化合价为+6价。
电子层结构法
【例2】元素X的原子最外层上有1个电子,元素Y的原子最外层上有6个电子,则X、Y两元素可形成的化合物的化学式为[] A.XYB.X2YC.XY2D.X3Y 解析:本题的关键可以说是首先得确定在形成化合物时,X、Y两元素所表现的化合价。因X最外层上只有1个电子,最高正价为+1价,Y最外层6个电子,离8电子稳定结构尚差2个,故最低负价为-2价,则X、Y所形成化合物分子式为X2Y,应选B。
质量分数法
【例3】某元素的相对原子质量为59,在其氧化物中该元素的质量分数为71%,则它的化合价为[] A.+1B.+2C.+3D.+4 解析:设该元素的氧化物化学式为RxOy 依题意有59x/(59x+16y)*100%=71% 解得x/y=2:3 故化学式为R2O3,R化合价为+3价,选C。
质量守恒定律法
【例4】某金属氧化物与足量的盐酸反应,生成的氯化物与水的分子数之比为2∶3,则该金属的化合价是[] A.+1B.+2C.+3D.+4
解析:设生成的氯化物化学式为RClx,依题意有分子数之比RClx∶H2O=2∶3根据质量守恒定律可知,反应前后各元素的原子种类和数目不变,生成物中H、Cl的原子个数比也应为1:1,故x值为3,则R的化合价为+3价,选C。
相对分子质量法
【例5】某金属元素的氧化物相对分子质量为M,同价态的氯化物相对分子质量为N,则该元素的化合价数值为[]
解析:设该元素化合价为+x价,相对原子质量为MR
(1)如x为奇数时,氧化物化学式为R2Ox,氯化物化学式为RClx,据题意有
2MR+16x=M(1)
MR+35.5x=N(2)
(2)*2-(1)得x的值为x=+(2N-M)/55
(2)x为偶数时,氧化物化学式为Rox/2氯化物化学式为RClx,据题意有 MR+35.5x=N(4) x=+(N-M)/27.5
质量关系法
【例6】相对原子质量为M的金属单质ag与足量的稀硫酸反应,产生bg氢气,则反应中该金属元素的化合价为[]
解析:设金属在反应中化合价为+x价,则金属单质与生成H2有如下关系:
2R~xH2
2M 2x
a b
故应选B。
相关因素讨论法
【例7】某元素M原子最外层电子数少于5,其氧化物化学式为MxOy,氯化物化学式MClz当y∶z=1∶2时,M的化合价可能是[]
A.+1B.+2C.+3D.+4
解析:M的化合价在数值上等于z的值
如y=1z=2(合理) y=2z=4(合理) y=3z=6(与最外层电子数少于5不符) 故应选B、D。
地壳是由沙、黏土、岩石等组成的,其中含量最多的是氧元素,含量排在第二位至第五位的元素依次是硅、铝、铁、钙等。地壳中含量最高的非金属元素是氧元素;地壳中含量最高的金属元素是铝元素。(关键记清地壳中含量最高的前四位元素)
海水中元素分布:
海水中的元素分布海洋约占地球表面的70%左右,海水中的元素含量分布如下表所示。其中含量最多的是氧元素。其次是氢元素,这两种元素约占总量的96.5%。
| 元素 | O | H | Cl | Na、Mg |
| 质量分数/% | 85.5 | 10.7 | 2.0 | 1.5 |
人体中元素分布:
水占人体体重的70%左右。组成人体的元素中含最最多的是氧元索,其次是碳、氢、氮元素。碳,氢、氮三种元素在地壳中的含量较少,但却是生命的必需元素。
| 元素 | O | C | H | N | Ca | P | S、K |
| 质量分数/% | 65 | 18 | 10 | 3 | 1.5 | 1.0 | 1.5 |
与“小力同学对所学部分化学知识归纳如下,其中有错误的一组是( ...”考查相似的试题有:
- 以下是某加碘食盐包装袋上的部分文字说明,请仔细阅读后回答下列问题.配料表氯化钠、碘酸钾氯化钠含量(以NaCl计)≥98.0%碘...
- 《化学发展简史》一书中介绍的科学家,哪位发现了“元素周期律”和“元素周期表”( )A.牛顿B.道尔顿C.阿伏加德罗D.门捷列夫
- 人体内钠元素过量和缺乏都将导致生理疾病,医疗上常用的生理盐水是质量分数为0.9%(密度近似为1g/cm3)的氯化钠溶液,它是对...
- (3分)某些厂家为延长食品保质期,常在食品中添加苯甲酸(C6H5COOH)作为防腐剂。回答下列问题:(1)苯甲酸是由 种元素组成...
- 维生素C的化学式为CXHyO6,其相对分子质量为176,碳元素的质量分数为40.9%,问 x和 y的值(保留为整数)为多少?
- 2008年发生的毒奶粉事件,是不法分子在奶粉中掺入了不可食用的三聚氰胺而造成的.三聚氰胺的化学式为C3H6N6,其中氮元素的质...
- 某地每吨化肥的市场价格如下:尿素[CO(NH2)2]1080元;硝酸铵(NH4NO3)810元;碳酸氢铵(NH4HCO3)330元,某农民现有800元...
- “酒驾”是当前热门话题之一。交巡警检查驾驶员是否饮酒的仪器里装有K2Cr2O7,K2Cr2O7中Cr元素的化合价为[ ]A.+ 2价B.+5价C.+...
- 硒是抗衰老元素,能抑制癌细胞生长,硒酸根离子(SeO42-)中硒元素的化合价为( )A.+4B.+6C.-2D.-4
- 某化合物化学式为HnRO2n-1,若n=2时,R的化合价为______.